よむ、つかう、まなぶ。
総-3参考7 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_67369.html |
| 出典情報 | 中央社会保険医療協議会 総会(第636回 12/17)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
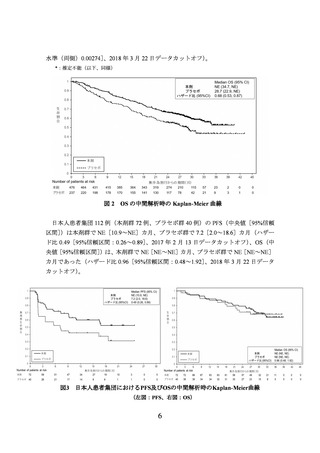
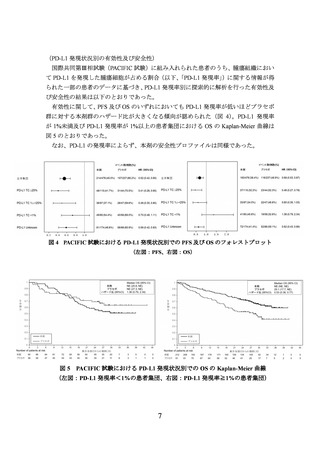
EFS 中央値 (月) [95% CI]
本剤併用群
NE [31.9~NE]
対照群
25.9 [18.9~NE]
ハザード比 [95%CI] 0.68 [0.53~0.88]
(2022 年 11 月 10 日データカットオフ)
at risk 数
本剤併用群 366
271
140
78
49
30
11
1
0
対照群
257
136
74
50
25
13
1
0
374
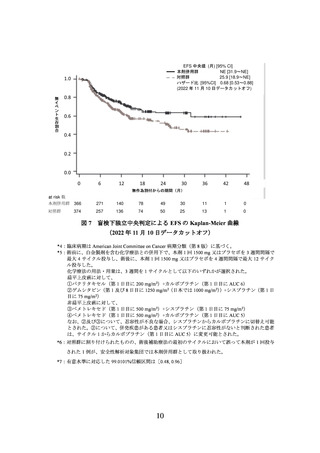
図 7 盲検下独立中央判定による EFS の Kaplan-Meier 曲線
(2022 年 11 月 10 日データカットオフ)
*4:臨床病期は American Joint Committee on Cancer 病期分類(第 8 版)に基づく。
*5:術前に、白金製剤を含む化学療法との併用下で、本剤 1 回 1500 mg 又はプラセボを 3 週間間隔で
最大 4 サイクル投与し、術後に、本剤 1 回 1500 mg 又はプラセボを 4 週間間隔で最大 12 サイク
ル投与した。
化学療法の用法・用量は、3 週間を 1 サイクルとして以下のいずれかが選択された。
扁平上皮癌に対して、
①パクリタキセル(第 1 日目に 200 mg/m2)+カルボプラチン(第 1 日目に AUC 6)
②ゲムシタビン(第 1 及び 8 日目に 1250 mg/m2(日本では 1000 mg/m2)
)+シスプラチン(第 1 日
目に 75 mg/m2)
非扁平上皮癌に対して、
③ペメトレキセド(第 1 日目に 500 mg/m2)+シスプラチン(第 1 日目に 75 mg/m2)
④ペメトレキセド(第 1 日目に 500 mg/m2)+カルボプラチン(第 1 日目に AUC 5)
なお、②及び③について、忍容性が不良な場合、シスプラチンからカルボプラチンに切替え可能
とされた。②について、併発疾患がある患者又はシスプラチンに忍容性がないと判断された患者
は、サイクル 1 からカルボプラチン(第 1 日目に AUC 5)に変更可能とされた。
*6:対照群に割り付けられたものの、術後補助療法の最初のサイクルにおいて誤って本剤が 1 回投与
された 1 例が、安全性解析対象集団では本剤併用群として取り扱われた。
*7:有意水準に対応した 99.0101%信頼区間は[0.48, 0.96]
10
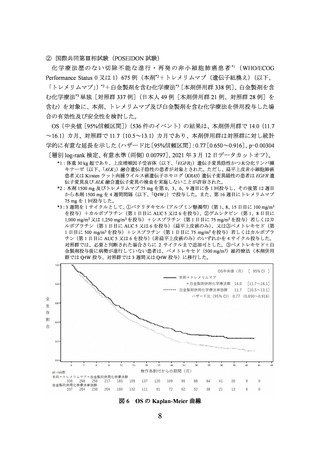
本剤併用群
NE [31.9~NE]
対照群
25.9 [18.9~NE]
ハザード比 [95%CI] 0.68 [0.53~0.88]
(2022 年 11 月 10 日データカットオフ)
at risk 数
本剤併用群 366
271
140
78
49
30
11
1
0
対照群
257
136
74
50
25
13
1
0
374
図 7 盲検下独立中央判定による EFS の Kaplan-Meier 曲線
(2022 年 11 月 10 日データカットオフ)
*4:臨床病期は American Joint Committee on Cancer 病期分類(第 8 版)に基づく。
*5:術前に、白金製剤を含む化学療法との併用下で、本剤 1 回 1500 mg 又はプラセボを 3 週間間隔で
最大 4 サイクル投与し、術後に、本剤 1 回 1500 mg 又はプラセボを 4 週間間隔で最大 12 サイク
ル投与した。
化学療法の用法・用量は、3 週間を 1 サイクルとして以下のいずれかが選択された。
扁平上皮癌に対して、
①パクリタキセル(第 1 日目に 200 mg/m2)+カルボプラチン(第 1 日目に AUC 6)
②ゲムシタビン(第 1 及び 8 日目に 1250 mg/m2(日本では 1000 mg/m2)
)+シスプラチン(第 1 日
目に 75 mg/m2)
非扁平上皮癌に対して、
③ペメトレキセド(第 1 日目に 500 mg/m2)+シスプラチン(第 1 日目に 75 mg/m2)
④ペメトレキセド(第 1 日目に 500 mg/m2)+カルボプラチン(第 1 日目に AUC 5)
なお、②及び③について、忍容性が不良な場合、シスプラチンからカルボプラチンに切替え可能
とされた。②について、併発疾患がある患者又はシスプラチンに忍容性がないと判断された患者
は、サイクル 1 からカルボプラチン(第 1 日目に AUC 5)に変更可能とされた。
*6:対照群に割り付けられたものの、術後補助療法の最初のサイクルにおいて誤って本剤が 1 回投与
された 1 例が、安全性解析対象集団では本剤併用群として取り扱われた。
*7:有意水準に対応した 99.0101%信頼区間は[0.48, 0.96]
10