よむ、つかう、まなぶ。
資料1-8 新規新型コロナワクチンを含むコホート調査並びに副反応シグナル全国調査[8.4MB] (89 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_39491.html |
| 出典情報 | 予防接種・ワクチン分科会副反応検討部会(第101回 4/15)医薬品等安全対策部会安全対策調査会(令和6年度第1回 4/15)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
5~11歳の小児を対象としたファイザー社ワクチン
(起源株1価、オミクロン株対応2価、XBB.1.5株対応1価)追加接種後 まとめ
•
•
•
•
•
•
•
•
•
•
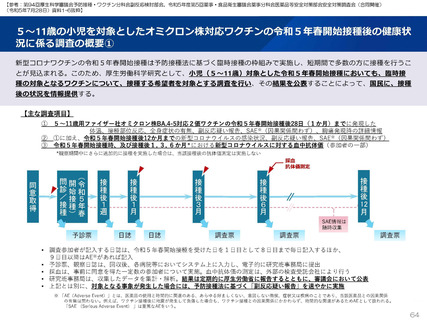
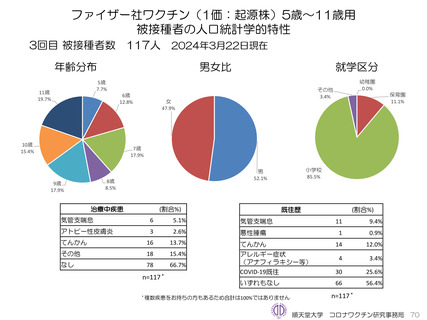
2022年8月30日に追加免疫の用法・用量が承認となり、2022年9月6日に3回目接種が臨時接種の対象となった新型コロナワ
クチンのファイザー社5~11歳用ワクチン(1価:起源株)を3回目接種した調査対象者に対し、2022年10月5日から調査を開
始した。2023年3月7日までに117人が3回目接種した。
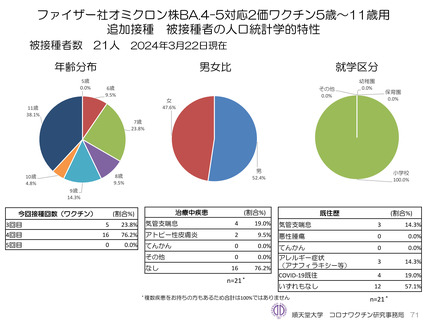
2023年2月28日に特例承認となり、2023年3月8日に臨時接種の対象となった新型コロナワクチンのファイザー社5~11歳用
オミクロン株対応2価ワクチン(起源株/オミクロン株BA.4-5)を追加接種した調査対象者に対し、2023年5月20日から調査
を開始した。2023年9月19日までに21人が追加接種した。
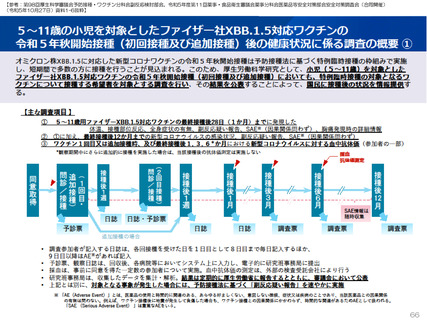
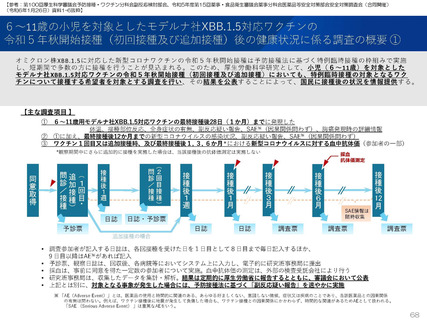
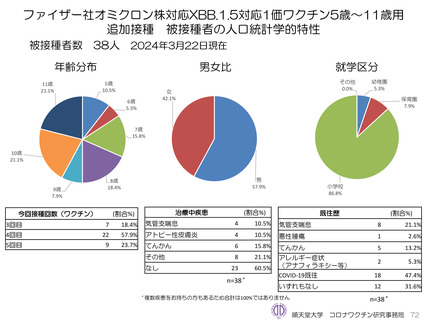
2023年7月25日に特例承認となり、2023年8月4日に臨時接種の対象となった新型コロナワクチンのファイザー社5~11歳用
オミクロン株XBB.1.5対応1価ワクチンを追加接種した調査対象者に対し、2023年11月10日から調査を開始した。2024年3
月22日までに38人が追加接種した。
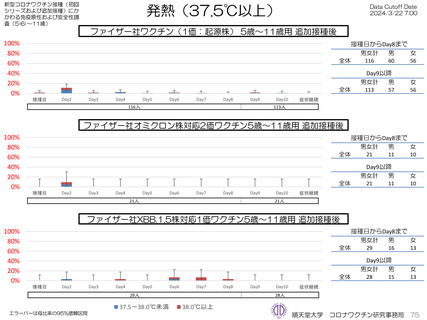
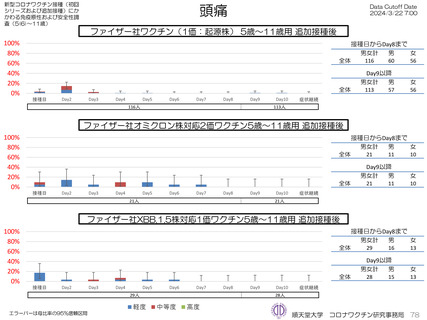
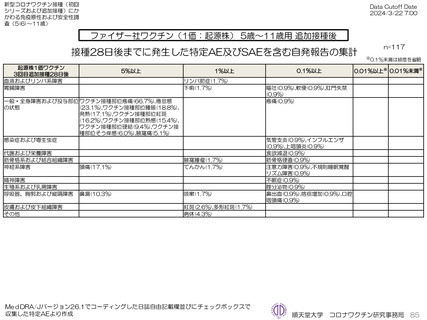
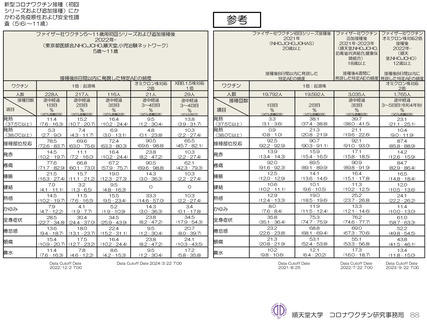
ファイザー社5~11歳用ワクチン(1価:起源株)3回目接種後1週間(Day8)までの日誌が回収できた116人では、37.5℃以
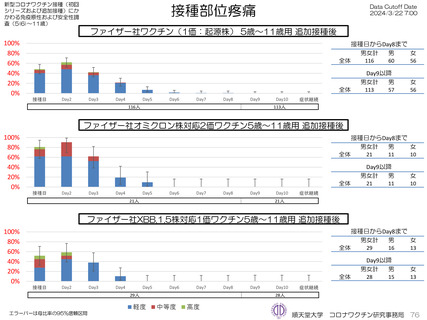
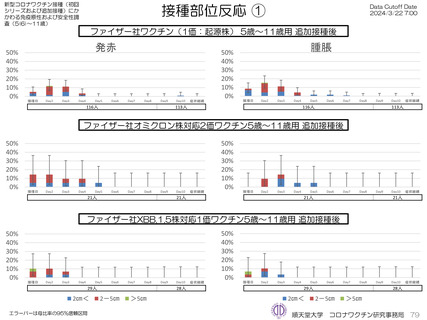
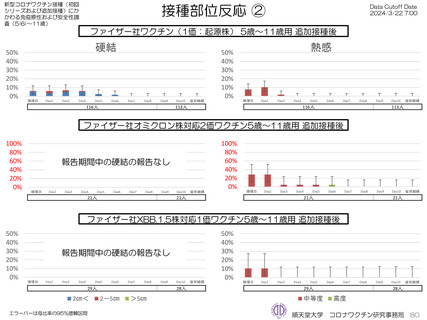
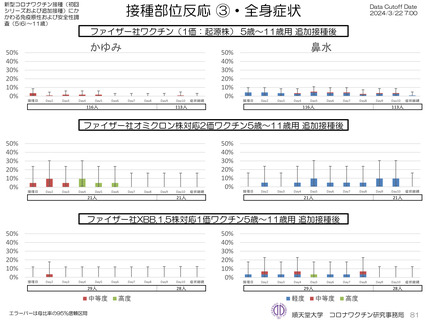
上の発熱が16.4%(38.0℃以上は6.9%)にみられ、局所反応は疼痛が67.2%にみられた。
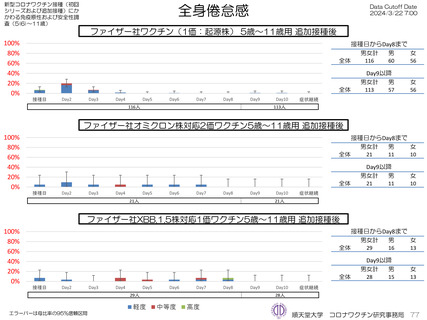
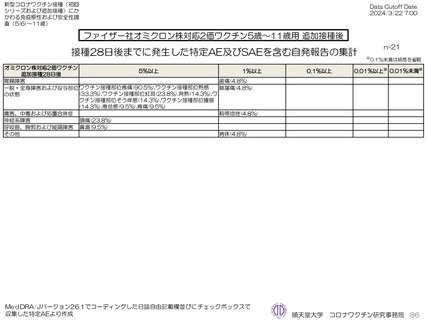
ファイザー社5~11歳用オミクロン株対応2価ワクチン(起源株/オミクロン株BA.4-5)追加接種後1週間(Day8)までの日誌
が回収できた21人では、37.5℃以上の発熱が9.5%(38.0℃以上は4.8%)にみられ、局所反応は疼痛が90.5%にみられた。安
全性情報は、ファイザー社5~11歳用ワクチン(1価:起源株)3回目追加接種と同様の傾向であったが、被接種者数は少ないの
で、有害事象の発生率などの解釈には留意が必要と考える。
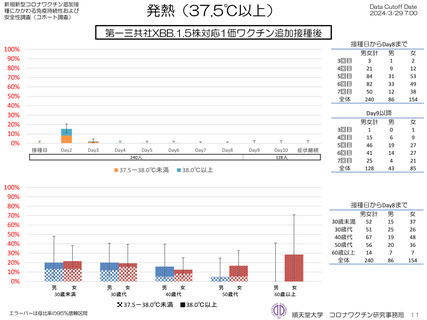
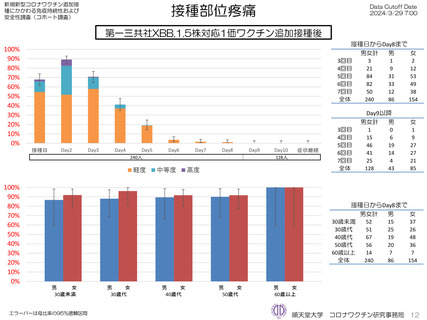
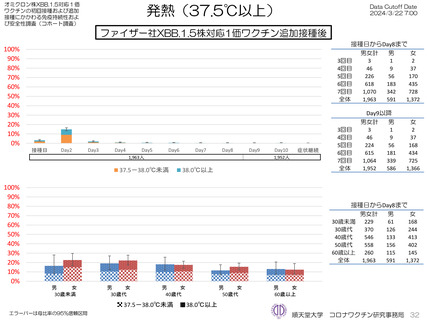
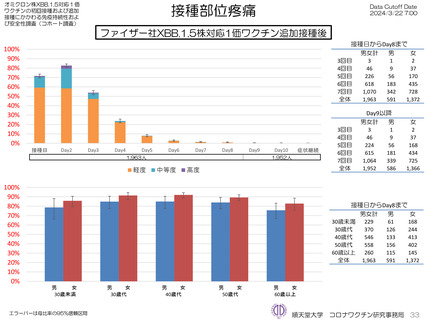
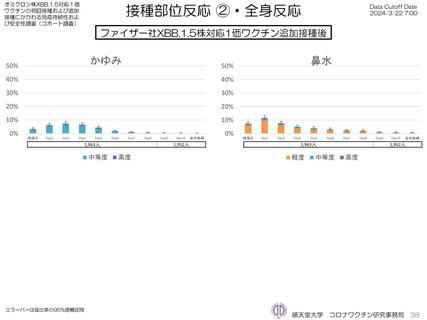
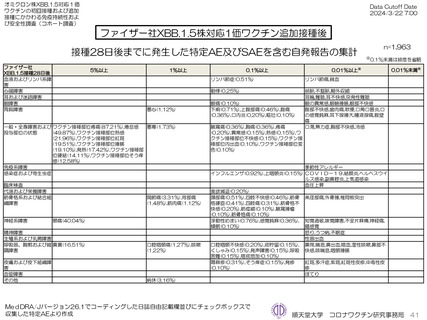
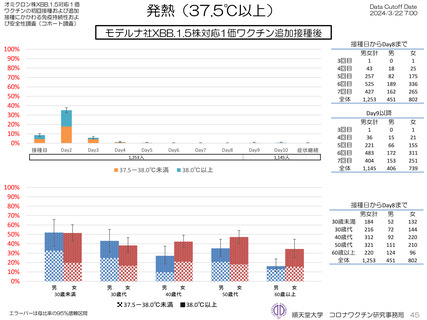
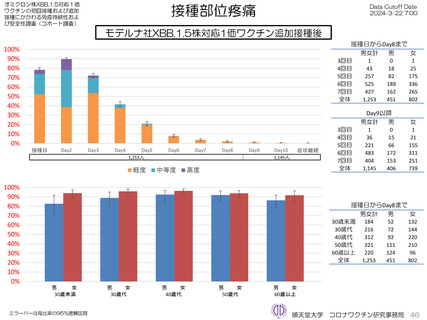
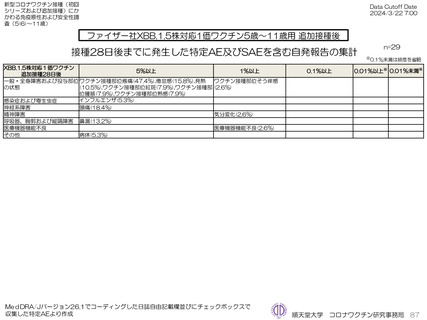
ファイザー社5~11歳用オミクロン株対応1価ワクチン(XBB.1.5)追加接種後1週間(Day8)までの日誌が回収できた29人で
は、37.5℃以上の発熱が13.8%(38.0℃以上は10.3%)にみられ、局所反応は疼痛が62.1%にみられた。安全性情報は、ファ
イザー社5~11歳用ワクチン(1価:起源株)3回目追加接種と同様の傾向であったが、被接種者数は少ないので、有害事象の発
生率などの解釈には留意が必要と考える。
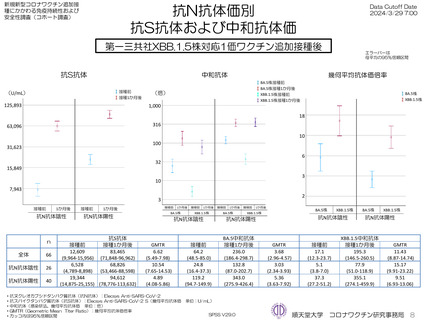
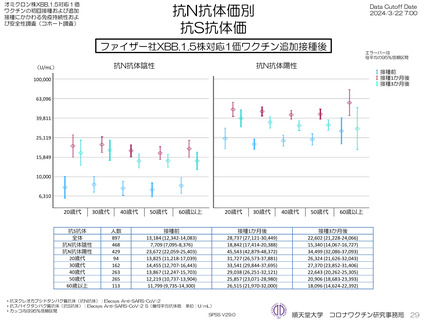
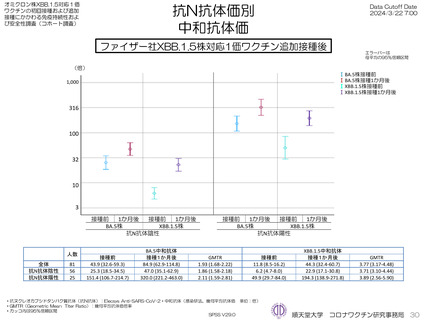
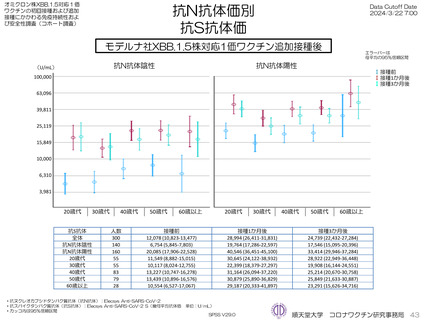
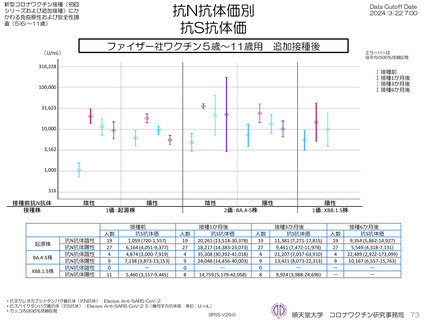
ファイザー社5~11歳用ワクチン(1価:起源株)を3回目接種し、抗体価を測定した46人の接種前の抗スパイクタンパク質幾
何平均抗体価(抗S抗体)は接種前の抗ヌクレオカプシドタンパク質抗体(抗N抗体)陰性者(19人)は1,059 U/mL、陽性者(27
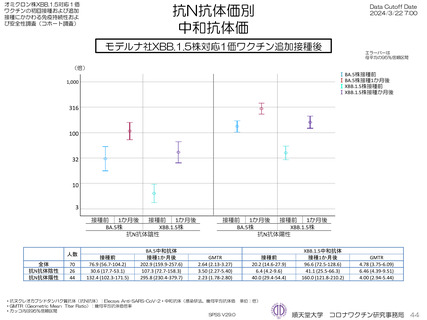
人)は6,164 U/mLと異なったが、接種1か月後から6か月後まで大きな違いは見られなかった。同様にオミクロン対応2価
(BA4-5株)の接種開始前から接種6か月まで、およびXBB.1.5株対応1価ワクチンの抗体価3か月までの抗体価推移に大きな
違いはみられなかった。
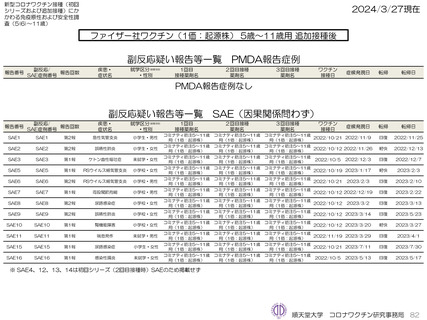
ファイザー社5~11歳用ワクチン(1価:起源株)3回目接種後では、因果関係を問わないSAEが12件認められている。PMDA
への副反応疑い報告は認められていない。
ファイザー社5~11歳用オミクロン株対応2価ワクチン(起源株/オミクロン株BA.4-5)接種後では、因果関係を問わないSAE、
PMDAへの副反応疑い報告は認められていない。
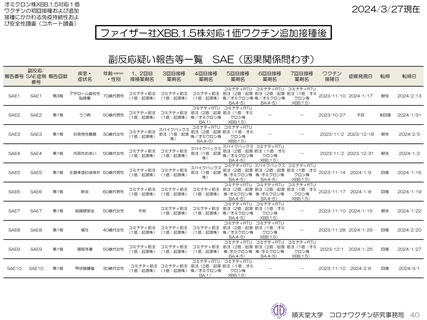
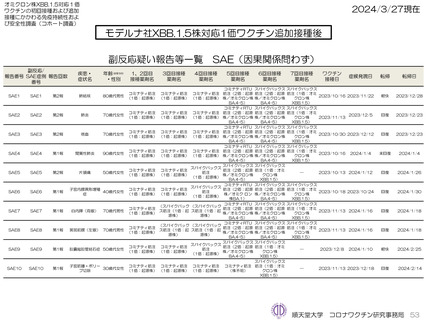
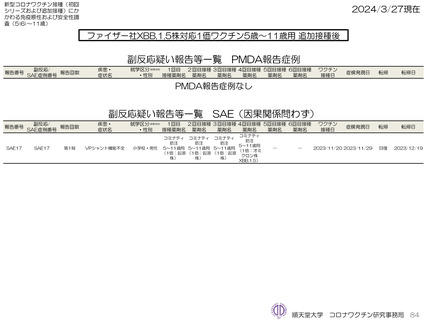
ファイザー社5~11歳用ワクチン(1価:XBB.1.5)3回目接種後では、因果関係を問わないSAEが1件認められている。PMDA
への副反応疑い報告は認められていない。
順天堂大学 コロナワクチン研究事務局 89
(起源株1価、オミクロン株対応2価、XBB.1.5株対応1価)追加接種後 まとめ
•
•
•
•
•
•
•
•
•
•
2022年8月30日に追加免疫の用法・用量が承認となり、2022年9月6日に3回目接種が臨時接種の対象となった新型コロナワ
クチンのファイザー社5~11歳用ワクチン(1価:起源株)を3回目接種した調査対象者に対し、2022年10月5日から調査を開
始した。2023年3月7日までに117人が3回目接種した。
2023年2月28日に特例承認となり、2023年3月8日に臨時接種の対象となった新型コロナワクチンのファイザー社5~11歳用
オミクロン株対応2価ワクチン(起源株/オミクロン株BA.4-5)を追加接種した調査対象者に対し、2023年5月20日から調査
を開始した。2023年9月19日までに21人が追加接種した。
2023年7月25日に特例承認となり、2023年8月4日に臨時接種の対象となった新型コロナワクチンのファイザー社5~11歳用
オミクロン株XBB.1.5対応1価ワクチンを追加接種した調査対象者に対し、2023年11月10日から調査を開始した。2024年3
月22日までに38人が追加接種した。
ファイザー社5~11歳用ワクチン(1価:起源株)3回目接種後1週間(Day8)までの日誌が回収できた116人では、37.5℃以
上の発熱が16.4%(38.0℃以上は6.9%)にみられ、局所反応は疼痛が67.2%にみられた。
ファイザー社5~11歳用オミクロン株対応2価ワクチン(起源株/オミクロン株BA.4-5)追加接種後1週間(Day8)までの日誌
が回収できた21人では、37.5℃以上の発熱が9.5%(38.0℃以上は4.8%)にみられ、局所反応は疼痛が90.5%にみられた。安
全性情報は、ファイザー社5~11歳用ワクチン(1価:起源株)3回目追加接種と同様の傾向であったが、被接種者数は少ないの
で、有害事象の発生率などの解釈には留意が必要と考える。
ファイザー社5~11歳用オミクロン株対応1価ワクチン(XBB.1.5)追加接種後1週間(Day8)までの日誌が回収できた29人で
は、37.5℃以上の発熱が13.8%(38.0℃以上は10.3%)にみられ、局所反応は疼痛が62.1%にみられた。安全性情報は、ファ
イザー社5~11歳用ワクチン(1価:起源株)3回目追加接種と同様の傾向であったが、被接種者数は少ないので、有害事象の発
生率などの解釈には留意が必要と考える。
ファイザー社5~11歳用ワクチン(1価:起源株)を3回目接種し、抗体価を測定した46人の接種前の抗スパイクタンパク質幾
何平均抗体価(抗S抗体)は接種前の抗ヌクレオカプシドタンパク質抗体(抗N抗体)陰性者(19人)は1,059 U/mL、陽性者(27
人)は6,164 U/mLと異なったが、接種1か月後から6か月後まで大きな違いは見られなかった。同様にオミクロン対応2価
(BA4-5株)の接種開始前から接種6か月まで、およびXBB.1.5株対応1価ワクチンの抗体価3か月までの抗体価推移に大きな
違いはみられなかった。
ファイザー社5~11歳用ワクチン(1価:起源株)3回目接種後では、因果関係を問わないSAEが12件認められている。PMDA
への副反応疑い報告は認められていない。
ファイザー社5~11歳用オミクロン株対応2価ワクチン(起源株/オミクロン株BA.4-5)接種後では、因果関係を問わないSAE、
PMDAへの副反応疑い報告は認められていない。
ファイザー社5~11歳用ワクチン(1価:XBB.1.5)3回目接種後では、因果関係を問わないSAEが1件認められている。PMDA
への副反応疑い報告は認められていない。
順天堂大学 コロナワクチン研究事務局 89