よむ、つかう、まなぶ。
資料1-8 新規新型コロナワクチンを含むコホート調査並びに副反応シグナル全国調査[8.4MB] (56 ページ)
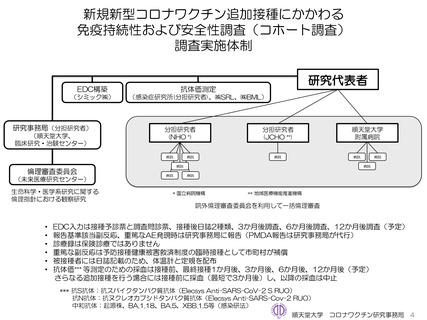
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_39491.html |
| 出典情報 | 予防接種・ワクチン分科会副反応検討部会(第101回 4/15)医薬品等安全対策部会安全対策調査会(令和6年度第1回 4/15)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ファイザー社及びモデルナ社
オミクロン株XBB.1.5対応1価ワクチン追加接種後 まとめ
•
•
•
•
•
•
•
•
•
•
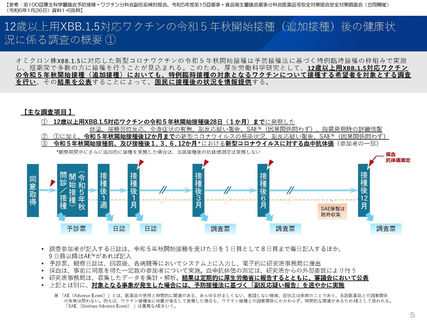
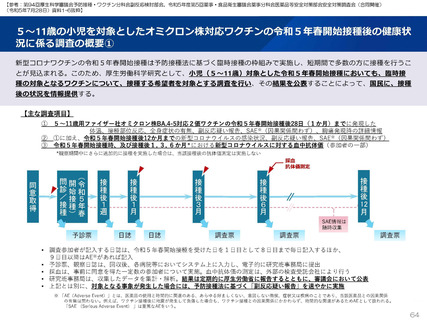
2023年9月1日に特例承認となり、2023年9月20日に臨時接種の対象となった新型コロナワクチンのファイザー社オミクロン株XBB.1.5対
応1価ワクチンを初回接種および追加接種した調査対象者に対し、2023年9月20日から調査を開始した。
2023年9月12日に特例承認となり、2023年9月25日に臨時接種の対象となった新型コロナワクチンのモデルナ社オミクロン株XBB.1.5対
応1価ワクチンを初回接種および追加接種した調査対象者に対し、2023年10月3日から調査を開始した。
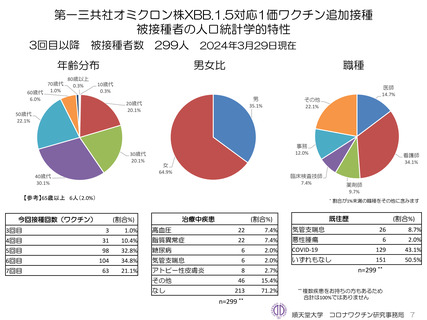
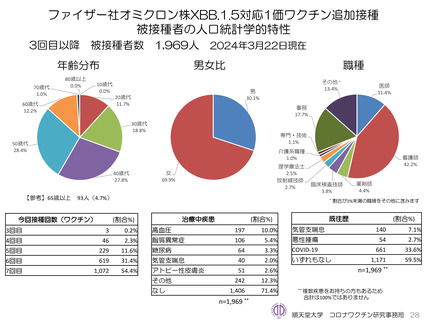
ファイザー社オミクロン株XBB.1.5対応1価ワクチンについて、3~7回目の追加接種について2023年9月29日から接種開始し、2024年3
月22日までに1,969人が追加接種した。なお、モデルナ社オミクロン株XBB.1.5対応1価ワクチンについては、 2023年10月13日から接
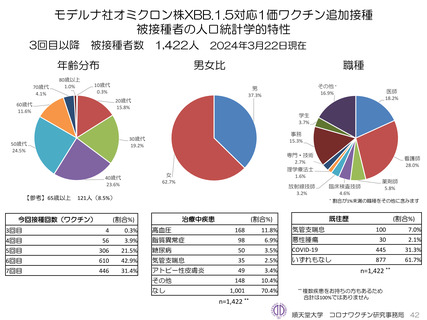
種開始し、2024年3月22日までに1,422人が追加接種した。いずれのワクチンでも初回接種となる調査対象者は登録されていない。
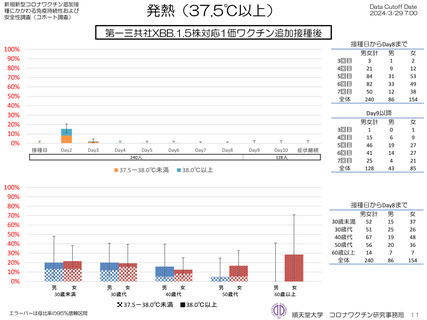
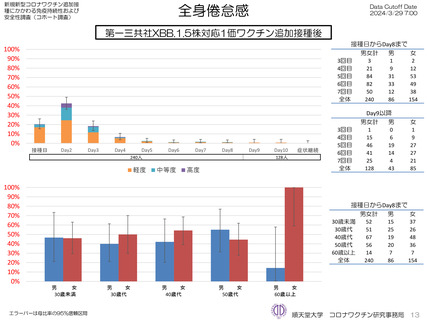
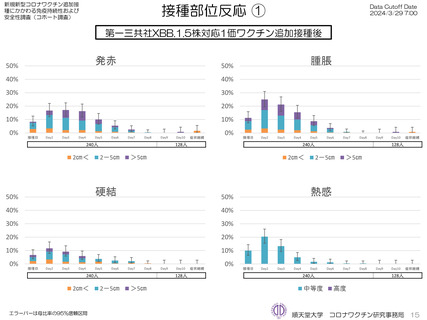
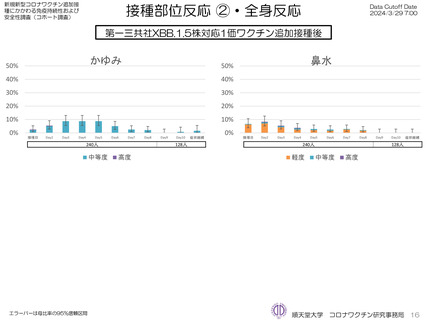
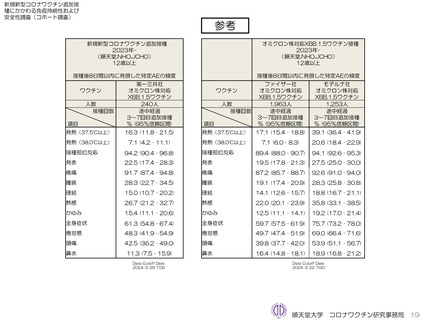
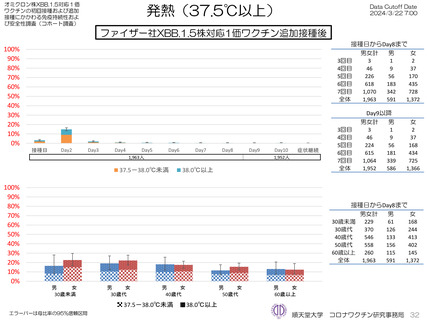
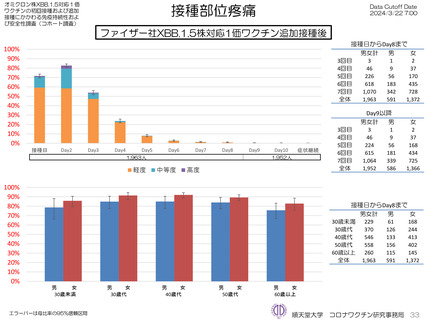
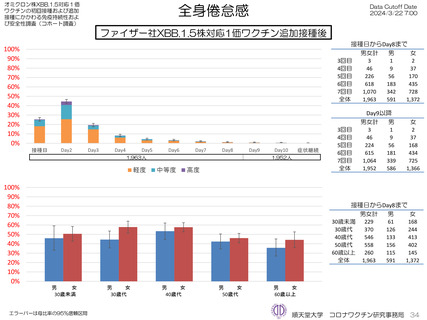
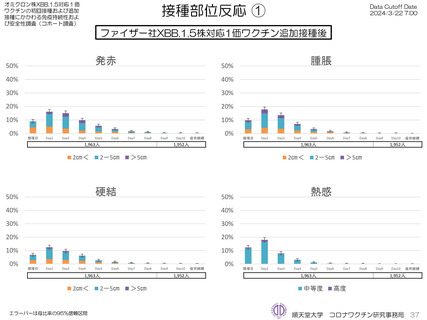
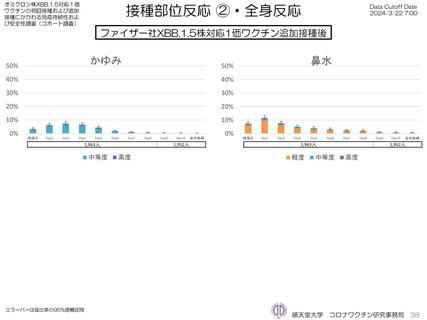
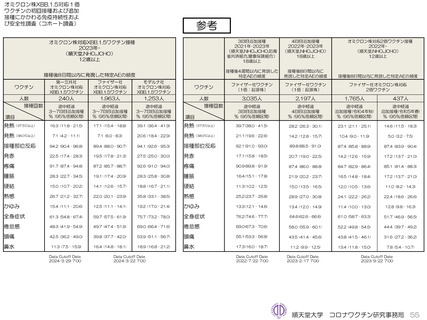
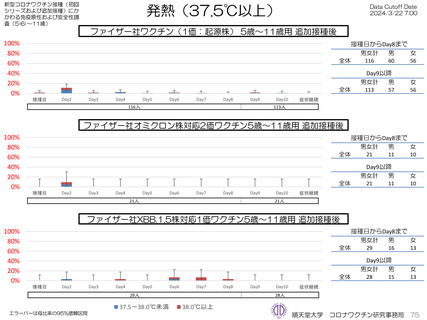
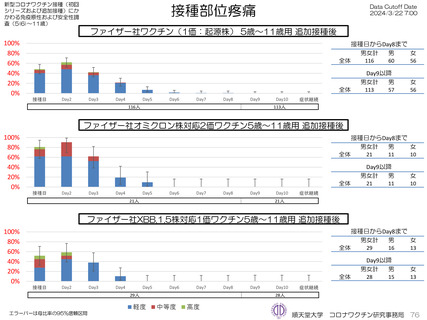
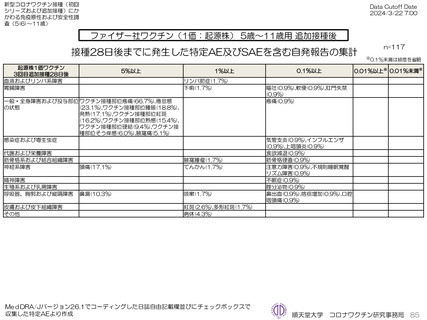
ファイザー社オミクロン株XBB.1.5対応1価ワクチンについて、追加接種後1週間(Day8)の日誌が回収できた1,963人では、37.5℃以上
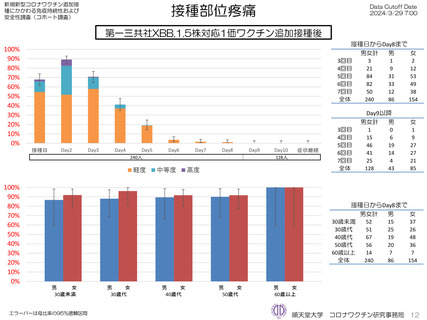
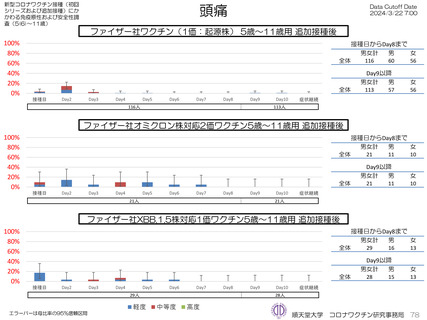
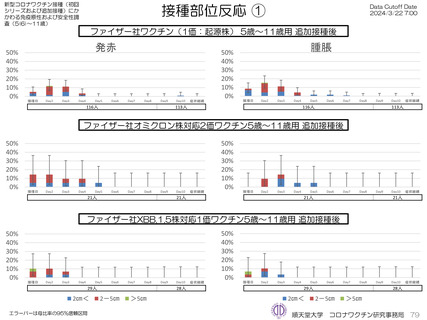
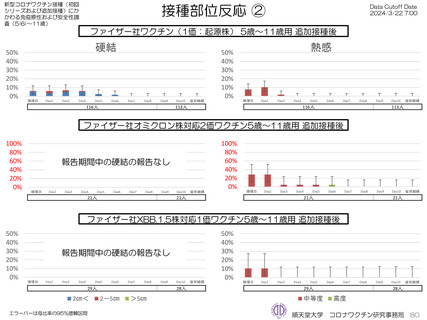
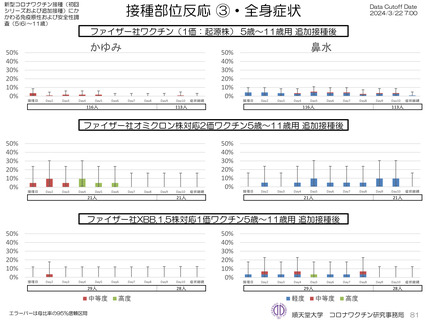
の発熱が17.1%(38.0℃以上は7.1%)にみられ、局所反応は疼痛が87.2%にみられた。
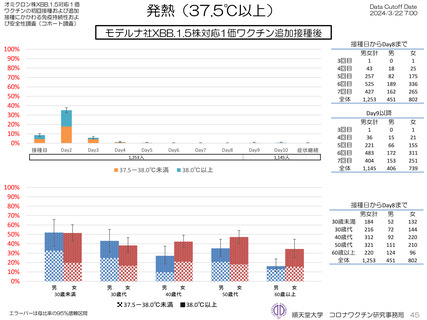
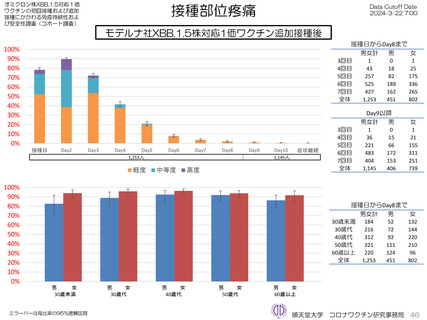
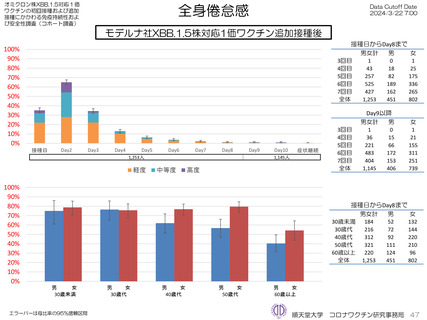
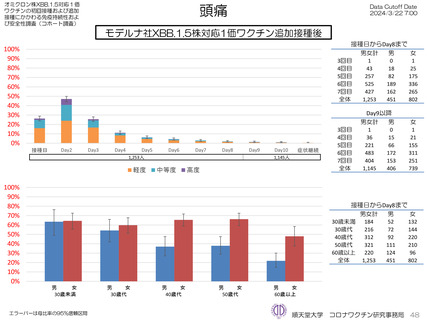
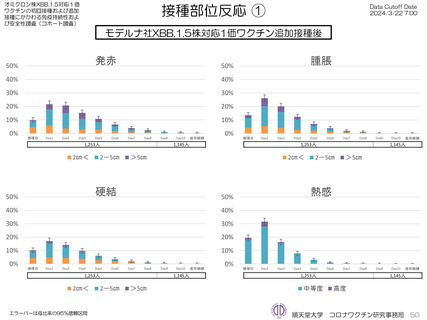
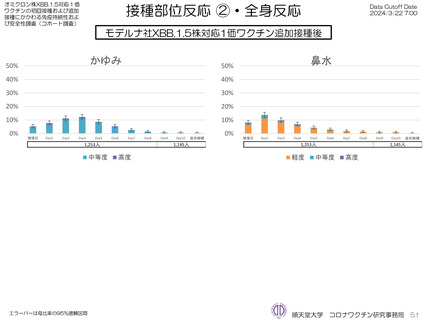
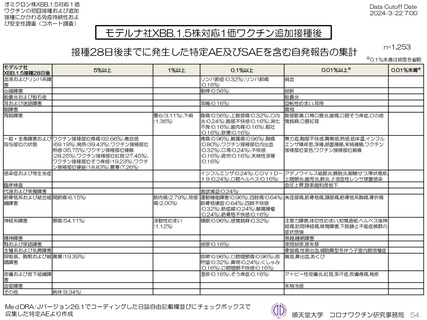
モデルナ社オミクロン株XBB.1.5対応1価ワクチンについて、追加接種後1週間(Day8)の日誌が回収できた1,251人では、37.5℃以上の
発熱が39.1%(38.0℃以上は20.6%)にみられ、局所反応は疼痛が92.6%にみられた。
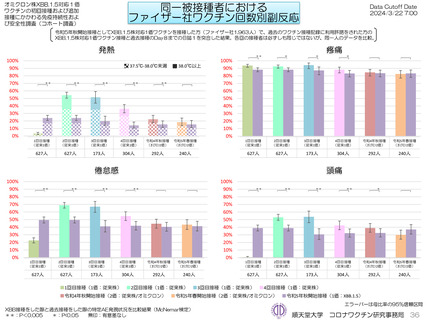
ファイザー社XBB.1.5対応1価ワクチンを接種した1,963人のうち、本コホート調査に参加してファイザー社ワクチンを接種した初回シリー
ズ627人、3回目接種173人、4回目接種304人、令和4年秋開始接種292人、令和5年春開始接種240人について、文書同意のもとに、過
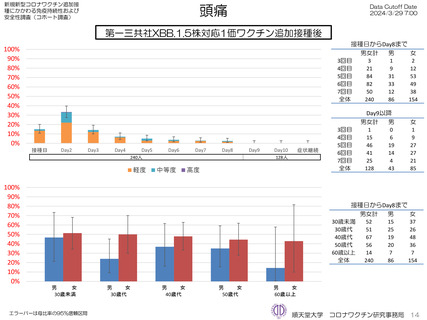
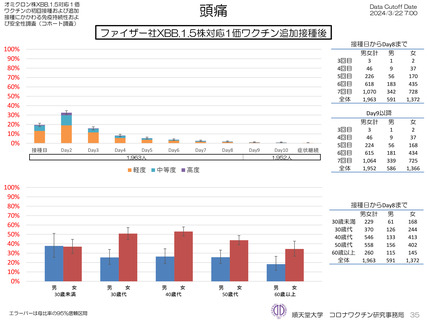
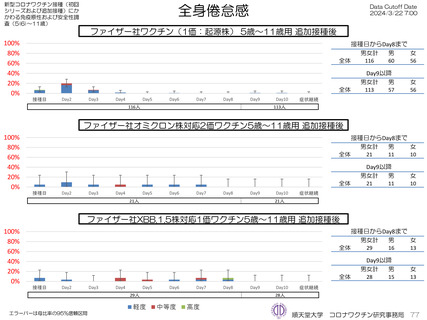
去の発熱、局所疼痛、倦怠感、頭痛について同一被接種者毎に比較した。その結果、XBB.1.5対応1価ワクチンは2回目から令和4年秋開始接
種に比べて発熱の頻度が低く、倦怠感、頭痛は2回目から4回目接種より頻度が低かった。1回目接種に比べて発熱、倦怠感、頭痛は頻度が高
く、局所の疼痛は1回目から4回目接種よりも頻度が低かったが、全体的に大きな違いは認めなかった。
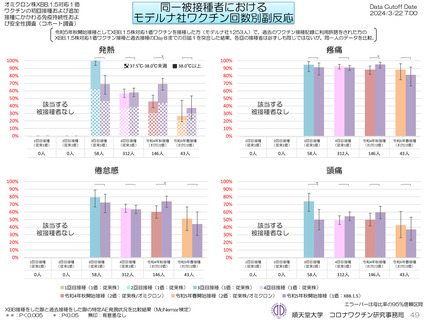
モデルナ社初回シリーズは自衛隊職員が対象であったため、モデルナ社XBB.1.5対応1価ワクチン接種と初回シリーズとの比較ができなかった
が、モデルナ社XBB.1.5対応1価ワクチンを接種した1,253人のうち、本コホート調査に参加してモデルナ社ワクチンを接種した、3回目接種
58人、4回目接種312人、令和4年秋開始接種146人、令和5年春開始接種43人について、文書同意のもとに、過去の発熱、局所疼痛、倦怠
感、頭痛について同一被接種者毎に比較した。その結果、XBB.1.5対応1価ワクチンは3回目接種に比べて頭痛の頻度が低く、令和4年秋開始
接種より発熱、倦怠感、頭痛の頻度が高かったが、局所疼痛の頻度は全体的に大きな違いは認めなかった。
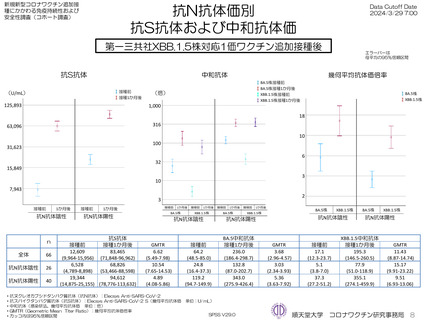
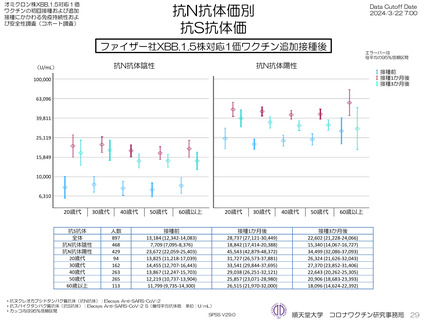
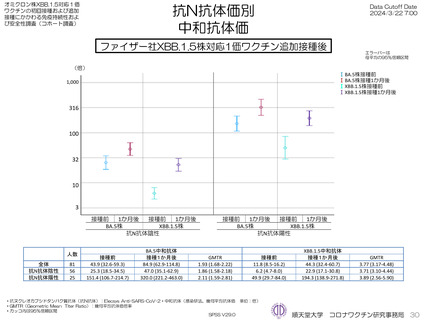
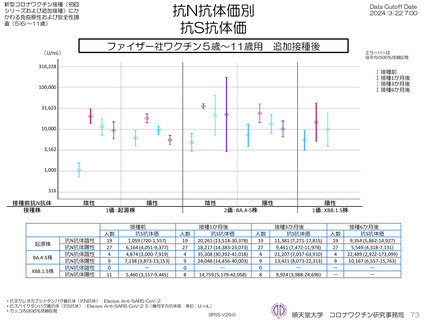
ファイザー社オミクロン株XBB.1.5対応1価ワクチンを接種し、接種3か月後までの採血結果のある897人の接種前および接種後の抗S抗体価
は接種前の抗ヌクレオカプシドタンパク質抗体(抗N抗体)価が陰性者は接種前7,709 U/mL、接種1か月後18,842 U/mL、接種3か月後
15,340 U/mLであった。抗N抗体陽性者は接種前23,672 U/mL、接種1か月後45,543 U/mL、接種3か月後34,499 U/mLと異なった
が、年齢階層別には大きな違いを認めなかった。接種前抗N抗体陰性者56例、陽性者26名のXBB.1.5中和抗体価は接種前および接種1か月後
で抗N抗体陰性者6.2倍→22.9倍、抗N抗体陽性者49.9倍→194.3倍であった(参考として測定したBA.5抗体価はそれぞれ25.3倍→47.0倍、
151.4倍→320倍であった)。XBB.1.5株に対する幾何抗体平均倍率は3.77倍であった。
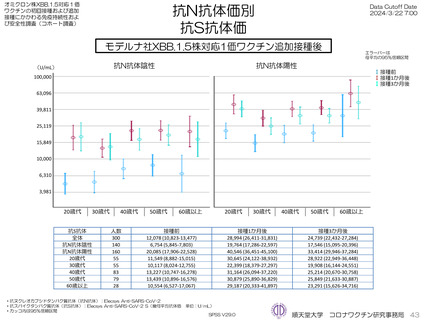
モデルナ社オミクロン株XBB.1.5対応1価ワクチンをを接種し、接種3か月後までの採血結果のある300人の接種前および接種後の抗S抗体価
は接種前の抗ヌクレオカプシドタンパク質抗体(抗N抗体)価が陰性者は接種前6,754 U/mL、接種1か月後19,7642 U/mL、接種3か月後
17,546 U/mLであった。抗N抗体陽性者は接種前20,085 U/mL、接種1か月後40,546 U/mL、接種3か月後33,414 U/mLと異なった
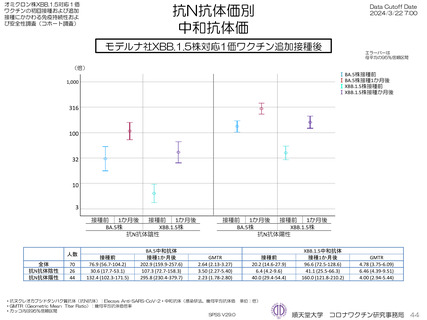
が、年齢階層別には大きな違いを認めなかった。接種前抗N抗体陰性者26例、陽性者44名のXBB.1.5中和抗体価は接種前および接種1か月後
で抗N抗体陰性者6.4倍→41.1倍、抗N抗体陽性者40.0倍→160.0倍であった(参考として測定したBA.5抗体価はそれぞれ30.6倍→107.3
倍、132.4倍→295.8倍であった)。XBB.1.5株に対する幾何抗体平均倍率は4.78倍であった。
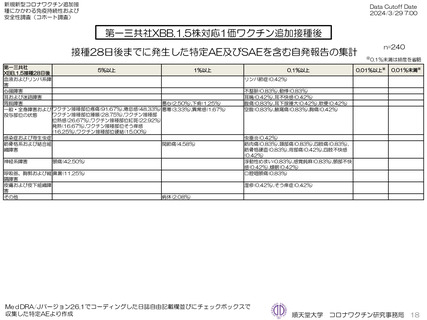
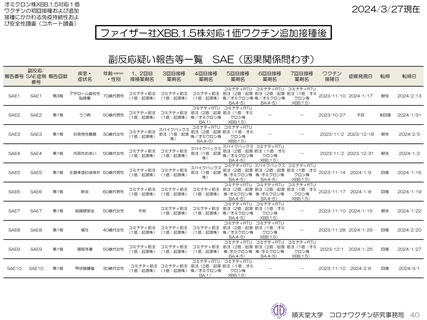
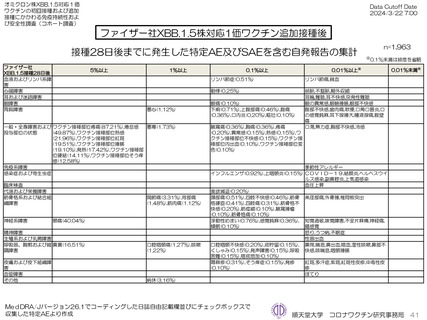
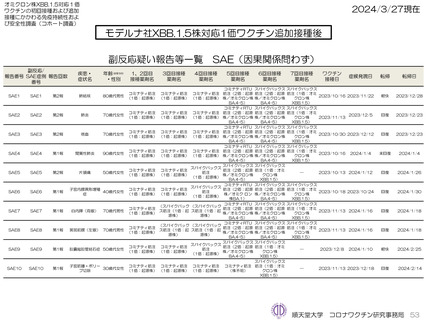
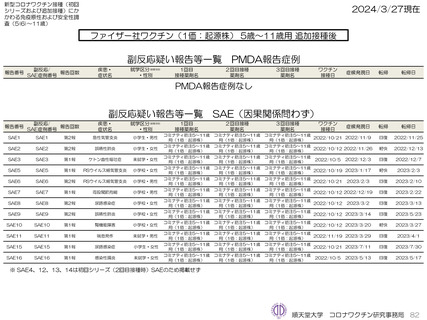
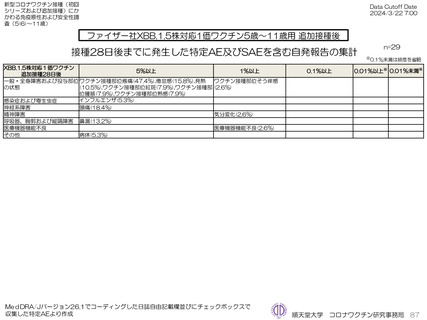
ファイザー社オミクロン株XBB.1.5対応1価ワクチン、モデルナ社オミクロン株XBB.1.5対応1価ワクチンいずれも、PMDAへの副反応疑い
報告は認められていない。ファイザー社オミクロン株XBB.1.5対応1価ワクチンにおいては10件、モデルナ社オミクロン株XBB.1.5対応1価
ワクチンにおいて8件の因果関係を問わないSAEが認められている。
順天堂大学 コロナワクチン研究事務局 56
オミクロン株XBB.1.5対応1価ワクチン追加接種後 まとめ
•
•
•
•
•
•
•
•
•
•
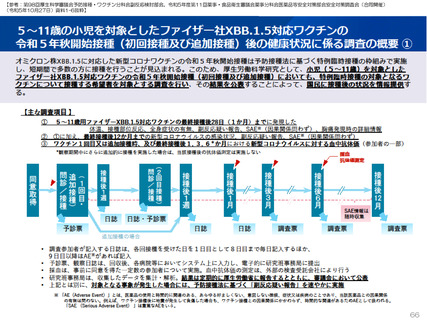
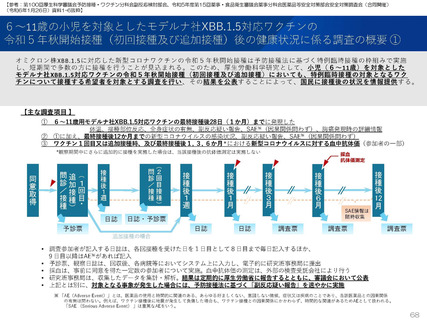
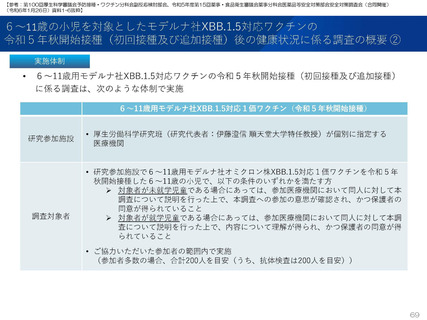
2023年9月1日に特例承認となり、2023年9月20日に臨時接種の対象となった新型コロナワクチンのファイザー社オミクロン株XBB.1.5対
応1価ワクチンを初回接種および追加接種した調査対象者に対し、2023年9月20日から調査を開始した。
2023年9月12日に特例承認となり、2023年9月25日に臨時接種の対象となった新型コロナワクチンのモデルナ社オミクロン株XBB.1.5対
応1価ワクチンを初回接種および追加接種した調査対象者に対し、2023年10月3日から調査を開始した。
ファイザー社オミクロン株XBB.1.5対応1価ワクチンについて、3~7回目の追加接種について2023年9月29日から接種開始し、2024年3
月22日までに1,969人が追加接種した。なお、モデルナ社オミクロン株XBB.1.5対応1価ワクチンについては、 2023年10月13日から接
種開始し、2024年3月22日までに1,422人が追加接種した。いずれのワクチンでも初回接種となる調査対象者は登録されていない。
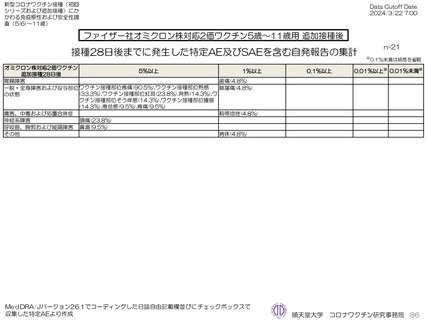
ファイザー社オミクロン株XBB.1.5対応1価ワクチンについて、追加接種後1週間(Day8)の日誌が回収できた1,963人では、37.5℃以上
の発熱が17.1%(38.0℃以上は7.1%)にみられ、局所反応は疼痛が87.2%にみられた。
モデルナ社オミクロン株XBB.1.5対応1価ワクチンについて、追加接種後1週間(Day8)の日誌が回収できた1,251人では、37.5℃以上の
発熱が39.1%(38.0℃以上は20.6%)にみられ、局所反応は疼痛が92.6%にみられた。
ファイザー社XBB.1.5対応1価ワクチンを接種した1,963人のうち、本コホート調査に参加してファイザー社ワクチンを接種した初回シリー
ズ627人、3回目接種173人、4回目接種304人、令和4年秋開始接種292人、令和5年春開始接種240人について、文書同意のもとに、過
去の発熱、局所疼痛、倦怠感、頭痛について同一被接種者毎に比較した。その結果、XBB.1.5対応1価ワクチンは2回目から令和4年秋開始接
種に比べて発熱の頻度が低く、倦怠感、頭痛は2回目から4回目接種より頻度が低かった。1回目接種に比べて発熱、倦怠感、頭痛は頻度が高
く、局所の疼痛は1回目から4回目接種よりも頻度が低かったが、全体的に大きな違いは認めなかった。
モデルナ社初回シリーズは自衛隊職員が対象であったため、モデルナ社XBB.1.5対応1価ワクチン接種と初回シリーズとの比較ができなかった
が、モデルナ社XBB.1.5対応1価ワクチンを接種した1,253人のうち、本コホート調査に参加してモデルナ社ワクチンを接種した、3回目接種
58人、4回目接種312人、令和4年秋開始接種146人、令和5年春開始接種43人について、文書同意のもとに、過去の発熱、局所疼痛、倦怠
感、頭痛について同一被接種者毎に比較した。その結果、XBB.1.5対応1価ワクチンは3回目接種に比べて頭痛の頻度が低く、令和4年秋開始
接種より発熱、倦怠感、頭痛の頻度が高かったが、局所疼痛の頻度は全体的に大きな違いは認めなかった。
ファイザー社オミクロン株XBB.1.5対応1価ワクチンを接種し、接種3か月後までの採血結果のある897人の接種前および接種後の抗S抗体価
は接種前の抗ヌクレオカプシドタンパク質抗体(抗N抗体)価が陰性者は接種前7,709 U/mL、接種1か月後18,842 U/mL、接種3か月後
15,340 U/mLであった。抗N抗体陽性者は接種前23,672 U/mL、接種1か月後45,543 U/mL、接種3か月後34,499 U/mLと異なった
が、年齢階層別には大きな違いを認めなかった。接種前抗N抗体陰性者56例、陽性者26名のXBB.1.5中和抗体価は接種前および接種1か月後
で抗N抗体陰性者6.2倍→22.9倍、抗N抗体陽性者49.9倍→194.3倍であった(参考として測定したBA.5抗体価はそれぞれ25.3倍→47.0倍、
151.4倍→320倍であった)。XBB.1.5株に対する幾何抗体平均倍率は3.77倍であった。
モデルナ社オミクロン株XBB.1.5対応1価ワクチンをを接種し、接種3か月後までの採血結果のある300人の接種前および接種後の抗S抗体価
は接種前の抗ヌクレオカプシドタンパク質抗体(抗N抗体)価が陰性者は接種前6,754 U/mL、接種1か月後19,7642 U/mL、接種3か月後
17,546 U/mLであった。抗N抗体陽性者は接種前20,085 U/mL、接種1か月後40,546 U/mL、接種3か月後33,414 U/mLと異なった
が、年齢階層別には大きな違いを認めなかった。接種前抗N抗体陰性者26例、陽性者44名のXBB.1.5中和抗体価は接種前および接種1か月後
で抗N抗体陰性者6.4倍→41.1倍、抗N抗体陽性者40.0倍→160.0倍であった(参考として測定したBA.5抗体価はそれぞれ30.6倍→107.3
倍、132.4倍→295.8倍であった)。XBB.1.5株に対する幾何抗体平均倍率は4.78倍であった。
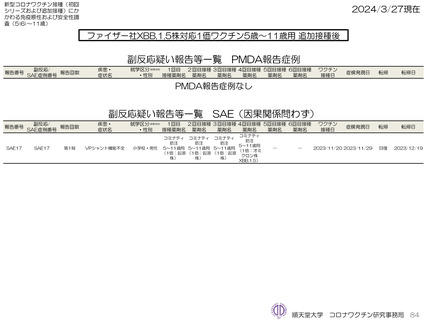
ファイザー社オミクロン株XBB.1.5対応1価ワクチン、モデルナ社オミクロン株XBB.1.5対応1価ワクチンいずれも、PMDAへの副反応疑い
報告は認められていない。ファイザー社オミクロン株XBB.1.5対応1価ワクチンにおいては10件、モデルナ社オミクロン株XBB.1.5対応1価
ワクチンにおいて8件の因果関係を問わないSAEが認められている。
順天堂大学 コロナワクチン研究事務局 56