よむ、つかう、まなぶ。
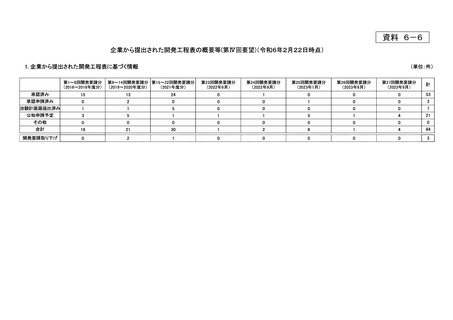
資料6-6 企業から提出された開発工程表の概要等(第IV回要望) (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00032.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第58回 3/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
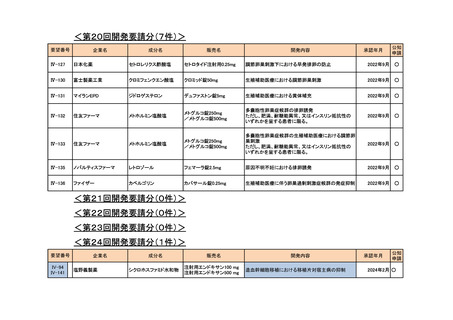
<第24回開発要請分(0件)>
<第25回開発要請分(0件)>
<第26回開発要請分(0件)>
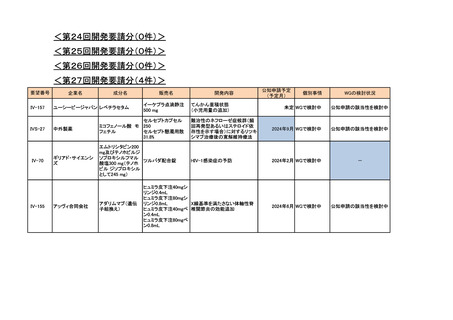
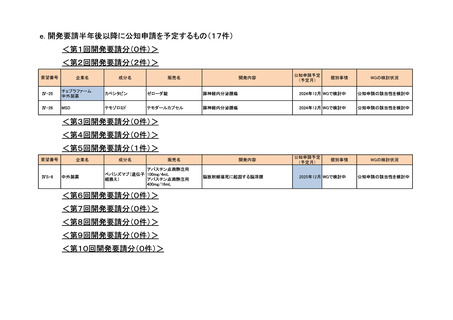
<第27回開発要請分(4件)>
要望番号
IV-157
IVS-27
IV-70
IV-155
企業名
成分名
ユーシービージャパン レベチラセタム
販売名
イーケプラ点滴静注
500 mg
開発内容
てんかん重積状態
(小児用量の追加)
公知申請予定
(予定月)
個別事情
WGの検討状況
未定 WGで検討中
公知申請の該当性を検討中
中外製薬
セルセプトカプセル
ミコフェノール酸 モ 250
フェチル
セルセプト懸濁用散
31.8%
難治性のネフローゼ症候群(頻
回再発型あるいはステロイド依
存性を示す場合)に対するリツキ
シマブ治療後の寛解維持療法
2024年9月 WGで検討中
公知申請の該当性を検討中
ギリアド・サイエンシ
ズ
エムトリシタビン200
mg及びテノホビルジ
ソプロキシルフマル
ツルバダ配合錠
酸塩300 mg(テノホ
ビル ジソプロキシル
として245 mg)
HIV-1感染症の予防
2024年2月 WGで検討中
-
2024年6月 WGで検討中
公知申請の該当性を検討中
アッヴィ合同会社
アダリムマブ(遺伝
子組換え)
ヒュミラ皮下注40mgシ
リンジ0.4mL
ヒュミラ皮下注80mgシ
リンジ0.8mL
X線基準を満たさない体軸性脊
ヒュミラ皮下注40mgペ 椎関節炎の効能追加
ン0.4mL
ヒュミラ皮下注80mgペ
ン0.8mL
202 / 213
<第25回開発要請分(0件)>
<第26回開発要請分(0件)>
<第27回開発要請分(4件)>
要望番号
IV-157
IVS-27
IV-70
IV-155
企業名
成分名
ユーシービージャパン レベチラセタム
販売名
イーケプラ点滴静注
500 mg
開発内容
てんかん重積状態
(小児用量の追加)
公知申請予定
(予定月)
個別事情
WGの検討状況
未定 WGで検討中
公知申請の該当性を検討中
中外製薬
セルセプトカプセル
ミコフェノール酸 モ 250
フェチル
セルセプト懸濁用散
31.8%
難治性のネフローゼ症候群(頻
回再発型あるいはステロイド依
存性を示す場合)に対するリツキ
シマブ治療後の寛解維持療法
2024年9月 WGで検討中
公知申請の該当性を検討中
ギリアド・サイエンシ
ズ
エムトリシタビン200
mg及びテノホビルジ
ソプロキシルフマル
ツルバダ配合錠
酸塩300 mg(テノホ
ビル ジソプロキシル
として245 mg)
HIV-1感染症の予防
2024年2月 WGで検討中
-
2024年6月 WGで検討中
公知申請の該当性を検討中
アッヴィ合同会社
アダリムマブ(遺伝
子組換え)
ヒュミラ皮下注40mgシ
リンジ0.4mL
ヒュミラ皮下注80mgシ
リンジ0.8mL
X線基準を満たさない体軸性脊
ヒュミラ皮下注40mgペ 椎関節炎の効能追加
ン0.4mL
ヒュミラ皮下注80mgペ
ン0.8mL
202 / 213