よむ、つかう、まなぶ。
資料2-1 令和3年度の安全対策について (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26332.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第1回 6/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
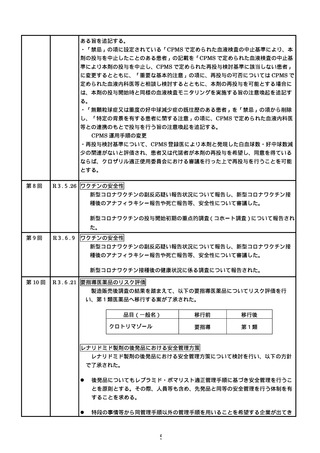
「血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)」の追加、
その報告期間として「28 日」とすることとし、新規に臨時接種の対象となった新型
コロナワクチンも含め同一の報告基準とすることについて審議し、了承された。
第 15 回※
R3.8.4 ワクチンの安全性
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、心筋炎・心膜炎報告等、安全性について
審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
○ 令和3年1月1日から令和3年3月 31 日までの麻しん、風しん、おたふくかぜ、水
痘、帯状疱疹、23 価肺炎球菌、HPV、百日せき、ジフテリア、破傷風、不活化ポリ
オ、7価、13 価肺炎球菌、Hib、BCG、日本脳炎、B型肝炎、ロタウイルスのワク
チン及び令和2年 10 月1日から令和3年3月 31 日までのインフルエンザワクチン
の副反応が疑われる症例の報告状況について審議した。
第 16 回※
R3.8.25 ワクチンの安全性
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、血小板減少を伴う血栓症の報告、心筋
炎・心膜炎報告等、安全性について審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
第 17 回※
R3.9.10 ワクチンの安全性
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、血小板減少を伴う血栓症の報告、心筋
炎・心膜炎報告、モデルナ筋注使用見合わせロットに係る副反応疑い報告等、安全
性について審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
第 18 回※
R3.10.1 ワクチンの安全性
○ HPV ワクチンの積極的勧奨の再開について審議した。
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、血小板減少を伴う血栓症の報告、心筋
炎・心膜炎報告、モデルナ筋注使用見合わせロットに係る副反応疑い報告、性・年
齢別解析等、安全性について審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
第 19 回※
R3.10.15 ワクチンの安全性
○ モデルナ社ワクチン接種後の若年男性における心筋炎・心膜炎の報告頻度が高いこ
とを踏まえ、ファイザー社ワクチン及びモデルナ社ワクチンの電子化された添付文
書の改訂等による情報提供の実施について審議し、了承された。
7
その報告期間として「28 日」とすることとし、新規に臨時接種の対象となった新型
コロナワクチンも含め同一の報告基準とすることについて審議し、了承された。
第 15 回※
R3.8.4 ワクチンの安全性
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、心筋炎・心膜炎報告等、安全性について
審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
○ 令和3年1月1日から令和3年3月 31 日までの麻しん、風しん、おたふくかぜ、水
痘、帯状疱疹、23 価肺炎球菌、HPV、百日せき、ジフテリア、破傷風、不活化ポリ
オ、7価、13 価肺炎球菌、Hib、BCG、日本脳炎、B型肝炎、ロタウイルスのワク
チン及び令和2年 10 月1日から令和3年3月 31 日までのインフルエンザワクチン
の副反応が疑われる症例の報告状況について審議した。
第 16 回※
R3.8.25 ワクチンの安全性
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、血小板減少を伴う血栓症の報告、心筋
炎・心膜炎報告等、安全性について審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
第 17 回※
R3.9.10 ワクチンの安全性
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、血小板減少を伴う血栓症の報告、心筋
炎・心膜炎報告、モデルナ筋注使用見合わせロットに係る副反応疑い報告等、安全
性について審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
第 18 回※
R3.10.1 ワクチンの安全性
○ HPV ワクチンの積極的勧奨の再開について審議した。
○ 新型コロナワクチンの副反応疑い報告状況について報告し、新型コロナワクチン接
種後のアナフィラキシー報告、死亡報告、血小板減少を伴う血栓症の報告、心筋
炎・心膜炎報告、モデルナ筋注使用見合わせロットに係る副反応疑い報告、性・年
齢別解析等、安全性について審議した。
○ 新型コロナワクチン接種後の健康状況に係る調査について報告された。
第 19 回※
R3.10.15 ワクチンの安全性
○ モデルナ社ワクチン接種後の若年男性における心筋炎・心膜炎の報告頻度が高いこ
とを踏まえ、ファイザー社ワクチン及びモデルナ社ワクチンの電子化された添付文
書の改訂等による情報提供の実施について審議し、了承された。
7