よむ、つかう、まなぶ。
総-4-1最適使用推進ガイドライン(デペモキマブ(気管支喘息)) (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72294.html |
| 出典情報 | 中央社会保険医療協議会 総会(第649回 4/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
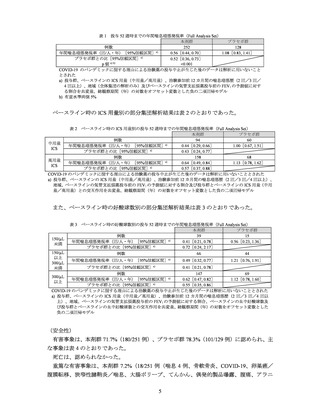
表 1 投与 52 週時までの年間喘息増悪発現率(Full Analysis Set)
本剤群
プラセボ群
例数
252
128
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.56[0.44, 0.70]
1.08[0.83, 1.41]
プラセボ群との比[95%信頼区間]a)
0.52[0.36, 0.73]
p 値 a) b)
<0.001
COVID-19 のパンデミックに関する理由による治験薬の投与中止が生じた後のデータは解析に用いないこと
とされた
a) 投与群、ベースラインの ICS 用量(中用量/高用量)、治験参加前 12 カ月間の喘息増悪歴(2 回/3 回/
4 回以上)、地域(全体集団の解析のみ)及びベースラインの気管支拡張薬投与前の FEV1 の予測値に対す
る割合を共変量、総観察期間(年)の対数をオフセット変数とした負の二項回帰モデル
b) 有意水準両側 5%
ベースライン時の ICS 用量別の部分集団解析結果は表 2 のとおりであった。
表 2 ベースライン時の ICS 用量別の投与 52 週時までの年間喘息増悪発現率(Full Analysis Set)
本剤群
プラセボ群
例数
94
60
中用量
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.44[0.29, 0.66]
1.00[0.67, 1.51]
ICS
プラセボ群との比[95%信頼区間]a)
0.43[0.24, 0.77]
例数
158
68
高用量
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.64[0.49, 0.84]
1.13[0.78, 1.62]
ICS
プラセボ群との比[95%信頼区間]a)
0.57[0.37, 0.88]
COVID-19 のパンデミックに関する理由による治験薬の投与中止が生じた後のデータは解析に用いないこととされた
a) 投与群、ベースラインの ICS 用量(中用量/高用量)、治験参加前 12 カ月間の喘息増悪歴(2 回/3 回/4 回以上)、
地域、ベースラインの気管支拡張薬投与前の FEV1 の予測値に対する割合及び投与群とベースラインの ICS 用量(中用
量/高用量)との交互作用を共変量、総観察期間(年)の対数をオフセット変数とした負の二項回帰モデル
また、ベースライン時の好酸球数別の部分集団解析結果は表 3 のとおりであった。
150/µL
未満
150/µL
以上
300/µL
未満
表 3 ベースライン時の好酸球数別の投与 52 週時までの年間喘息増悪発現率(Full Analysis Set)
本剤群
プラセボ群
例数
39
15
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.41[0.21, 0.78]
0.56[0.23, 1.36]
プラセボ群との比[95%信頼区間]a)
0.72[0.24, 2.17]
例数
66
44
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.49[0.32, 0.77]
1.21[0.76, 1.91]
プラセボ群との比[95%信頼区間]a)
0.41[0.21, 0.78]
例数
147
69
300/µL
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.62[0.47, 0.82]
1.12[0.78, 1.60]
以上
プラセボ群との比[95%信頼区間]a)
0.55[0.35, 0.86]
COVID-19 のパンデミックに関する理由による治験薬の投与中止が生じた後のデータは解析に用いないこととされた
a) 投与群、ベースラインの ICS 用量(中用量/高用量)、治験参加前 12 カ月間の喘息増悪歴(2 回/3 回/4 回以
上)、地域、ベースラインの気管支拡張薬投与前の FEV1 の予測値に対する割合、ベースラインの血中好酸球数及
び投与群とベースラインの血中好酸球数との交互作用を共変量、総観察期間(年)の対数をオフセット変数とした
負の二項回帰モデル
(安全性)
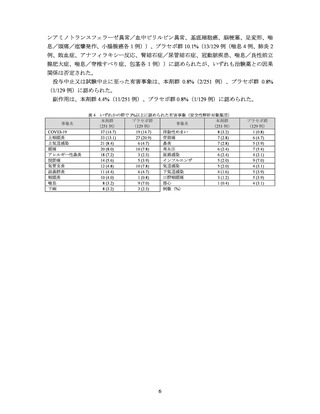
有害事象は、本剤群 71.7%(180/251 例)、プラセボ群 78.3%(101/129 例)に認められ、主
な事象は表 4 のとおりであった。
死亡は、認められなかった。
重篤な有害事象は、本剤群 7.2%(18/251 例(喘息 4 例、骨軟骨炎、COVID-19、卵巣癌/
腹膜転移、狭窄性腱鞘炎/喘息、大腸ポリープ、てんかん、偶発的製品曝露、腹痛、アラニ
5
本剤群
プラセボ群
例数
252
128
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.56[0.44, 0.70]
1.08[0.83, 1.41]
プラセボ群との比[95%信頼区間]a)
0.52[0.36, 0.73]
p 値 a) b)
<0.001
COVID-19 のパンデミックに関する理由による治験薬の投与中止が生じた後のデータは解析に用いないこと
とされた
a) 投与群、ベースラインの ICS 用量(中用量/高用量)、治験参加前 12 カ月間の喘息増悪歴(2 回/3 回/
4 回以上)、地域(全体集団の解析のみ)及びベースラインの気管支拡張薬投与前の FEV1 の予測値に対す
る割合を共変量、総観察期間(年)の対数をオフセット変数とした負の二項回帰モデル
b) 有意水準両側 5%
ベースライン時の ICS 用量別の部分集団解析結果は表 2 のとおりであった。
表 2 ベースライン時の ICS 用量別の投与 52 週時までの年間喘息増悪発現率(Full Analysis Set)
本剤群
プラセボ群
例数
94
60
中用量
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.44[0.29, 0.66]
1.00[0.67, 1.51]
ICS
プラセボ群との比[95%信頼区間]a)
0.43[0.24, 0.77]
例数
158
68
高用量
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.64[0.49, 0.84]
1.13[0.78, 1.62]
ICS
プラセボ群との比[95%信頼区間]a)
0.57[0.37, 0.88]
COVID-19 のパンデミックに関する理由による治験薬の投与中止が生じた後のデータは解析に用いないこととされた
a) 投与群、ベースラインの ICS 用量(中用量/高用量)、治験参加前 12 カ月間の喘息増悪歴(2 回/3 回/4 回以上)、
地域、ベースラインの気管支拡張薬投与前の FEV1 の予測値に対する割合及び投与群とベースラインの ICS 用量(中用
量/高用量)との交互作用を共変量、総観察期間(年)の対数をオフセット変数とした負の二項回帰モデル
また、ベースライン時の好酸球数別の部分集団解析結果は表 3 のとおりであった。
150/µL
未満
150/µL
以上
300/µL
未満
表 3 ベースライン時の好酸球数別の投与 52 週時までの年間喘息増悪発現率(Full Analysis Set)
本剤群
プラセボ群
例数
39
15
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.41[0.21, 0.78]
0.56[0.23, 1.36]
プラセボ群との比[95%信頼区間]a)
0.72[0.24, 2.17]
例数
66
44
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.49[0.32, 0.77]
1.21[0.76, 1.91]
プラセボ群との比[95%信頼区間]a)
0.41[0.21, 0.78]
例数
147
69
300/µL
年間喘息増悪発現率(回/人・年)[95%信頼区間]a)
0.62[0.47, 0.82]
1.12[0.78, 1.60]
以上
プラセボ群との比[95%信頼区間]a)
0.55[0.35, 0.86]
COVID-19 のパンデミックに関する理由による治験薬の投与中止が生じた後のデータは解析に用いないこととされた
a) 投与群、ベースラインの ICS 用量(中用量/高用量)、治験参加前 12 カ月間の喘息増悪歴(2 回/3 回/4 回以
上)、地域、ベースラインの気管支拡張薬投与前の FEV1 の予測値に対する割合、ベースラインの血中好酸球数及
び投与群とベースラインの血中好酸球数との交互作用を共変量、総観察期間(年)の対数をオフセット変数とした
負の二項回帰モデル
(安全性)
有害事象は、本剤群 71.7%(180/251 例)、プラセボ群 78.3%(101/129 例)に認められ、主
な事象は表 4 のとおりであった。
死亡は、認められなかった。
重篤な有害事象は、本剤群 7.2%(18/251 例(喘息 4 例、骨軟骨炎、COVID-19、卵巣癌/
腹膜転移、狭窄性腱鞘炎/喘息、大腸ポリープ、てんかん、偶発的製品曝露、腹痛、アラニ
5