よむ、つかう、まなぶ。
資料1 がんゲノム医療に係る取組について (26 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71567.html |
| 出典情報 | がんゲノム医療中核拠点病院等の指定要件に関するワーキンググループ(第7回 3/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
現在実施可能な標準治療終了前パネル検査を利用した先進医療Aについて
•
令和7年10月3日に開催された第147回先進医療会議で審議された本先進医療Aの概要は以下のとおり。
•
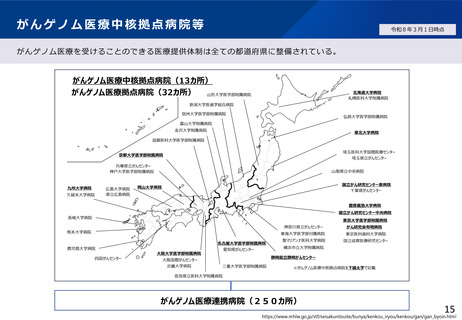
令和8年1月1日の告示後、全国のがんゲノム医療中核拠点病院等(令和8年3月1日現在計295施設)のうち、厚生局へ
届出を行い受理された施設で実施可能となっている。
先進医療の概要
• 先進医療技術名:標準治療終了前におけるがんゲノムプロファイリング検査
• 適応症:進行再発固形がん
• 試験名:進行または再発した固形がん患者に対して標準治療終了前に実施するCGP検査の臨床的有用性を評価する前向き研究
• 試験デザイン:単群前向き研究
• 期間:5年6ヶ月
• 主要評価項目:本試験で実施したCGP検査結果で検出された治療標的となる遺伝子異常(=actionableな遺伝子異常)に対応する分
子標的治療を受ける患者の割合(コンパニオン診断を含む)
• 副次評価項目:
(1)本試験で実施したCGP検査結果で検出された、
-actionableな遺伝子異常に対応する分子標的治療が推奨された患者の割合(コンパニオン診断を含む)
-actionableな遺伝子異常に対応する分子標的治療を行う治験への登録割合
-診断に有用な遺伝子異常が検出された患者の割合
(2)全生存期間
実施医療機関の要件
厚生労働大臣が指定するがんゲノム医療中核拠点病院・拠点病院・連携病院のいずれかであること等。
出典:001573497.pdf
26
•
令和7年10月3日に開催された第147回先進医療会議で審議された本先進医療Aの概要は以下のとおり。
•
令和8年1月1日の告示後、全国のがんゲノム医療中核拠点病院等(令和8年3月1日現在計295施設)のうち、厚生局へ
届出を行い受理された施設で実施可能となっている。
先進医療の概要
• 先進医療技術名:標準治療終了前におけるがんゲノムプロファイリング検査
• 適応症:進行再発固形がん
• 試験名:進行または再発した固形がん患者に対して標準治療終了前に実施するCGP検査の臨床的有用性を評価する前向き研究
• 試験デザイン:単群前向き研究
• 期間:5年6ヶ月
• 主要評価項目:本試験で実施したCGP検査結果で検出された治療標的となる遺伝子異常(=actionableな遺伝子異常)に対応する分
子標的治療を受ける患者の割合(コンパニオン診断を含む)
• 副次評価項目:
(1)本試験で実施したCGP検査結果で検出された、
-actionableな遺伝子異常に対応する分子標的治療が推奨された患者の割合(コンパニオン診断を含む)
-actionableな遺伝子異常に対応する分子標的治療を行う治験への登録割合
-診断に有用な遺伝子異常が検出された患者の割合
(2)全生存期間
実施医療機関の要件
厚生労働大臣が指定するがんゲノム医療中核拠点病院・拠点病院・連携病院のいずれかであること等。
出典:001573497.pdf
26