よむ、つかう、まなぶ。
総-3参考2 (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_67369.html |
| 出典情報 | 中央社会保険医療協議会 総会(第636回 12/17)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【用法・用量】
母集団薬物動態解析結果等に基づき、非小細胞肺癌及び小細胞肺癌に係る効能・効果に対
して本薬単独投与の際に、1,200 mg Q3W 投与に加え、1,680 mg 4 週間間隔(以下、
「Q4W」と
いう。)投与を可能とする製造販売承認事項一部変更承認申請が行われた。本剤の母集団薬物
動態モデルを用いたシミュレーション*により、進展型 SCLC 患者に本剤 1680 mg を Q4W で
投与したときの血清中濃度が検討された結果は表 2 のとおりであり、IMpower133 試験の日本
人集団における 1680 mg の Q4W 投与時の血中濃度は、全体集団における 1200 mg の Q3W 投
与時と同程度以上に維持できると推定された。また、曝露-反応解析の結果から本剤の曝露
量と安全性との間に明確な関連は認められなかったこと。なお、日本人の進行固形癌患者を
対象に本剤 1680 mg を Q4W で投与した国内第Ⅰ/Ⅱ相試験(JO44110 試験)において、安全
性に特段の懸念は認められていない。
*:国際共同第Ⅰ/ Ⅲ相試験(IMpower133 試験)に組み入れられた全体集団及び日本人集団の患者背景の分布に
基づき、1000 例の仮想患者集団をそれぞれ生成し、当該仮想患者集団に本薬を 1200 mg Q3W 及び 1680 mg
Q4W 反復静脈内投与した時のサイクル 1 及び定常状態における曝露量が推定された。
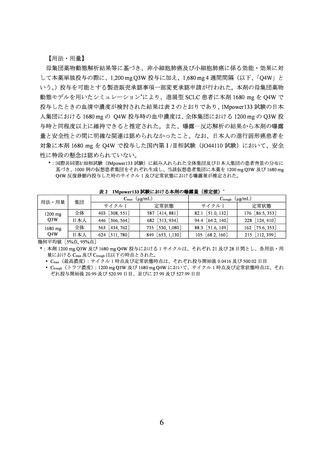
表2
用法・用量
集団
IMpower133 試験における本剤の曝露量(推定値)*
Cmax(µg/mL)
Ctrough(µg/mL)
サイクル 1
定常状態
サイクル 1
定常状態
全体
403[308,
551]
587[414,
881]
82.1[51.0,
132]
176[86.5,
353]
1200 mg
Q3W
日本人
446[366, 564]
682[513, 934]
94.4[64.2, 140]
228[124, 410]
全体
563[434, 762]
735[530, 1,080]
88.3[51.6, 149]
162[75.6, 353]
1680 mg
Q4W
日本人
624[511, 780]
849[653, 1,130]
105[68.2, 160]
215[112, 399]
幾何平均値[5%点, 95%点]
*:本剤 1200 mg Q3W 及び 1680 mg Q4W 投与における 1 サイクルは、それぞれ 21 及び 28 日間とし、各用法・用
量における Cmax 及び Ctrough は以下の時点とされた。
Cmax(最高濃度)
:サイクル 1 時点及び定常状態時点は、それぞれ投与開始後 0.0416 及び 500.02 日目
Ctrough(トラフ濃度)
:1200 mg Q3W 及び 1680 mg Q4W において、サイクル 1 時点及び定常状態時点は、それ
ぞれ投与開始後 20.99 及び 520.99 日目、並びに 27.99 及び 527.99 日目
6
母集団薬物動態解析結果等に基づき、非小細胞肺癌及び小細胞肺癌に係る効能・効果に対
して本薬単独投与の際に、1,200 mg Q3W 投与に加え、1,680 mg 4 週間間隔(以下、
「Q4W」と
いう。)投与を可能とする製造販売承認事項一部変更承認申請が行われた。本剤の母集団薬物
動態モデルを用いたシミュレーション*により、進展型 SCLC 患者に本剤 1680 mg を Q4W で
投与したときの血清中濃度が検討された結果は表 2 のとおりであり、IMpower133 試験の日本
人集団における 1680 mg の Q4W 投与時の血中濃度は、全体集団における 1200 mg の Q3W 投
与時と同程度以上に維持できると推定された。また、曝露-反応解析の結果から本剤の曝露
量と安全性との間に明確な関連は認められなかったこと。なお、日本人の進行固形癌患者を
対象に本剤 1680 mg を Q4W で投与した国内第Ⅰ/Ⅱ相試験(JO44110 試験)において、安全
性に特段の懸念は認められていない。
*:国際共同第Ⅰ/ Ⅲ相試験(IMpower133 試験)に組み入れられた全体集団及び日本人集団の患者背景の分布に
基づき、1000 例の仮想患者集団をそれぞれ生成し、当該仮想患者集団に本薬を 1200 mg Q3W 及び 1680 mg
Q4W 反復静脈内投与した時のサイクル 1 及び定常状態における曝露量が推定された。
表2
用法・用量
集団
IMpower133 試験における本剤の曝露量(推定値)*
Cmax(µg/mL)
Ctrough(µg/mL)
サイクル 1
定常状態
サイクル 1
定常状態
全体
403[308,
551]
587[414,
881]
82.1[51.0,
132]
176[86.5,
353]
1200 mg
Q3W
日本人
446[366, 564]
682[513, 934]
94.4[64.2, 140]
228[124, 410]
全体
563[434, 762]
735[530, 1,080]
88.3[51.6, 149]
162[75.6, 353]
1680 mg
Q4W
日本人
624[511, 780]
849[653, 1,130]
105[68.2, 160]
215[112, 399]
幾何平均値[5%点, 95%点]
*:本剤 1200 mg Q3W 及び 1680 mg Q4W 投与における 1 サイクルは、それぞれ 21 及び 28 日間とし、各用法・用
量における Cmax 及び Ctrough は以下の時点とされた。
Cmax(最高濃度)
:サイクル 1 時点及び定常状態時点は、それぞれ投与開始後 0.0416 及び 500.02 日目
Ctrough(トラフ濃度)
:1200 mg Q3W 及び 1680 mg Q4W において、サイクル 1 時点及び定常状態時点は、それ
ぞれ投与開始後 20.99 及び 520.99 日目、並びに 27.99 及び 527.99 日目
6