よむ、つかう、まなぶ。
資料4-2 ロミプロスチム(遺伝子組換え) (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00032.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第58回 3/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
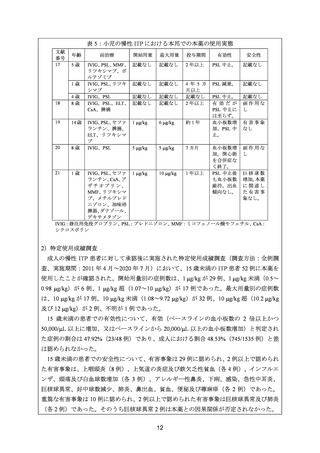
公表文献及び特定使用成績調査より、本邦で開始用量を 1 g/kg、最大用量を 10 g/kg とし
て本薬が使用されていることが確認された(6.(2)参照)
。したがって、小児の慢性 ITP に
対する用法・用量は、既承認の成人の慢性 ITP と同様に、開始用量 1 g/kg、最大用量 10 g/kg
の週 1 回皮下投与とし、血小板数、症状に応じて適宜増減可能とすることが妥当と判断す
る。
また、血小板反応に基づく用量の調節方法について、欧米の承認の根拠となった海外第
Ⅲ相試験の規定を踏まえ、既承認の成人の慢性 ITP に対する規定と同様に設定し、成人と
同様に用法及び用量に関連する注意の項に記載することが妥当と判断する。
9.要望内容に係る更なる使用実態調査等の必要性について
(1)要望内容について現時点で国内外のエビデンスまたは臨床使用実態が不足している点
の有無について
検討会議は、要望内容に関して不足しているエビデンスはないと判断した。
(2)上記(1)で臨床使用実態が不足している場合は、必要とされる使用実態調査等の内
容について
なし。
(3)その他、製造販売後における留意点について
なし。
10.備考
なし
11.参考文献一覧
1) 米国添付文書:NPLATE (romiplostim) for injection, for subcutaneous use(Amgen Inc.)
2) 英国添付文書:Nplate 125/250/500 micrograms powder for solution for injection(Amgen
Europe B.V.)
3) 独国添付文書:Nplate 125/250/500 Mikrogramm Pulver zur Herstellung einer Injektionslösung
(Amgen Europe B.V.)
4) 仏国添付文書:Nplate 125/250/500 microgrammes poudre pour solution injectable(Amgen
Europe B.V.)
5) 加国添付文書:Nplate (romiplostim for injection)(Amgen Canada Inc.)
6) 豪州添付文書:Nplate(Amgen Australia Pty Ltd)
17
70 / 213
て本薬が使用されていることが確認された(6.(2)参照)
。したがって、小児の慢性 ITP に
対する用法・用量は、既承認の成人の慢性 ITP と同様に、開始用量 1 g/kg、最大用量 10 g/kg
の週 1 回皮下投与とし、血小板数、症状に応じて適宜増減可能とすることが妥当と判断す
る。
また、血小板反応に基づく用量の調節方法について、欧米の承認の根拠となった海外第
Ⅲ相試験の規定を踏まえ、既承認の成人の慢性 ITP に対する規定と同様に設定し、成人と
同様に用法及び用量に関連する注意の項に記載することが妥当と判断する。
9.要望内容に係る更なる使用実態調査等の必要性について
(1)要望内容について現時点で国内外のエビデンスまたは臨床使用実態が不足している点
の有無について
検討会議は、要望内容に関して不足しているエビデンスはないと判断した。
(2)上記(1)で臨床使用実態が不足している場合は、必要とされる使用実態調査等の内
容について
なし。
(3)その他、製造販売後における留意点について
なし。
10.備考
なし
11.参考文献一覧
1) 米国添付文書:NPLATE (romiplostim) for injection, for subcutaneous use(Amgen Inc.)
2) 英国添付文書:Nplate 125/250/500 micrograms powder for solution for injection(Amgen
Europe B.V.)
3) 独国添付文書:Nplate 125/250/500 Mikrogramm Pulver zur Herstellung einer Injektionslösung
(Amgen Europe B.V.)
4) 仏国添付文書:Nplate 125/250/500 microgrammes poudre pour solution injectable(Amgen
Europe B.V.)
5) 加国添付文書:Nplate (romiplostim for injection)(Amgen Canada Inc.)
6) 豪州添付文書:Nplate(Amgen Australia Pty Ltd)
17
70 / 213