よむ、つかう、まなぶ。
薬費参考○高額医薬品(認知症薬)に対する対応について (26 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000211220_00017.html |
| 出典情報 | 中央社会保険医療協議会 費用対効果評価専門部会・薬価専門部会 合同部会(第1回 10/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
薬価算定の基準に関する薬価算定組織の意見
中医協 総-3
5. 9.27
(2023年8月23日の薬価専門部会における意見)
4.その他
(3) 新たな評価を行う上での留意点
【背景・課題】
〇
薬価算定においては、薬事承認の審査過程で評価されている臨床試験成績等を基に判断しているが、医薬
品医療機器等法の改正により導入された緊急承認制度のように、有効性が検証されていない段階でも早期に
承認し、市販後に検証するような対応が進むと、新規収載時に有用性の評価に必要なデータが十分把握でき
ない場合が生じうる。また、実際の薬価算定においても、有効性・安全性以外の観点のものなど、薬事承認
の審査過程で評価されていないデータや、比較薬と直接比較する臨床試験の実施が困難な領域を中心に、間
接比較のデータを根拠に有用性系加算の適用を主張されることがある。再算定においても、薬価収載後に得
られ、薬事承認において評価されていないデータを根拠に加算の主張がなされることがある。
〇 一方で、薬事承認の審査過程で評価されていない新たなデータを評価する際には、単に論文化されている
だけではなく、客観的な評価手法が確立され、信頼性の確保されたデータを根拠として評価することが重要
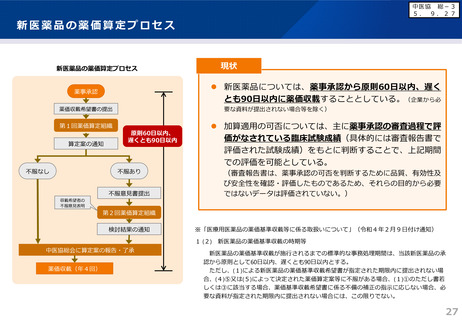
であり、薬事承認から原則60日以内、遅くとも90日以内に薬価収載するスケジュールを維持しながら、客観
性・頑健性を担保しつつ、どのような評価が可能かという課題がある。
なお、別の課題として、薬価算定は薬価基準収載希望書に記載された企業の主張を基に行っていることか
ら、企業にとって不利な情報が記載されることは稀であり、情報の不均一性が存在するという課題もあるこ
とに留意が必要である。
【意見】
〇
革新的な新薬のイノベーションを適切に評価することは重要であるが、その評価に際しては、現行の薬価
収載のスケジュールを維持しつつ、企業から提出されたデータの妥当性を合理的に判断するための評価のあ
り方及びその体制について、慎重に検討する必要があるのではないか。また、収載時に評価が困難なものに
ついては、収載後に評価することも考慮すべきではないか。
26
中医協 総-3
5. 9.27
(2023年8月23日の薬価専門部会における意見)
4.その他
(3) 新たな評価を行う上での留意点
【背景・課題】
〇
薬価算定においては、薬事承認の審査過程で評価されている臨床試験成績等を基に判断しているが、医薬
品医療機器等法の改正により導入された緊急承認制度のように、有効性が検証されていない段階でも早期に
承認し、市販後に検証するような対応が進むと、新規収載時に有用性の評価に必要なデータが十分把握でき
ない場合が生じうる。また、実際の薬価算定においても、有効性・安全性以外の観点のものなど、薬事承認
の審査過程で評価されていないデータや、比較薬と直接比較する臨床試験の実施が困難な領域を中心に、間
接比較のデータを根拠に有用性系加算の適用を主張されることがある。再算定においても、薬価収載後に得
られ、薬事承認において評価されていないデータを根拠に加算の主張がなされることがある。
〇 一方で、薬事承認の審査過程で評価されていない新たなデータを評価する際には、単に論文化されている
だけではなく、客観的な評価手法が確立され、信頼性の確保されたデータを根拠として評価することが重要
であり、薬事承認から原則60日以内、遅くとも90日以内に薬価収載するスケジュールを維持しながら、客観
性・頑健性を担保しつつ、どのような評価が可能かという課題がある。
なお、別の課題として、薬価算定は薬価基準収載希望書に記載された企業の主張を基に行っていることか
ら、企業にとって不利な情報が記載されることは稀であり、情報の不均一性が存在するという課題もあるこ
とに留意が必要である。
【意見】
〇
革新的な新薬のイノベーションを適切に評価することは重要であるが、その評価に際しては、現行の薬価
収載のスケジュールを維持しつつ、企業から提出されたデータの妥当性を合理的に判断するための評価のあ
り方及びその体制について、慎重に検討する必要があるのではないか。また、収載時に評価が困難なものに
ついては、収載後に評価することも考慮すべきではないか。
26