よむ、つかう、まなぶ。
再生医療等の安全性の確保等に関する法律施行5年後の見直しに係る検討 (22 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24369.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第74回 3/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
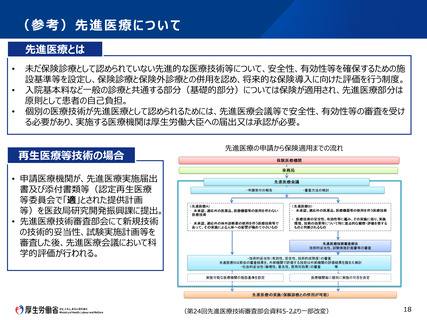
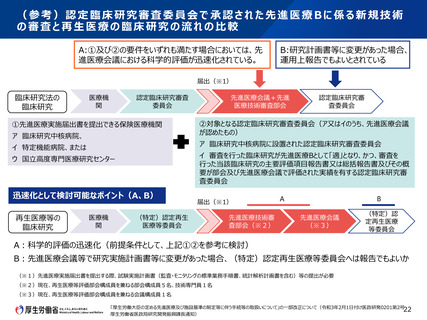
(参考)認定臨床研究審査委員会で承認された先進医療Bに係る新規技術
の審査と再生医療の臨床研究の流れの比較
A:①及び②の要件をいずれも満たす場合においては、先
進医療会議における科学的評価が迅速化されている。
B:研究計画書等に変更があった場合、
運用上報告でもよいとされている
届出(※1)
臨床研究法の
臨床研究
医療機
関
認定臨床研究審査
委員会
①先進医療実施届出書を提出できる保険医療機関
ア 臨床研究中核病院、
認定臨床研究審
査委員会
②対象となる認定臨床研究審査委員会(ア又はイのうち、先進医療会議
が認めたもの)
ア 臨床研究中核病院に設置された認定臨床研究審査委員会
イ 特定機能病院、または
イ 審査を行った臨床研究が先進医療Bとして「適」となり、かつ、審査を
行った当該臨床研究の主要評価項目報告書又は総括報告書及びその概
要が部会及び先進医療会議で評価された実績を有する認定臨床研究審
査委員会
ウ 国立高度専門医療研究センター
迅速化として検討可能なポイント(A、B)
再生医療等の
臨床研究
先進医療会議+先進
医療技術審査部会
医療機
関
届出(※1)
(特定)認定再生
医療等委員会
先進医療技術審
査部会(※2)
A
B
先進医療会議
(※3)
(特定)認
定再生医療
等委員会
A:科学的評価の迅速化(前提条件として、上記①②を参考に検討)
B:先進医療会議等で研究実施計画書等に変更があった場合、(特定)認定再生医療等委員会へは報告でもよいか
(※1)先進医療実施届出書を提出する際、試験実施計画書(監査・モニタリングの標準業務手順書、統計解析計画書を含む)等の提出が必要
(※2)現在、再生医療等評価部会構成員を兼ねる部会構成員5名、技術専門員1名
(※3)現在、再生医療等評価部会構成員を兼ねる会議構成員1名
「厚生労働大臣の定める先進医療及び施設基準の制定等に伴う手続等の取扱いについて」の一部改正について(令和3年2月1日付け医政研発0201第2号
22
厚生労働省医政局研究開発振興課長通知)
の審査と再生医療の臨床研究の流れの比較
A:①及び②の要件をいずれも満たす場合においては、先
進医療会議における科学的評価が迅速化されている。
B:研究計画書等に変更があった場合、
運用上報告でもよいとされている
届出(※1)
臨床研究法の
臨床研究
医療機
関
認定臨床研究審査
委員会
①先進医療実施届出書を提出できる保険医療機関
ア 臨床研究中核病院、
認定臨床研究審
査委員会
②対象となる認定臨床研究審査委員会(ア又はイのうち、先進医療会議
が認めたもの)
ア 臨床研究中核病院に設置された認定臨床研究審査委員会
イ 特定機能病院、または
イ 審査を行った臨床研究が先進医療Bとして「適」となり、かつ、審査を
行った当該臨床研究の主要評価項目報告書又は総括報告書及びその概
要が部会及び先進医療会議で評価された実績を有する認定臨床研究審
査委員会
ウ 国立高度専門医療研究センター
迅速化として検討可能なポイント(A、B)
再生医療等の
臨床研究
先進医療会議+先進
医療技術審査部会
医療機
関
届出(※1)
(特定)認定再生
医療等委員会
先進医療技術審
査部会(※2)
A
B
先進医療会議
(※3)
(特定)認
定再生医療
等委員会
A:科学的評価の迅速化(前提条件として、上記①②を参考に検討)
B:先進医療会議等で研究実施計画書等に変更があった場合、(特定)認定再生医療等委員会へは報告でもよいか
(※1)先進医療実施届出書を提出する際、試験実施計画書(監査・モニタリングの標準業務手順書、統計解析計画書を含む)等の提出が必要
(※2)現在、再生医療等評価部会構成員を兼ねる部会構成員5名、技術専門員1名
(※3)現在、再生医療等評価部会構成員を兼ねる会議構成員1名
「厚生労働大臣の定める先進医療及び施設基準の制定等に伴う手続等の取扱いについて」の一部改正について(令和3年2月1日付け医政研発0201第2号
22
厚生労働省医政局研究開発振興課長通知)