よむ、つかう、まなぶ。
09_参考資料3_SCARDAにおけるワクチン・新規モダリティ研究開発事業採択課題一覧について (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_33297.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 研究開発及び生産・流通部会(第32回 5/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
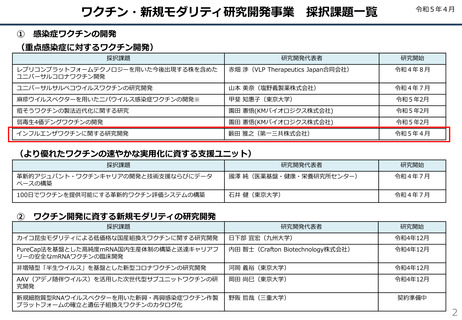
インフルエンザワクチンに関する研究開発
(令和5年2月時点)
(提案者:第一三共株式会社 籔田 雅之)
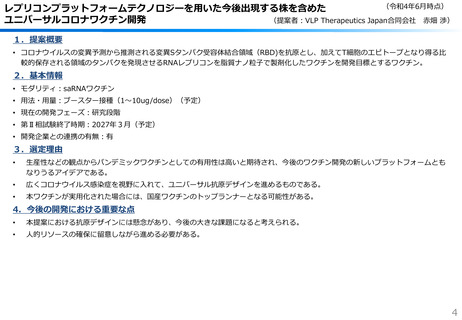
1.提案概要
•
mRNA encapsulated in lipid nanoparticle (LNP-mRNA)技術を用いたインフルエンザウイルス赤血球凝集素(HA)抗原を含む⾼
病原性鳥インフルエンザ(HPAI)ワクチンの開発をパンデミックに備えて目指すものである。
※ LNP-mRNA技術は、約10年前から新規モダリティとして提案者である第一三共社が独自に研究開発したもの。同技術を用いたCOVID-19ワクチン
製剤について国内承認申請中である。
2.基本情報
•
対象とする感染症:⾼病原性鳥インフルエンザ
•
モダリティ:mRNAワクチン
•
用法・用量:筋肉内投与 1回又は2回
•
現在の開発フェーズ:⾮臨床
•
第Ⅱ相試験終了時期:2026年度中(予定)
•
開発企業(アカデミア)との連携の有無:東京大学医科学研究所、第一三共バイオテック株式会社
3.選定理由
•
有用性の観点では、mRNAワクチンが、新しいモダリティとして特にその開発・製造スピードが優れていることは、新型コロナウイ
ルスのワクチン開発で実証されており、新型インフルエンザウイルスによる有事の際にも感染拡大抑制への貢献が期待できる。
•
新型コロナウイルス以外の感染症においてmRNAワクチンの有効性及び有用性は不明であるため、mRNAワクチンの汎用性をインフ
ルエンザワクチンで検証する意義はあると考える。
4.今後の開発における重要な点
•
COVID-19に対するmRNAワクチンにおいて冷蔵温度帯(2-8℃)での流通可能なワクチンを目指しており、その安定性について本
事業においても、計画内で確認が必要である。
•
第Ⅲ相試験実施や生産体制整備は今後の検討課題であり、早期に関係省庁と調整する必要がある。
9
(令和5年2月時点)
(提案者:第一三共株式会社 籔田 雅之)
1.提案概要
•
mRNA encapsulated in lipid nanoparticle (LNP-mRNA)技術を用いたインフルエンザウイルス赤血球凝集素(HA)抗原を含む⾼
病原性鳥インフルエンザ(HPAI)ワクチンの開発をパンデミックに備えて目指すものである。
※ LNP-mRNA技術は、約10年前から新規モダリティとして提案者である第一三共社が独自に研究開発したもの。同技術を用いたCOVID-19ワクチン
製剤について国内承認申請中である。
2.基本情報
•
対象とする感染症:⾼病原性鳥インフルエンザ
•
モダリティ:mRNAワクチン
•
用法・用量:筋肉内投与 1回又は2回
•
現在の開発フェーズ:⾮臨床
•
第Ⅱ相試験終了時期:2026年度中(予定)
•
開発企業(アカデミア)との連携の有無:東京大学医科学研究所、第一三共バイオテック株式会社
3.選定理由
•
有用性の観点では、mRNAワクチンが、新しいモダリティとして特にその開発・製造スピードが優れていることは、新型コロナウイ
ルスのワクチン開発で実証されており、新型インフルエンザウイルスによる有事の際にも感染拡大抑制への貢献が期待できる。
•
新型コロナウイルス以外の感染症においてmRNAワクチンの有効性及び有用性は不明であるため、mRNAワクチンの汎用性をインフ
ルエンザワクチンで検証する意義はあると考える。
4.今後の開発における重要な点
•
COVID-19に対するmRNAワクチンにおいて冷蔵温度帯(2-8℃)での流通可能なワクチンを目指しており、その安定性について本
事業においても、計画内で確認が必要である。
•
第Ⅲ相試験実施や生産体制整備は今後の検討課題であり、早期に関係省庁と調整する必要がある。
9