よむ、つかう、まなぶ。
資料2.緊急時の薬事承認の在り方 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_22281.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和3度第1回 11/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
制度設計に当たっての論点
3. 承認の期限・条件
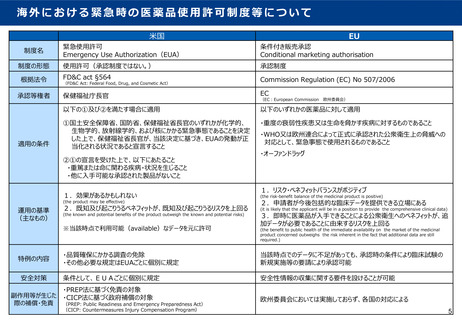
○ 米国EUAでは、緊急使用許可として期限が設定される。
○ 我が国の特例承認制度では、必要に応じて条件・期限を付すことができる。また、再生医療等製品の条件・期限
付き承認では、適正な使用の確保のために必要な条件と7年を超えない範囲の期限を付すこととしている。
✔ 緊急時における薬事承認であることを踏まえると、米国EUAを参考とし、承認の期限が必要ではないか。
✔ 緊急時における薬事承認であることを踏まえると、使用成績調査等の保健衛生上必要な措置を行うこと等の条
件が必要ではないか。
4. 市販後の対応
○ 米国EUAでは、期限の到来により効力は失効する。EUAで使用許可された製品について引き続き使用するために
は、その有効性や安全性を確認するため、正式な承認審査を受けることとなる。
○ 我が国では、期限付きの承認を受けた医薬品等は、期限の到来により承認の効力は失効する。当該製品を引き続
き使用するためには、使用成績に関する資料等を添付して、期限内に改めて通常の承認申請をすることとしている。
✔ 緊急時における薬事承認であることを踏まえると、当該医薬品等を引き続き使用するためには、
有効性・安全性を市販後に改めて確認することが必要ではないか。
○ 米国EUAでは、市販後安全対策については、個別の条件に基づき、副作用報告や市販後調査を実施している。
有害事象への救済措置として、個人又は遺族が給付金を受けることが可能な政府の補償プログラムがある。
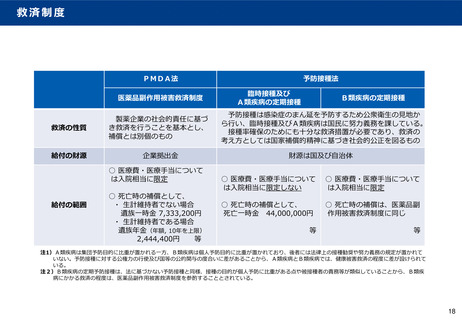
○ 我が国の市販後安全対策については、副作用報告制度等が措置されており、安全性の情報の収集・評価を実施し
ている。副作用によって生じた健康被害への救済措置としては、医薬品副作用被害救済制度や予防接種健康被害救
済制度が措置されている。
✔ 通常の承認と同様に、副作用報告制度や救済制度を適用してはどうか。
8
3. 承認の期限・条件
○ 米国EUAでは、緊急使用許可として期限が設定される。
○ 我が国の特例承認制度では、必要に応じて条件・期限を付すことができる。また、再生医療等製品の条件・期限
付き承認では、適正な使用の確保のために必要な条件と7年を超えない範囲の期限を付すこととしている。
✔ 緊急時における薬事承認であることを踏まえると、米国EUAを参考とし、承認の期限が必要ではないか。
✔ 緊急時における薬事承認であることを踏まえると、使用成績調査等の保健衛生上必要な措置を行うこと等の条
件が必要ではないか。
4. 市販後の対応
○ 米国EUAでは、期限の到来により効力は失効する。EUAで使用許可された製品について引き続き使用するために
は、その有効性や安全性を確認するため、正式な承認審査を受けることとなる。
○ 我が国では、期限付きの承認を受けた医薬品等は、期限の到来により承認の効力は失効する。当該製品を引き続
き使用するためには、使用成績に関する資料等を添付して、期限内に改めて通常の承認申請をすることとしている。
✔ 緊急時における薬事承認であることを踏まえると、当該医薬品等を引き続き使用するためには、
有効性・安全性を市販後に改めて確認することが必要ではないか。
○ 米国EUAでは、市販後安全対策については、個別の条件に基づき、副作用報告や市販後調査を実施している。
有害事象への救済措置として、個人又は遺族が給付金を受けることが可能な政府の補償プログラムがある。
○ 我が国の市販後安全対策については、副作用報告制度等が措置されており、安全性の情報の収集・評価を実施し
ている。副作用によって生じた健康被害への救済措置としては、医薬品副作用被害救済制度や予防接種健康被害救
済制度が措置されている。
✔ 通常の承認と同様に、副作用報告制度や救済制度を適用してはどうか。
8