よむ、つかう、まなぶ。
別紙1○先進医療Bの総括報告書に関する評価について(告示番号旧5/ jRCTc030190194) (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00054.html |
| 出典情報 | 先進医療会議(第118回 2/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別紙1
先進医療B
評価委員
総括報告書に関する評価表(告示旧 5)
主担当:
松山
副担当:
平川
技術専門委員:
-
先 進 医 療 NKT細胞を用いた免疫療法
の名称
申 請 医 療 千葉大学医学部附属病院
機関
医療技術
の概要
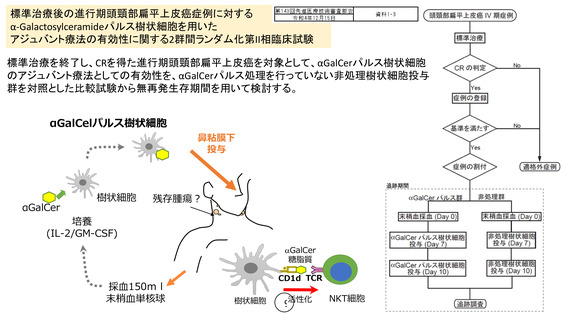
末梢血単核球由来の培養樹状細胞にNKT細胞特異的リガンドを提示
させて鼻粘膜に投与することで、Ⅳ期頭頸部扁平上皮癌初回治療後
完全奏効例の微小転移巣において内在性NKT細胞を活性化させ、抗腫
瘍効果を得ることを狙った新規の免疫細胞治療は、低侵襲で免疫全
体を賦活化し、再発を抑制し生存期間を延長できる画期的な治療と
考えられる。本研究はⅣ期頭頸部扁平上皮癌初回治療後CR例に対し
て、α-ガラクトシルセラミド (αGalCer)パルス樹状細胞のアジュ
バント療法としての有効性を、非処理樹状細胞投与を対照とした二
重盲検比較試験から明らかにすることが目的である。
○主要評価項目:無再発生存期間
○副次評価項目:
安全性評価基準:有害事象頻度と重篤度
有効性評価基準:2年無再発生存率、2年全生存率、末梢血 NKT 細
胞特異的免疫反応の評価
○目標症例数:
66 例(登録症例数:23 例)
○試験期間:
2013年3月~2021年7月
医 療 技 術 ○有効性の評価結果
の 試 験 結 症例数は試験計画時に行った統計学的考察により予定した組入れ数
果
に達しておらず、有効な評価はできなかったと考える。ただし少な
くとも実施できた症例数の中での解析では、本治療法における有効
性は証明されなかった。
○安全性の評価結果
本試験における有害事象発生率は39.1%と低値で、Grade1か2であ
1
先進医療B
評価委員
総括報告書に関する評価表(告示旧 5)
主担当:
松山
副担当:
平川
技術専門委員:
-
先 進 医 療 NKT細胞を用いた免疫療法
の名称
申 請 医 療 千葉大学医学部附属病院
機関
医療技術
の概要
末梢血単核球由来の培養樹状細胞にNKT細胞特異的リガンドを提示
させて鼻粘膜に投与することで、Ⅳ期頭頸部扁平上皮癌初回治療後
完全奏効例の微小転移巣において内在性NKT細胞を活性化させ、抗腫
瘍効果を得ることを狙った新規の免疫細胞治療は、低侵襲で免疫全
体を賦活化し、再発を抑制し生存期間を延長できる画期的な治療と
考えられる。本研究はⅣ期頭頸部扁平上皮癌初回治療後CR例に対し
て、α-ガラクトシルセラミド (αGalCer)パルス樹状細胞のアジュ
バント療法としての有効性を、非処理樹状細胞投与を対照とした二
重盲検比較試験から明らかにすることが目的である。
○主要評価項目:無再発生存期間
○副次評価項目:
安全性評価基準:有害事象頻度と重篤度
有効性評価基準:2年無再発生存率、2年全生存率、末梢血 NKT 細
胞特異的免疫反応の評価
○目標症例数:
66 例(登録症例数:23 例)
○試験期間:
2013年3月~2021年7月
医 療 技 術 ○有効性の評価結果
の 試 験 結 症例数は試験計画時に行った統計学的考察により予定した組入れ数
果
に達しておらず、有効な評価はできなかったと考える。ただし少な
くとも実施できた症例数の中での解析では、本治療法における有効
性は証明されなかった。
○安全性の評価結果
本試験における有害事象発生率は39.1%と低値で、Grade1か2であ
1