よむ、つかう、まなぶ。
資料7 先進医療Bの試験実施計画の変更について(告示番号47/ jRCTs031200326) (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_28927.html |
| 出典情報 | 先進医療会議 先進医療技術審査部会(第141回 11/17)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
【実施期間】
被験者登録期間:2021 年 2 月 1 日~2023 年 1 月 31 日
研究実施期間 :2021 年 2 月 1 日~2025 年 1 月 31 日
(登録期間 2 年、追跡期間 1 年、解析期間 1 年)
【予定症例数】
PhaseⅠ:6 例(最大 12 例)
PhaseⅡ:PhaseⅠとあわせて 22 例
【現在の登録状況】
19 症例(2022 年 11 月 1 日現在)
【主な変更内容】
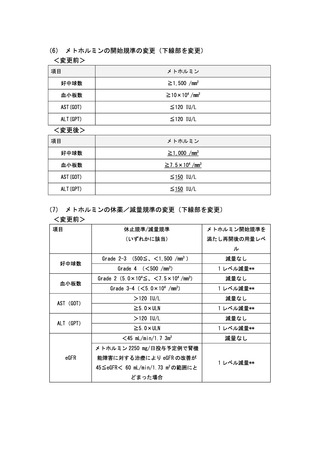
(1) 適格規準の修正
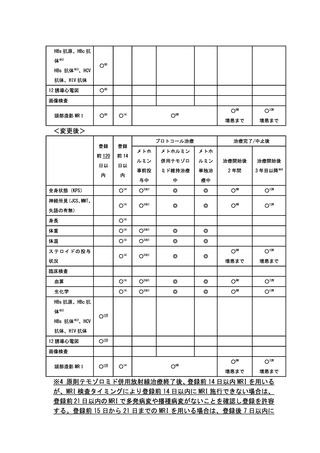
<変更前>
適格基準 11)④AST(GOT)≦120 IU/L ⑤ALT(GPT)≦120 IU/L
<変更後>
適格基準 11)④AST(GOT)≦150 IU/L ⑤ALT(GPT)≦150 IU/L
(2) 除外規準の変更
<変更前>
1) 活動性の重複がんを有する
<変更後>
1) 2 年以内の活動性の重複がんを有する
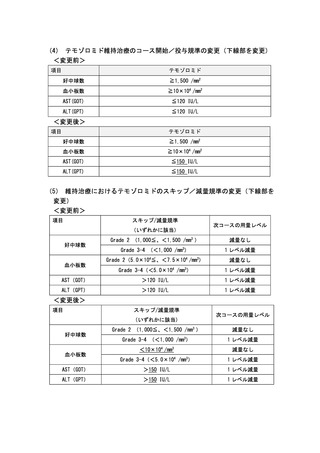
(3) テモゾロミド投与方法の変更(下線部を追記)
テモゾロミドは各コースの day 1 から day 5 に 1 日 1 回空腹時に内服す
る(朝・昼・夕、時刻は問わない)。食後 2 時間以上あけて内服し、内服
後は 2 時間以上食事をしない。各コースのテモゾロミドは 5 日間連日内
服し、その後 23 日間休薬する。(ただし、前後4日間は許容する。)
被験者登録期間:2021 年 2 月 1 日~2023 年 1 月 31 日
研究実施期間 :2021 年 2 月 1 日~2025 年 1 月 31 日
(登録期間 2 年、追跡期間 1 年、解析期間 1 年)
【予定症例数】
PhaseⅠ:6 例(最大 12 例)
PhaseⅡ:PhaseⅠとあわせて 22 例
【現在の登録状況】
19 症例(2022 年 11 月 1 日現在)
【主な変更内容】
(1) 適格規準の修正
<変更前>
適格基準 11)④AST(GOT)≦120 IU/L ⑤ALT(GPT)≦120 IU/L
<変更後>
適格基準 11)④AST(GOT)≦150 IU/L ⑤ALT(GPT)≦150 IU/L
(2) 除外規準の変更
<変更前>
1) 活動性の重複がんを有する
<変更後>
1) 2 年以内の活動性の重複がんを有する
(3) テモゾロミド投与方法の変更(下線部を追記)
テモゾロミドは各コースの day 1 から day 5 に 1 日 1 回空腹時に内服す
る(朝・昼・夕、時刻は問わない)。食後 2 時間以上あけて内服し、内服
後は 2 時間以上食事をしない。各コースのテモゾロミドは 5 日間連日内
服し、その後 23 日間休薬する。(ただし、前後4日間は許容する。)