よむ、つかう、まなぶ。
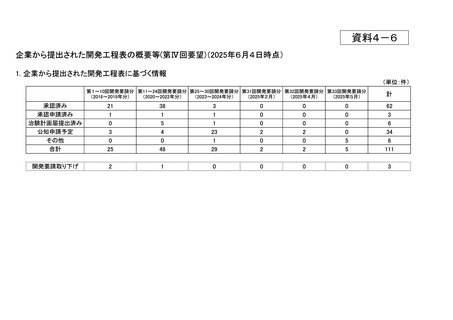
資料 4-6 企業から提出された開発工程表の概要等(第Ⅳ回要望) [340KB] (25 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第68回 7/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
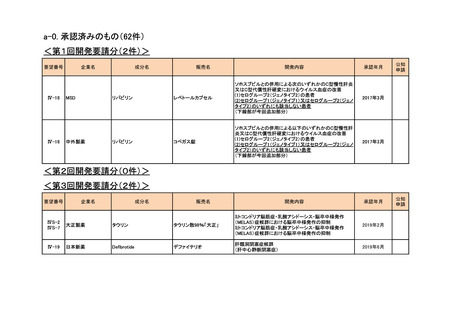
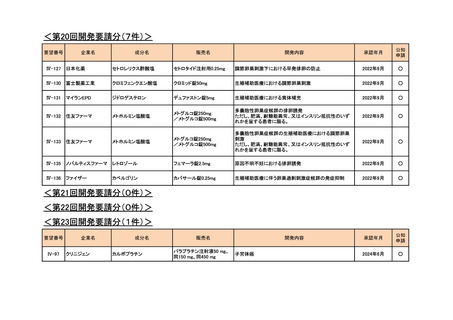
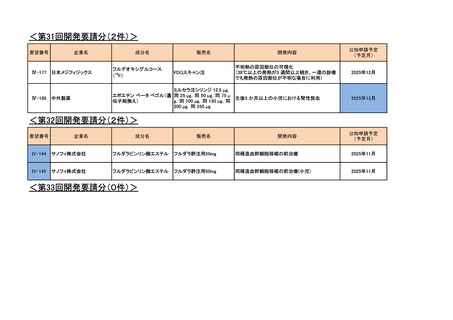
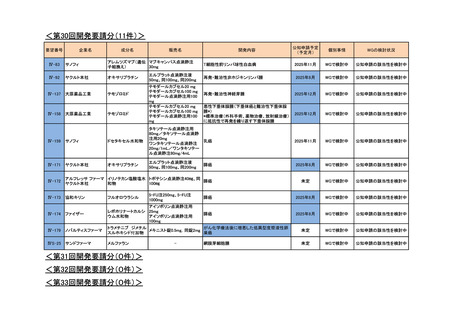
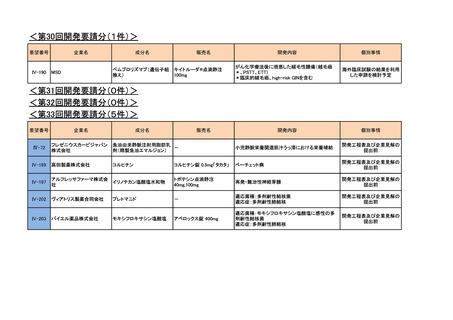
<第30回開発要請分(11件)>
要望番号
企業名
成分名
Ⅳ-83
サノフィ
アレムツズマブ(遺伝 マブキャンパス点滴静注
子組換え)
30mg
Ⅳ-92
ヤクルト本社
オキサリプラチン
Ⅳ-137
大原薬品工業
テモゾロミド
Ⅳ-158
大原薬品工業
テモゾロミド
開発内容
公知申請予定
(予定月)
個別事情
WGの検討状況
T細胞性前リンパ球性白血病
2025年11月
WGで検討中
公知申請の該当性を検討中
再発・難治性非ホジキンリンパ腫
2025年8月
WGで検討中
公知申請の該当性を検討中
再発・難治性神経芽腫
2025年12月
WGで検討中
公知申請の該当性を検討中
悪性下垂体腺腫(下垂体癌と難治性下垂体腺
腫*)
*標準治療(外科手術、薬物治療、放射線治療)
に抵抗性で再発を繰り返す下垂体腺腫
2025年12月
WGで検討中
公知申請の該当性を検討中
2025年11月
WGで検討中
公知申請の該当性を検討中
2025年8月
WGで検討中
公知申請の該当性を検討中
未定
WGで検討中
公知申請の該当性を検討中
販売名
エルプラット点滴静注液
50mg、同100mg、同200mg
テモダールカプセル20 mg
テモダールカプセル100 mg
テモダール点滴静注用100
mg
テモダールカプセル20 mg
テモダールカプセル100 mg
テモダール点滴静注用100
mg
Ⅳ-159
サノフィ
ドセタキセル水和物
タキソテール点滴静注用
80mg/タキソテール点滴静
注用20mg
乳癌
ワンタキソテール点滴静注
20mg/1mL/ワンタキソテー
ル点滴静注80mg/4mL
Ⅳ-171
ヤクルト本社
オキサリプラチン
エルプラット点滴静注液
50mg、同100mg、同200mg
Ⅳ-172
アルフレッサ ファーマ イリノテカン塩酸塩水 トポテシン点滴静注40㎎、同
膵癌
ヤクルト本社
和物
100㎎
Ⅳ-173
協和キリン
フルオロウラシル
5-FU注250mg、5-FU注
1000mg
膵癌
2025年8月
WGで検討中
公知申請の該当性を検討中
Ⅳ-174
ファイザー
アイソボリン点滴静注用
レボホリナートカルシ 25mg
ウム水和物
アイソボリン点滴静注用
100mg
膵癌
2025年8月
WGで検討中
公知申請の該当性を検討中
Ⅳ-179
ノバルティスファーマ
トラメチニブ ジメチル
がん化学療法後に増悪した低異型度漿液性卵
メキニスト錠0.5mg,同錠2mg
スルホキシド付加物
巣癌
未定
WGで検討中
公知申請の該当性を検討中
メルファラン
未定
WGで検討中
公知申請の該当性を検討中
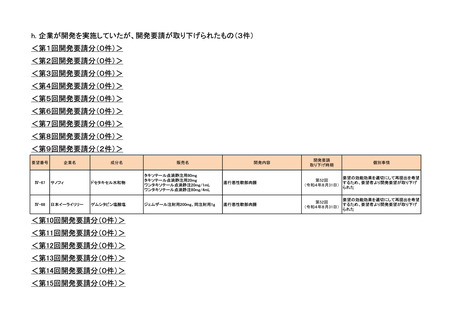
ⅣS-25 サンドファーマ
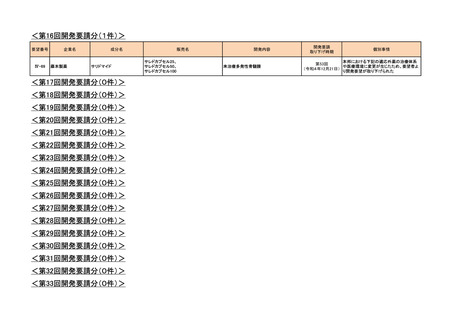
<第31回開発要請分(0件)>
<第32回開発要請分(0件)>
<第33回開発要請分(0件)>
-
膵癌
網膜芽細胞腫
要望番号
企業名
成分名
Ⅳ-83
サノフィ
アレムツズマブ(遺伝 マブキャンパス点滴静注
子組換え)
30mg
Ⅳ-92
ヤクルト本社
オキサリプラチン
Ⅳ-137
大原薬品工業
テモゾロミド
Ⅳ-158
大原薬品工業
テモゾロミド
開発内容
公知申請予定
(予定月)
個別事情
WGの検討状況
T細胞性前リンパ球性白血病
2025年11月
WGで検討中
公知申請の該当性を検討中
再発・難治性非ホジキンリンパ腫
2025年8月
WGで検討中
公知申請の該当性を検討中
再発・難治性神経芽腫
2025年12月
WGで検討中
公知申請の該当性を検討中
悪性下垂体腺腫(下垂体癌と難治性下垂体腺
腫*)
*標準治療(外科手術、薬物治療、放射線治療)
に抵抗性で再発を繰り返す下垂体腺腫
2025年12月
WGで検討中
公知申請の該当性を検討中
2025年11月
WGで検討中
公知申請の該当性を検討中
2025年8月
WGで検討中
公知申請の該当性を検討中
未定
WGで検討中
公知申請の該当性を検討中
販売名
エルプラット点滴静注液
50mg、同100mg、同200mg
テモダールカプセル20 mg
テモダールカプセル100 mg
テモダール点滴静注用100
mg
テモダールカプセル20 mg
テモダールカプセル100 mg
テモダール点滴静注用100
mg
Ⅳ-159
サノフィ
ドセタキセル水和物
タキソテール点滴静注用
80mg/タキソテール点滴静
注用20mg
乳癌
ワンタキソテール点滴静注
20mg/1mL/ワンタキソテー
ル点滴静注80mg/4mL
Ⅳ-171
ヤクルト本社
オキサリプラチン
エルプラット点滴静注液
50mg、同100mg、同200mg
Ⅳ-172
アルフレッサ ファーマ イリノテカン塩酸塩水 トポテシン点滴静注40㎎、同
膵癌
ヤクルト本社
和物
100㎎
Ⅳ-173
協和キリン
フルオロウラシル
5-FU注250mg、5-FU注
1000mg
膵癌
2025年8月
WGで検討中
公知申請の該当性を検討中
Ⅳ-174
ファイザー
アイソボリン点滴静注用
レボホリナートカルシ 25mg
ウム水和物
アイソボリン点滴静注用
100mg
膵癌
2025年8月
WGで検討中
公知申請の該当性を検討中
Ⅳ-179
ノバルティスファーマ
トラメチニブ ジメチル
がん化学療法後に増悪した低異型度漿液性卵
メキニスト錠0.5mg,同錠2mg
スルホキシド付加物
巣癌
未定
WGで検討中
公知申請の該当性を検討中
メルファラン
未定
WGで検討中
公知申請の該当性を検討中
ⅣS-25 サンドファーマ
<第31回開発要請分(0件)>
<第32回開発要請分(0件)>
<第33回開発要請分(0件)>
-
膵癌
網膜芽細胞腫