よむ、つかう、まなぶ。
第6回 健康・医療新産業協議会 資料7 消費者庁提出資料 (4 ページ)
出典
| 公開元URL | |
| 出典情報 | 健康・医療新産業協議会(第6回 5/30)《経済産業省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
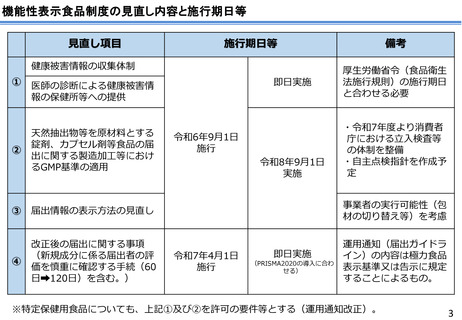
機能性表示食品制度の見直し内容と施行期日等
見直し項目
施行期日等
健康被害情報の収集体制
①
②
即日実施
医師の診断による健康被害情
報の保健所等への提供
天然抽出物等を原材料とする
錠剤、カプセル剤等食品の届
出に関する製造加工等におけ
るGMP基準の適用
令和6年9月1日
施行
令和8年9月1日
実施
備考
厚生労働省令(食品衛生
法施行規則)の施行期日
と合わせる必要
・令和7年度より消費者
庁における立入検査等
の体制を整備
・自主点検指針を作成予
定
③
届出情報の表示方法の見直し
事業者の実行可能性(包
材の切り替え等)を考慮
④
改正後の届出に関する事項
(新規成分に係る届出者の評
価を慎重に確認する手続(60
日 120日)を含む。)
運用通知(届出ガイドラ
イン)の内容は極力食品
表示基準又は告示に規定
することによるもの。
令和7年4月1日
施行
即日実施
(PRISMA2020の導入に合わ
せる)
※特定保健用食品についても、上記①及び②を許可の要件等とする(運用通知改正)。
3
見直し項目
施行期日等
健康被害情報の収集体制
①
②
即日実施
医師の診断による健康被害情
報の保健所等への提供
天然抽出物等を原材料とする
錠剤、カプセル剤等食品の届
出に関する製造加工等におけ
るGMP基準の適用
令和6年9月1日
施行
令和8年9月1日
実施
備考
厚生労働省令(食品衛生
法施行規則)の施行期日
と合わせる必要
・令和7年度より消費者
庁における立入検査等
の体制を整備
・自主点検指針を作成予
定
③
届出情報の表示方法の見直し
事業者の実行可能性(包
材の切り替え等)を考慮
④
改正後の届出に関する事項
(新規成分に係る届出者の評
価を慎重に確認する手続(60
日 120日)を含む。)
運用通知(届出ガイドラ
イン)の内容は極力食品
表示基準又は告示に規定
することによるもの。
令和7年4月1日
施行
即日実施
(PRISMA2020の導入に合わ
せる)
※特定保健用食品についても、上記①及び②を許可の要件等とする(運用通知改正)。
3