よむ、つかう、まなぶ。
第6回 健康・医療新産業協議会 資料7 消費者庁提出資料 (2 ページ)
出典
| 公開元URL | |
| 出典情報 | 健康・医療新産業協議会(第6回 5/30)《経済産業省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
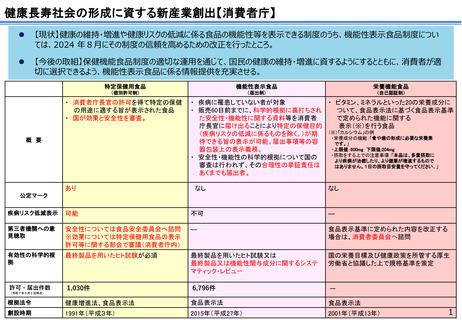
健康長寿社会の形成に資する新産業創出【消費者庁】
⚫
【現状】健康の維持・増進や健康リスクの低減に係る食品の機能性等を表示できる制度のうち、機能性表示食品制度につい
ては、2024 年8月にその制度の信頼を高めるための改正を行ったところ。
⚫
【今後の取組】保健機能食品制度の適切な運用を通じて、国民の健康の維持・増進に資するようにするとともに、消費者が適
切に選択できるよう、機能性表示食品に係る情報提供を充実させる。
特定保健用食品
機能性表示食品
栄養機能食品
(個別許可制)
(届出制)
(自己認証制)
・ 消費者庁長官の許可を得て特定の保健
の用途に適する旨が表示された食品
・ 国が効果と安全性を審査。
・ 疾病に罹患していない者が対象
・ ビタミン、ミネラルといった20の栄養成分に
・ 販売60日前までに、科学的根拠に裏打ちされ
ついて、食品表示法に基づく食品表示基準
た安全性・機能性に関する資料等を消費者
で定められた機能に関する
庁長官に届け出ることにより特定の保健目的
表示(※)を行う食品
(※)「カルシウム」の例
(疾病リスクの低減に係るものを除く。)が期
・栄養成分の機能:「骨や歯の形成に必要な栄養素
待できる旨の表示が可能。届出事項等の容
です。」
・上限値:600mg 下限値:204mg
器包装上の表示義務。
・摂取をする上での注意事項:「本品は、多量摂取に
・ 安全性・機能性の科学的根拠について国の
より疾病が治癒したり、より健康が増進するもので
審査は行われず、その合理性の挙証責任は
はありません。1日の摂取目安量を守ってください。」
あくまでも届出者。
あり
なし
なし
疾病リスク低減表示
可能
不可
―
第三者機関への意
見聴取
安全性については食品安全委員会へ諮問
※効果については特定保健用食品の表示
許可等に関する部会で審議(消費者庁内)
―
食品表示基準に定められた内容を改正する
場合は、消費者委員会へ諮問
有効性の科学的根
拠
最終製品を用いたヒト試験が必須
最終製品を用いたヒト試験又は
最終製品又は機能性関与成分に関するシステ
マティック・レビュー
国の栄養目標及び健康政策を所管する厚生
労働省と協議した上で規格基準を策定
許可・届出件数
1,030件
6,796件
―
根拠法令
健康増進法、食品表示法
食品表示法
食品表示法
創設時期
1991年(平成3年)
2015年(平成27年)
2001年(平成13年)
概 要
公定マーク
(令和7年5月1日時点)
1
⚫
【現状】健康の維持・増進や健康リスクの低減に係る食品の機能性等を表示できる制度のうち、機能性表示食品制度につい
ては、2024 年8月にその制度の信頼を高めるための改正を行ったところ。
⚫
【今後の取組】保健機能食品制度の適切な運用を通じて、国民の健康の維持・増進に資するようにするとともに、消費者が適
切に選択できるよう、機能性表示食品に係る情報提供を充実させる。
特定保健用食品
機能性表示食品
栄養機能食品
(個別許可制)
(届出制)
(自己認証制)
・ 消費者庁長官の許可を得て特定の保健
の用途に適する旨が表示された食品
・ 国が効果と安全性を審査。
・ 疾病に罹患していない者が対象
・ ビタミン、ミネラルといった20の栄養成分に
・ 販売60日前までに、科学的根拠に裏打ちされ
ついて、食品表示法に基づく食品表示基準
た安全性・機能性に関する資料等を消費者
で定められた機能に関する
庁長官に届け出ることにより特定の保健目的
表示(※)を行う食品
(※)「カルシウム」の例
(疾病リスクの低減に係るものを除く。)が期
・栄養成分の機能:「骨や歯の形成に必要な栄養素
待できる旨の表示が可能。届出事項等の容
です。」
・上限値:600mg 下限値:204mg
器包装上の表示義務。
・摂取をする上での注意事項:「本品は、多量摂取に
・ 安全性・機能性の科学的根拠について国の
より疾病が治癒したり、より健康が増進するもので
審査は行われず、その合理性の挙証責任は
はありません。1日の摂取目安量を守ってください。」
あくまでも届出者。
あり
なし
なし
疾病リスク低減表示
可能
不可
―
第三者機関への意
見聴取
安全性については食品安全委員会へ諮問
※効果については特定保健用食品の表示
許可等に関する部会で審議(消費者庁内)
―
食品表示基準に定められた内容を改正する
場合は、消費者委員会へ諮問
有効性の科学的根
拠
最終製品を用いたヒト試験が必須
最終製品を用いたヒト試験又は
最終製品又は機能性関与成分に関するシステ
マティック・レビュー
国の栄養目標及び健康政策を所管する厚生
労働省と協議した上で規格基準を策定
許可・届出件数
1,030件
6,796件
―
根拠法令
健康増進法、食品表示法
食品表示法
食品表示法
創設時期
1991年(平成3年)
2015年(平成27年)
2001年(平成13年)
概 要
公定マーク
(令和7年5月1日時点)
1