よむ、つかう、まなぶ。
○最適使用推進ガイドラインについて-3-2 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00143.html |
| 出典情報 | 中央社会保険医療協議会 総会(第519回 4/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
3.臨床成績
尿路上皮癌における術後補助療法の承認時に評価を行った主な臨床試験の成績を示
す。
【有効性】
国際共同第Ⅲ相試験(ONO-4538-33/CA209274 試験)
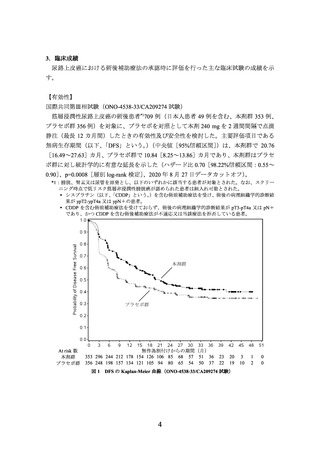
筋層浸潤性尿路上皮癌の術後患者*1709 例(日本人患者 49 例を含む、本剤群 353 例、
プラセボ群 356 例)を対象に、プラセボを対照として本剤 240 mg を 2 週間間隔で点滴
静注(最長 12 カ月間)したときの有効性及び安全性を検討した。主要評価項目である
無病生存期間(以下、「DFS」という。)(中央値[95%信頼区間])は、本剤群で 20.76
[16.49~27.63]カ月、プラセボ群で 10.84[8.25~13.86]カ月であり、本剤群はプラセ
ボ群に対し統計学的に有意な延長を示した(ハザード比 0.70[98.22%信頼区間:0.55~
0.90]、p=0.0008[層別 log-rank 検定]、2020 年 8 月 27 日データカットオフ)。
*1:膀胱、腎盂又は尿管を原発とし、以下のいずれかに該当する患者が対象とされた。なお、スクリー
ニング時点で低リスク筋層非浸潤性膀胱癌が認められた患者は組入れ可能とされた。
シスプラチン(以下、
「CDDP」という。
)を含む術前補助療法を受け、術後の病理組織学的診断結
果が ypT2-ypT4a 又は ypN+の患者。
CDDP を含む術前補助療法を受けておらず、術後の病理組織学的診断結果が pT3-pT4a 又は pN+
であり、かつ CDDP を含む術後補助療法が不適応又は当該療法を拒否している患者。
本剤群
プラセボ群
At risk 数
本剤群
プラセボ群
無作為割付けからの期間(月)
353 296 244 212 178 154 126 106 85 68 57 51 36
356 248 198 157 134 121 105 94 80 65 54 50 37
図1
23
22
20
19
DFS の Kaplan-Meier 曲線(ONO-4538-33/CA209274 試験)
4
3
10
1
2
0
0
尿路上皮癌における術後補助療法の承認時に評価を行った主な臨床試験の成績を示
す。
【有効性】
国際共同第Ⅲ相試験(ONO-4538-33/CA209274 試験)
筋層浸潤性尿路上皮癌の術後患者*1709 例(日本人患者 49 例を含む、本剤群 353 例、
プラセボ群 356 例)を対象に、プラセボを対照として本剤 240 mg を 2 週間間隔で点滴
静注(最長 12 カ月間)したときの有効性及び安全性を検討した。主要評価項目である
無病生存期間(以下、「DFS」という。)(中央値[95%信頼区間])は、本剤群で 20.76
[16.49~27.63]カ月、プラセボ群で 10.84[8.25~13.86]カ月であり、本剤群はプラセ
ボ群に対し統計学的に有意な延長を示した(ハザード比 0.70[98.22%信頼区間:0.55~
0.90]、p=0.0008[層別 log-rank 検定]、2020 年 8 月 27 日データカットオフ)。
*1:膀胱、腎盂又は尿管を原発とし、以下のいずれかに該当する患者が対象とされた。なお、スクリー
ニング時点で低リスク筋層非浸潤性膀胱癌が認められた患者は組入れ可能とされた。
シスプラチン(以下、
「CDDP」という。
)を含む術前補助療法を受け、術後の病理組織学的診断結
果が ypT2-ypT4a 又は ypN+の患者。
CDDP を含む術前補助療法を受けておらず、術後の病理組織学的診断結果が pT3-pT4a 又は pN+
であり、かつ CDDP を含む術後補助療法が不適応又は当該療法を拒否している患者。
本剤群
プラセボ群
At risk 数
本剤群
プラセボ群
無作為割付けからの期間(月)
353 296 244 212 178 154 126 106 85 68 57 51 36
356 248 198 157 134 121 105 94 80 65 54 50 37
図1
23
22
20
19
DFS の Kaplan-Meier 曲線(ONO-4538-33/CA209274 試験)
4
3
10
1
2
0
0