よむ、つかう、まなぶ。
総-1-1参考2○高額医薬品(感染症治療薬)に対する対応について (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00250.html |
| 出典情報 | 中央社会保険医療協議会 総会(第586回 3/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
高額医薬品(感染症治療薬)に対する対応案
現状
<審査の結果等>
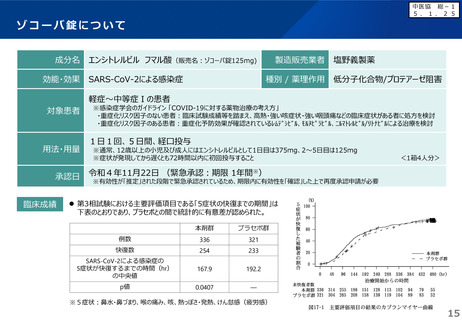
○ 本剤については、本年3月5日付けで通常承認を取得したが、効能・効果、用法・用量等の承認事項は緊急承認から変更はない。
○ 本剤の投与にあたり、想定している投与対象の重症度、症状等については変更ない。
○ 緊急承認においては、有効性・安全性に係る情報が限られていることから、本剤の有効性・安全性に関する情報について文書による
説明・同意を得てから投与することが承認条件で求められていたが、当該承認条件は削除された。
○ 同意書の取得は不要となったが、引き続き、妊娠の可能性のある女性に対して、資材を用いて入念に説明、確認を行うことが求めら
れている。
<感染動向や本剤の投与状況など>
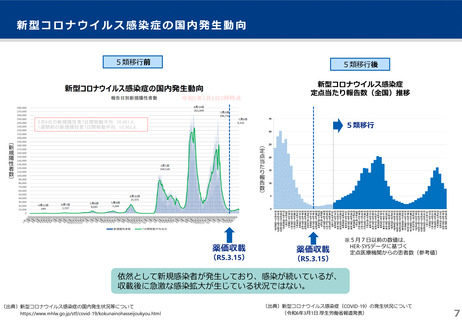
○ 感染動向は、依然として感染が継続しているが、収載後に急激な感染拡大が生じている状況ではない。
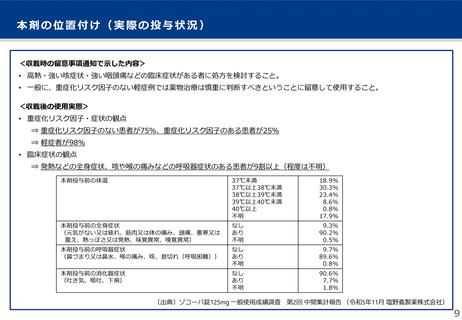
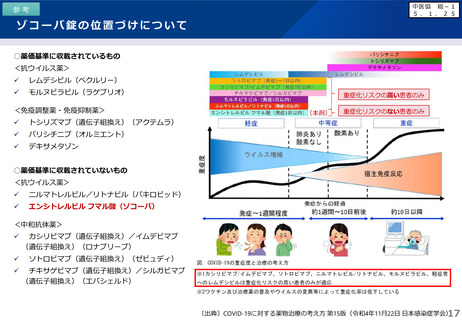
○ 本剤投与の患者は、重症化リスク因子なしが75%であり、症状は軽症が98%であった。
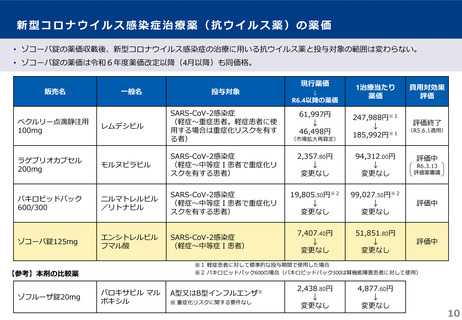
○ 本剤収載後、新型コロナウイルス感染症の治療に用いる抗ウイルス薬と投与対象範囲は変わっていない。
<実際の市場規模>
○ 本剤は、一般流通が開始されてから令和6年2月11日までに約100万人の患者に投与されていると推定されており、直近の推定使用患
者数から単純に換算すると、年間市場規模は280億円程度となる。収載時の使用規模予測(令和5年度:年間192億円)から、市場拡
大再算定が適用される市場規模には達していない。
対応案
• 本剤の通常承認にあたっては、緊急承認の時点から承認事項や本剤の位置づけ等に変化があるものではないが、通常承認
に基づく薬価は、本剤に係る審査結果やこれまでの使用実態等を踏まえ、通常の新薬の薬価収載と同様に、企業の意見を
踏まえ、薬価算定組織において検討することとしてはどうか。その上で、中医協総会において、薬価算定組織における算
定結果に基づき検討することとしてはどうか。
• また、本剤に係る収載後の価格調整(市場拡大再算定)の扱いについては、対象疾患の特性を踏まえたルールとされてい
るが、本ルールを継続するかどうかについては、本剤の薬価の検討時に中医協総会において検討することとしてはどうか。
13
現状
<審査の結果等>
○ 本剤については、本年3月5日付けで通常承認を取得したが、効能・効果、用法・用量等の承認事項は緊急承認から変更はない。
○ 本剤の投与にあたり、想定している投与対象の重症度、症状等については変更ない。
○ 緊急承認においては、有効性・安全性に係る情報が限られていることから、本剤の有効性・安全性に関する情報について文書による
説明・同意を得てから投与することが承認条件で求められていたが、当該承認条件は削除された。
○ 同意書の取得は不要となったが、引き続き、妊娠の可能性のある女性に対して、資材を用いて入念に説明、確認を行うことが求めら
れている。
<感染動向や本剤の投与状況など>
○ 感染動向は、依然として感染が継続しているが、収載後に急激な感染拡大が生じている状況ではない。
○ 本剤投与の患者は、重症化リスク因子なしが75%であり、症状は軽症が98%であった。
○ 本剤収載後、新型コロナウイルス感染症の治療に用いる抗ウイルス薬と投与対象範囲は変わっていない。
<実際の市場規模>
○ 本剤は、一般流通が開始されてから令和6年2月11日までに約100万人の患者に投与されていると推定されており、直近の推定使用患
者数から単純に換算すると、年間市場規模は280億円程度となる。収載時の使用規模予測(令和5年度:年間192億円)から、市場拡
大再算定が適用される市場規模には達していない。
対応案
• 本剤の通常承認にあたっては、緊急承認の時点から承認事項や本剤の位置づけ等に変化があるものではないが、通常承認
に基づく薬価は、本剤に係る審査結果やこれまでの使用実態等を踏まえ、通常の新薬の薬価収載と同様に、企業の意見を
踏まえ、薬価算定組織において検討することとしてはどうか。その上で、中医協総会において、薬価算定組織における算
定結果に基づき検討することとしてはどうか。
• また、本剤に係る収載後の価格調整(市場拡大再算定)の扱いについては、対象疾患の特性を踏まえたルールとされてい
るが、本ルールを継続するかどうかについては、本剤の薬価の検討時に中医協総会において検討することとしてはどうか。
13