よむ、つかう、まなぶ。
資料1:認定臨床研究審査委員会について (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_37286.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第34回 1/31)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
CRBの課題について
現在の状況
○ CRBの数について
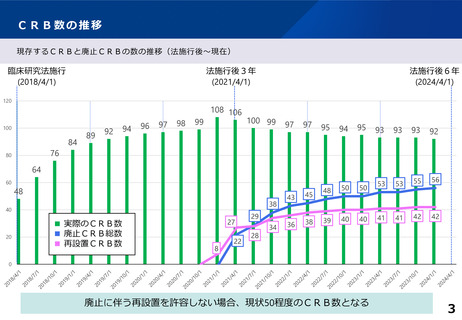
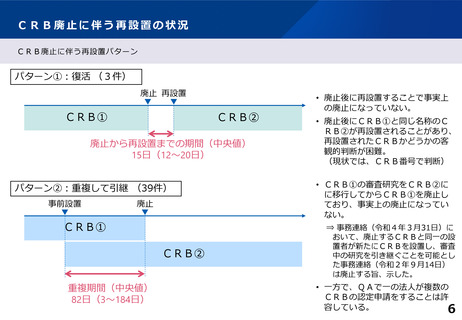
• CRBの考え方を示した事務連絡発出後も、廃止後に再設置するケースがある
• 廃止時手続き等の相談の際に、地方厚生局から再設置は控えるよう説明しているが、現行の法令で再設置
は禁止していないため、再設置の申請が提出された場合に受理せざるを得ない
• 令和6年は多くのCRBが法施行後2度目の更新時期に当たるため、同様の相談が増えると予想
○ CRBの審査の質について
• 審査の質の評価について模擬審査事業を実施してきたが、評価手法の検討が必要であり、被評価CRBへ
の十分なフィードバックとフォローアップができていない
• 令和4年度から臨床研究中核病院でピュアレビューを実施しており、今後他CRBへも展開していく予定
• 審査の内容が公表されていないため、他機関のCRBの審査の実態を知ることができない
今後の検討事項
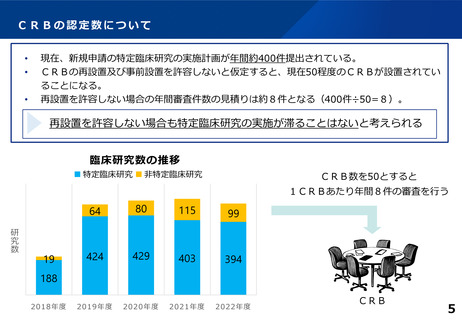
○ CRBの数について
• 臨床研究法施行規則で、CRBを再設置する場合に求める要件(改善計画の提出、欠格期間等)を追加す
るべきか。
(参考)臨床研究法第24条(欠格事由) 禁錮以上の刑、罰金刑、不正手段による認定等により認定が取り消され
認定の取消しの日から起算して三年を経過しない者 等
○ CRBの審査の質について
• 審査の質を定期的にモニタリングし、恒常的に質を維持するため、実際の審議内容を議事録等を用いて定
期的に評価を受けることを更新の要件とするか。
7
現在の状況
○ CRBの数について
• CRBの考え方を示した事務連絡発出後も、廃止後に再設置するケースがある
• 廃止時手続き等の相談の際に、地方厚生局から再設置は控えるよう説明しているが、現行の法令で再設置
は禁止していないため、再設置の申請が提出された場合に受理せざるを得ない
• 令和6年は多くのCRBが法施行後2度目の更新時期に当たるため、同様の相談が増えると予想
○ CRBの審査の質について
• 審査の質の評価について模擬審査事業を実施してきたが、評価手法の検討が必要であり、被評価CRBへ
の十分なフィードバックとフォローアップができていない
• 令和4年度から臨床研究中核病院でピュアレビューを実施しており、今後他CRBへも展開していく予定
• 審査の内容が公表されていないため、他機関のCRBの審査の実態を知ることができない
今後の検討事項
○ CRBの数について
• 臨床研究法施行規則で、CRBを再設置する場合に求める要件(改善計画の提出、欠格期間等)を追加す
るべきか。
(参考)臨床研究法第24条(欠格事由) 禁錮以上の刑、罰金刑、不正手段による認定等により認定が取り消され
認定の取消しの日から起算して三年を経過しない者 等
○ CRBの審査の質について
• 審査の質を定期的にモニタリングし、恒常的に質を維持するため、実際の審議内容を議事録等を用いて定
期的に評価を受けることを更新の要件とするか。
7