よむ、つかう、まなぶ。
○令和4年度保険医療材料制度の見直しについて-4-1参考1 (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00134.html |
| 出典情報 | 中央社会保険医療協議会 総会(第511回 1/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
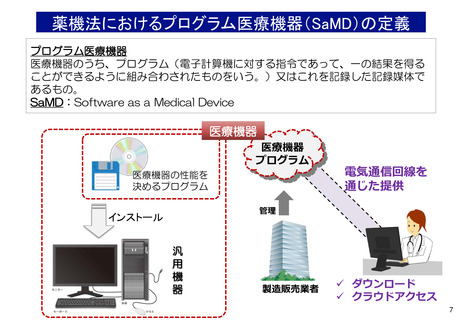
プログラム医療機器に対するこれまでの検討状況について
令和3年3月24日中医協総-6を改変
1.背景
○ 疾病の診断・治療を目的とした様々な新しいプログラムの開発により、アプリや人工知能(AI)を使用したプログ
ラム医療機器として薬事承認され、保険収載される事例が出てきている。
(令和2年11月11日中医協総会における指摘)
・ デジタルな部分について、技術料で評価していくのか、あるいは医療材料で評価していくのか、そういった考え方はやはりきち
んと今後整理していかないといけないのではないか。
・ 治療に資するプログラムの診療報酬の当てはめ方について、現行のような準用する形式でいいのか、あるいはまた新たな体系を
つくる必要があるのか、諸外国等の事例も踏まえて議論を深めておく必要があるのではないか。
○ 令和2年12月に第9回規制改革推進会議で決定された「当面の規制改革の実施事項」においても、プログラム医療
機器の医療保険における評価の考え方を明確化することが盛り込まれ、令和3年6月に、同様の内容が記載された
「規制改革実行計画」が閣議決定されたところ。
(当面の規制改革の実施事項)
(2)最先端の医療機器の開発・導入の促進
○ 厚生労働省は、プログラム医療機器(SaMD)の実用化に関し我が国における開発の立ち遅れ(いわゆるSaMDラグ)を解
消し、先端医療機器等の開発・導入並びにその産業化について、我が国が世界をリードしていけるよう、医薬品、医療機器等の品
質、有効性及び安全性の確保等に関する法律(昭和35年法律第145号。以下「医薬品医療機器等法」という。)に基づく医療機器
の承認審査等の仕組みについて以下の対応を講ずる。
ア
プログラム医療機器開発に関する事前相談体制の強化【令和2年度速やかに措置】
(略)
イ プログラム医療機器の該当・非該当の判断の容易化【令和2年度速やかに措置】
(略)
ウ プログラム医療機器の開発・導入の迅速化に資する審査体制・制度の見直し【令和2年度検討開始、早期に結論】
(略)
エ プログラム医療機器の普及に資する医療保険の評価の明確化【令和2年度検討開始、早期に結論】
a
診療報酬上の技術料等の算定における医療機器プログラムの評価については、医療従事者の働き方改革等の視点を含めて、
当該プログラム医療機器を活用して患者に対して提供される医療の質の確保・向上に係る評価の考え方を明確化する。
b
プログラム医療機器を使用した医療技術について、先進医療として保険外併用療養費制度の活用が可能であることを周知す
るとともに、選定療養の枠組みの適用についても検討する。
6
令和3年3月24日中医協総-6を改変
1.背景
○ 疾病の診断・治療を目的とした様々な新しいプログラムの開発により、アプリや人工知能(AI)を使用したプログ
ラム医療機器として薬事承認され、保険収載される事例が出てきている。
(令和2年11月11日中医協総会における指摘)
・ デジタルな部分について、技術料で評価していくのか、あるいは医療材料で評価していくのか、そういった考え方はやはりきち
んと今後整理していかないといけないのではないか。
・ 治療に資するプログラムの診療報酬の当てはめ方について、現行のような準用する形式でいいのか、あるいはまた新たな体系を
つくる必要があるのか、諸外国等の事例も踏まえて議論を深めておく必要があるのではないか。
○ 令和2年12月に第9回規制改革推進会議で決定された「当面の規制改革の実施事項」においても、プログラム医療
機器の医療保険における評価の考え方を明確化することが盛り込まれ、令和3年6月に、同様の内容が記載された
「規制改革実行計画」が閣議決定されたところ。
(当面の規制改革の実施事項)
(2)最先端の医療機器の開発・導入の促進
○ 厚生労働省は、プログラム医療機器(SaMD)の実用化に関し我が国における開発の立ち遅れ(いわゆるSaMDラグ)を解
消し、先端医療機器等の開発・導入並びにその産業化について、我が国が世界をリードしていけるよう、医薬品、医療機器等の品
質、有効性及び安全性の確保等に関する法律(昭和35年法律第145号。以下「医薬品医療機器等法」という。)に基づく医療機器
の承認審査等の仕組みについて以下の対応を講ずる。
ア
プログラム医療機器開発に関する事前相談体制の強化【令和2年度速やかに措置】
(略)
イ プログラム医療機器の該当・非該当の判断の容易化【令和2年度速やかに措置】
(略)
ウ プログラム医療機器の開発・導入の迅速化に資する審査体制・制度の見直し【令和2年度検討開始、早期に結論】
(略)
エ プログラム医療機器の普及に資する医療保険の評価の明確化【令和2年度検討開始、早期に結論】
a
診療報酬上の技術料等の算定における医療機器プログラムの評価については、医療従事者の働き方改革等の視点を含めて、
当該プログラム医療機器を活用して患者に対して提供される医療の質の確保・向上に係る評価の考え方を明確化する。
b
プログラム医療機器を使用した医療技術について、先進医療として保険外併用療養費制度の活用が可能であることを周知す
るとともに、選定療養の枠組みの適用についても検討する。
6