よむ、つかう、まなぶ。
資料1 遺伝子治療等臨床研究に関する指針の一部改正に係る検討の方向性 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27062.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会 遺伝子治療等臨床研究における個人情報の取扱いの在り方に関する専門委員会(第9回 7/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
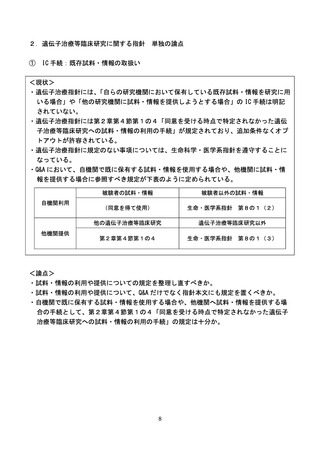
【生命科学・医学系指針見直しの方向性案】
・研究対象者等に通知し、又は研究対象者等が容易に知り得る状態に置くべき事項(遺伝子
治療指針第2章第4節第1の6(2)ロ(ロ)、第3章第5の2(2)ロ)として、研究
(又は第三者提供)の開始予定日を追加する。
・同意を受ける時点では特定されなかった研究を行う場合のオプトアウトが想定される場
合(遺伝子治療指針第2章第2節第2 研究計画書の記載事項(26)を記載する場合)に
は、同意取得時の説明事項(遺伝子治療指針第2章第4節第1の3)に、新たな研究又は
提供先の情報の確認方法(例えば、電子メールや文書による通知、ホームページの URL、
電話番号等)を追加する。
・オプトアウトの掲載場所に関するルールの策定や HP 上での周知等のオプトアウトの適切
な実施に向けた環境整備について、研究機関の長及び既存試料・情報の提供のみを行う機
関の長の責務として、新たに位置づける。
→
遺伝子治療指針でも同様に、通知の項目・同意取得時の説明事項を追加するとともに、
研究機関の長の責務として、周知等のオプトアウトの適切な実施に向けた環境整備につ
いて新たに位置づけることとしてよいか。
【参考】第2章第2節第2
研究計画書の記載事項
(26) 被験者から取得された試料・情報について、被験者等から同意を受ける時点では特定されない将
来の研究のために用いられる可能性又は他の研究機関に提供する可能性がある場合には、その旨及び同
意を受ける時点において想定される研究の内容
【参考】第2章第4節第1の3 説明事項
(17) 被験者から取得された試料・情報について、被験者等から同意を受ける時点では特定されない
将来の研究のために用いられる可能性又は他の研究機関に提供する可能性がある場合には、その旨及び
同意を受ける時点において想定される研究の内容
5
・研究対象者等に通知し、又は研究対象者等が容易に知り得る状態に置くべき事項(遺伝子
治療指針第2章第4節第1の6(2)ロ(ロ)、第3章第5の2(2)ロ)として、研究
(又は第三者提供)の開始予定日を追加する。
・同意を受ける時点では特定されなかった研究を行う場合のオプトアウトが想定される場
合(遺伝子治療指針第2章第2節第2 研究計画書の記載事項(26)を記載する場合)に
は、同意取得時の説明事項(遺伝子治療指針第2章第4節第1の3)に、新たな研究又は
提供先の情報の確認方法(例えば、電子メールや文書による通知、ホームページの URL、
電話番号等)を追加する。
・オプトアウトの掲載場所に関するルールの策定や HP 上での周知等のオプトアウトの適切
な実施に向けた環境整備について、研究機関の長及び既存試料・情報の提供のみを行う機
関の長の責務として、新たに位置づける。
→
遺伝子治療指針でも同様に、通知の項目・同意取得時の説明事項を追加するとともに、
研究機関の長の責務として、周知等のオプトアウトの適切な実施に向けた環境整備につ
いて新たに位置づけることとしてよいか。
【参考】第2章第2節第2
研究計画書の記載事項
(26) 被験者から取得された試料・情報について、被験者等から同意を受ける時点では特定されない将
来の研究のために用いられる可能性又は他の研究機関に提供する可能性がある場合には、その旨及び同
意を受ける時点において想定される研究の内容
【参考】第2章第4節第1の3 説明事項
(17) 被験者から取得された試料・情報について、被験者等から同意を受ける時点では特定されない
将来の研究のために用いられる可能性又は他の研究機関に提供する可能性がある場合には、その旨及び
同意を受ける時点において想定される研究の内容
5