よむ、つかう、まなぶ。
03【資料1】今後のパンデミックに備えるべき「重点感染症」について (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26623.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 研究開発及び生産・流通部会(第29回 7/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
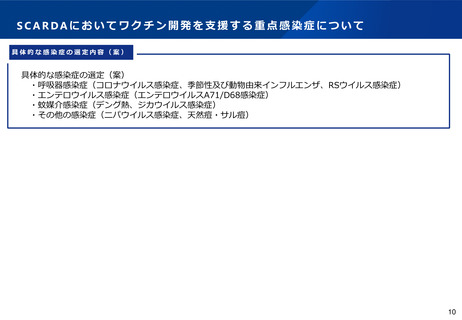
SCARDAにおいてワクチン開発を支援する重点感染症について
基本的考え方(案)
○SCARDAによる開発支援を実在するGroup B感染症に対して行うことにより、対象となるGroup B感染症は
もとより、Group A及びGroup X感染症による新たなパンデミック発生時にも即応できるよう準備する。
○Group Bに例示された感染症全てを対象とするのではなく、感染症ごとの研究開発の成功率を高める目的で
支援規模に見合うよう、パンデミックに対応するワクチンを開発する目的に沿い一定の絞り込みを行う。
○実際にSCARDAで開発支援を実施する感染症について、Group A及びBの例示から以下の点を考慮して選定
してはどうか。
1)飛沫感染など、先進国においてもヒトーヒト感染が容易に起こりうる感染経路を有するもの
2)有効なワクチンが存在せず、かつ国内に臨床試験段階に進められるシーズが存在しているもの
3)特にアジア地域において課題となっているもの
4)海外において発症予防試験の実施が期待できるもの ※
※国産ワクチンの実用化が遅れた要因を分析すると
・企業収益が感染症流行の動向に左右されるため研究開発投資の回収見通しが立てにくいこと
・国内企業規模が比較的小さく、数万例規模の発症予防試験を実施する研究開発投資力を持てないこと
・特に海外において大規模試験の経験がほとんど無く、速やかに実施するためのノウハウを持たなかったこと
・ワクチン開発を担う人材の育成・保持が不十分であること
などがあげられることから、平時に海外における大規模臨床試験を実施可能な感染症を重点感染症に含め、国
内ワクチン企業が海外/国際共同による発症予防試験の実施経験を積むことにより、パンデミック発生時の発
症予防試験の速やかな実施に繋げる。
9
基本的考え方(案)
○SCARDAによる開発支援を実在するGroup B感染症に対して行うことにより、対象となるGroup B感染症は
もとより、Group A及びGroup X感染症による新たなパンデミック発生時にも即応できるよう準備する。
○Group Bに例示された感染症全てを対象とするのではなく、感染症ごとの研究開発の成功率を高める目的で
支援規模に見合うよう、パンデミックに対応するワクチンを開発する目的に沿い一定の絞り込みを行う。
○実際にSCARDAで開発支援を実施する感染症について、Group A及びBの例示から以下の点を考慮して選定
してはどうか。
1)飛沫感染など、先進国においてもヒトーヒト感染が容易に起こりうる感染経路を有するもの
2)有効なワクチンが存在せず、かつ国内に臨床試験段階に進められるシーズが存在しているもの
3)特にアジア地域において課題となっているもの
4)海外において発症予防試験の実施が期待できるもの ※
※国産ワクチンの実用化が遅れた要因を分析すると
・企業収益が感染症流行の動向に左右されるため研究開発投資の回収見通しが立てにくいこと
・国内企業規模が比較的小さく、数万例規模の発症予防試験を実施する研究開発投資力を持てないこと
・特に海外において大規模試験の経験がほとんど無く、速やかに実施するためのノウハウを持たなかったこと
・ワクチン開発を担う人材の育成・保持が不十分であること
などがあげられることから、平時に海外における大規模臨床試験を実施可能な感染症を重点感染症に含め、国
内ワクチン企業が海外/国際共同による発症予防試験の実施経験を積むことにより、パンデミック発生時の発
症予防試験の速やかな実施に繋げる。
9