よむ、つかう、まなぶ。
医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律等の公布について (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/content/11120000/000940763.pdf |
| 出典情報 | 医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律等の公布について(5/20付 通知)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
・医薬品の安全性に関する非臨床試験の実施の基準に関する省令(平成9年厚生省令第 21 号)
・医薬品の臨床試験の実施の基準に関する省令(平成9年厚生省令第 28 号)
・独立行政法人医薬品医療機器総合機構法施行規則(平成 16 年厚生労働省令第 51 号)
・医療機器及び体外診断用医薬品の製造管理及び品質管理の基準に関する省令(平成 16 年厚生労働省令第 169 号)
・医薬品の製造販売後の調査及び試験の実施の基準に関する省令
・医療機器の臨床試験の実施の基準に関する省令(平成 17 年厚生労働省令第 36 号)
・医療機器の安全性に関する非臨床試験の実施の基準に関する省令(平成17 年厚生労働省令第 37 号)
・医療機器の製造販売後の調査及び試験の実施の基準に関する省令
・再生医療等製品の安全性に関する非臨床試験の実施の基準に関する省令(平成 26 年厚生労働省令第 88 号)
・再生医療等製品の臨床試験の実施の基準に関する省令(平成 26 年厚生労働省令第 89 号)
・再生医療等製品の製造販売後の調査及び試験の実施の基準に関する省令(平成 26 年厚生労働省令第 90 号)
・臨床研究法施行規則(平成 30 年厚生労働省令第 17 号)
第3 施行期日
1 緊急時に新たな医薬品等を速やかに薬事承認する仕組みの整備に関する事項は、公布の日から施行するものとすること。
(改正法:附則第1条関係、整備政令:附則関係、整備省令:附則関係)
2 電子処方箋の仕組みの整備に関する事項は、令和5年2月1日までの間において政令で定める日から施行するものとすること。
(改正法:附則第1条ただし書関係)
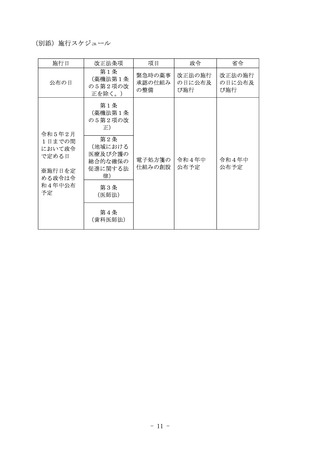
(※参考:別添「施行スケジュール」)
- 10 -
・医薬品の臨床試験の実施の基準に関する省令(平成9年厚生省令第 28 号)
・独立行政法人医薬品医療機器総合機構法施行規則(平成 16 年厚生労働省令第 51 号)
・医療機器及び体外診断用医薬品の製造管理及び品質管理の基準に関する省令(平成 16 年厚生労働省令第 169 号)
・医薬品の製造販売後の調査及び試験の実施の基準に関する省令
・医療機器の臨床試験の実施の基準に関する省令(平成 17 年厚生労働省令第 36 号)
・医療機器の安全性に関する非臨床試験の実施の基準に関する省令(平成17 年厚生労働省令第 37 号)
・医療機器の製造販売後の調査及び試験の実施の基準に関する省令
・再生医療等製品の安全性に関する非臨床試験の実施の基準に関する省令(平成 26 年厚生労働省令第 88 号)
・再生医療等製品の臨床試験の実施の基準に関する省令(平成 26 年厚生労働省令第 89 号)
・再生医療等製品の製造販売後の調査及び試験の実施の基準に関する省令(平成 26 年厚生労働省令第 90 号)
・臨床研究法施行規則(平成 30 年厚生労働省令第 17 号)
第3 施行期日
1 緊急時に新たな医薬品等を速やかに薬事承認する仕組みの整備に関する事項は、公布の日から施行するものとすること。
(改正法:附則第1条関係、整備政令:附則関係、整備省令:附則関係)
2 電子処方箋の仕組みの整備に関する事項は、令和5年2月1日までの間において政令で定める日から施行するものとすること。
(改正法:附則第1条ただし書関係)
(※参考:別添「施行スケジュール」)
- 10 -