よむ、つかう、まなぶ。
総-11-4再生医療等製品の医療保険上の取扱いについて(アムシェプリ) (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72294.html |
| 出典情報 | 中央社会保険医療協議会 総会(第649回 4/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
中医協 総-11-4
8 . 4 . 8
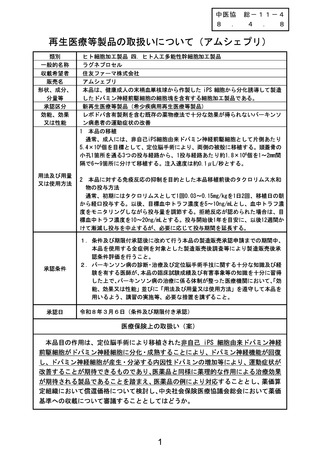
再生医療等製品の取扱いについて(アムシェプリ)
類別
一般的名称
ヒト細胞加工製品 四.ヒト人工多能性幹細胞加工製品
ラグネプロセル
収載希望者
販売名
形状、成分、
分量等
承認区分
効能、効果
又は性能
住友ファーマ株式会社
アムシェプリ
本品は、健康成人の末梢血単核球から作製した iPS 細胞から分化誘導して製造
したドパミン神経前駆細胞の細胞塊を含有する細胞加工製品である。
新再生医療等製品(希少疾病用再生医療等製品)
レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないパーキンソ
ン病患者の運動症状の改善
1 本品の移植
通常、成人には、非自己iPS細胞由来ドパミン神経前駆細胞として片側あたり
5.4×106個を目標として、定位脳手術により、両側の被殻に移植する。頭蓋骨の
小孔1箇所を通る3つの投与経路から、1投与経路あたり約1.8×106個を1~2mm間
隔で6~9箇所に分けて移植する。注入速度は約0.1μL/秒とする。
用法及び用量
又は使用方法
2 本品に対する免疫反応の抑制を目的とした本品移植前後のタクロリムス水和
物の投与方法
通常、初期にはタクロリムスとして1回0.03~0.15mg/kgを1日2回、移植日の朝
から経口投与する。以後、目標血中トラフ濃度を5~10ng/mLとし、血中トラフ濃
度をモニタリングしながら投与量を調節する。拒絶反応が認められた場合は、目
標血中トラフ濃度を10~20ng/mLとする。投与開始後1年を目安に、以後12週間か
けて漸減し投与を中止するが、必要に応じて投与期間を延長する。
承認条件
1. 条件及び期限付承認後に改めて行う本品の製造販売承認申請までの期間中、
本品を使用する全症例を対象とした製造販売後調査等により製造販売後承
認条件評価を行うこと。
2. パーキンソン病の診断・治療及び定位脳手術手技に関する十分な知識及び経
験を有する医師が、本品の臨床試験成績及び有害事象等の知識を十分に習得
した上で、パーキンソン病の治療に係る体制が整った医療機関において、
「効
能、効果又は性能」並びに「用法及び用量又は使用方法」を遵守して本品を
用いるよう、講習の実施等、必要な措置を講ずること。
承認日
令和8年3月6日(条件及び期限付き承認)
医療保険上の取扱い(案)
本品目の作用は、定位脳手術により移植された非自己 iPS 細胞由来ドパミン神経
前駆細胞がドパミン神経細胞に分化・成熟することにより、ドパミン神経機能が回復
し、ドパミン神経細胞が産生・分泌する内因性ドパミンの増加等により、運動症状が
改善することが期待できるものであり、医薬品と同様に薬理的な作用による治療効果
が期待される製品であることを踏まえ、医薬品の例により対応することとし、薬価算
定組織において償還価格について検討し、中央社会保険医療協議会総会において薬価
基準への収載について審議することとしてはどうか。
1
8 . 4 . 8
再生医療等製品の取扱いについて(アムシェプリ)
類別
一般的名称
ヒト細胞加工製品 四.ヒト人工多能性幹細胞加工製品
ラグネプロセル
収載希望者
販売名
形状、成分、
分量等
承認区分
効能、効果
又は性能
住友ファーマ株式会社
アムシェプリ
本品は、健康成人の末梢血単核球から作製した iPS 細胞から分化誘導して製造
したドパミン神経前駆細胞の細胞塊を含有する細胞加工製品である。
新再生医療等製品(希少疾病用再生医療等製品)
レボドパ含有製剤を含む既存の薬物療法で十分な効果が得られないパーキンソ
ン病患者の運動症状の改善
1 本品の移植
通常、成人には、非自己iPS細胞由来ドパミン神経前駆細胞として片側あたり
5.4×106個を目標として、定位脳手術により、両側の被殻に移植する。頭蓋骨の
小孔1箇所を通る3つの投与経路から、1投与経路あたり約1.8×106個を1~2mm間
隔で6~9箇所に分けて移植する。注入速度は約0.1μL/秒とする。
用法及び用量
又は使用方法
2 本品に対する免疫反応の抑制を目的とした本品移植前後のタクロリムス水和
物の投与方法
通常、初期にはタクロリムスとして1回0.03~0.15mg/kgを1日2回、移植日の朝
から経口投与する。以後、目標血中トラフ濃度を5~10ng/mLとし、血中トラフ濃
度をモニタリングしながら投与量を調節する。拒絶反応が認められた場合は、目
標血中トラフ濃度を10~20ng/mLとする。投与開始後1年を目安に、以後12週間か
けて漸減し投与を中止するが、必要に応じて投与期間を延長する。
承認条件
1. 条件及び期限付承認後に改めて行う本品の製造販売承認申請までの期間中、
本品を使用する全症例を対象とした製造販売後調査等により製造販売後承
認条件評価を行うこと。
2. パーキンソン病の診断・治療及び定位脳手術手技に関する十分な知識及び経
験を有する医師が、本品の臨床試験成績及び有害事象等の知識を十分に習得
した上で、パーキンソン病の治療に係る体制が整った医療機関において、
「効
能、効果又は性能」並びに「用法及び用量又は使用方法」を遵守して本品を
用いるよう、講習の実施等、必要な措置を講ずること。
承認日
令和8年3月6日(条件及び期限付き承認)
医療保険上の取扱い(案)
本品目の作用は、定位脳手術により移植された非自己 iPS 細胞由来ドパミン神経
前駆細胞がドパミン神経細胞に分化・成熟することにより、ドパミン神経機能が回復
し、ドパミン神経細胞が産生・分泌する内因性ドパミンの増加等により、運動症状が
改善することが期待できるものであり、医薬品と同様に薬理的な作用による治療効果
が期待される製品であることを踏まえ、医薬品の例により対応することとし、薬価算
定組織において償還価格について検討し、中央社会保険医療協議会総会において薬価
基準への収載について審議することとしてはどうか。
1