よむ、つかう、まなぶ。
【資料1】 本検討会の趣旨について (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71607.html |
| 出典情報 | 特定医療技術等開発推進検討会(第1回 3/16)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第1回
我が国における医薬品・医療技術開発の現状と課題
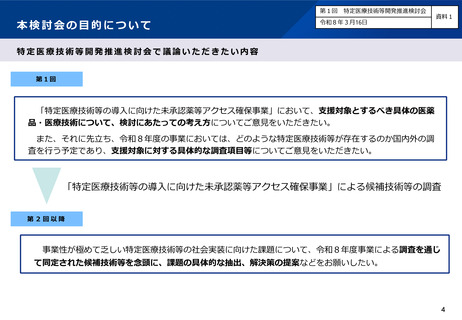
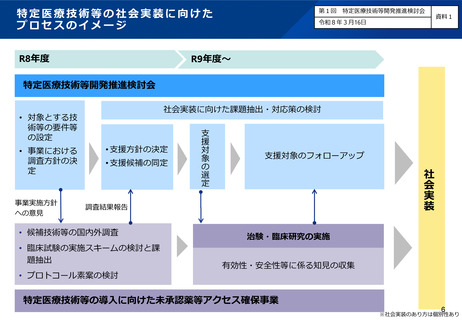
特定医療技術等開発推進検討会
令和8年3月16日
資料1
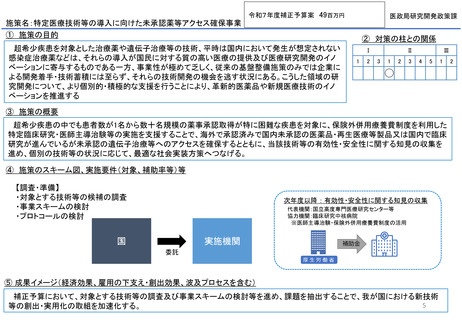
患者数が特に少ない超希少疾病等に対しては、市場性等の課題から、企業による医薬品や医療技術の開発が進まない現状がある。
他方、海外においては、超希少疾病に対しても、新規的な治療薬の開発が認められる。
医薬品・医療技術の開発における市場性等の課題の例
• ドラッグ・ロス
海外承認済だが、国内開発未着手・未承認の医薬品(ドラッグ・ロス)については、政府が情報収集し、企業への開発要請等を行って
いる。2016年から2020年に欧米で承認された品目のうち、ドラッグ・ロス品目は86品目あり、医療上の必要性を確認するべきと判断
された品目が55品目、その中から開発要請・開発公募に繋がった品目が23品目であり、開発公募品目のうち2品目について企業から開
発の意思の申し出があった。
ドラッグ・ロス86品目の中にはベンチャー企業が開発したものが56%、希少疾病用医薬品が47%、小児用医薬品が37%あり、日本の
医療環境の周知、市場規模の小さい医薬品の導入が課題となっている。
• 感染症に対する危機対応医薬品(MCM)
有事に備えMCMの開発は重要であるが、平時に患者数が少ないため企業の開発が進みにくい現状があり、政府の「感染症協議会」に
おいて、プッシュ・プル型研究開発支援を通じたMCMエコシステムの構築が求められている。
• 再生医療等技術
超希少疾病に対する細胞医療や遺伝子治療については、国内で有望なシーズが出てきているが、高額な製造費用に加え、対象疾患の患
者数が限定的であること、有限の治療で完治に至るものもあることから、開発企業にとっては継続的な収益が見込みづらい事例なども
あり、開発が進みづらい。
海外で、開発・承認された、革新的な医薬品・医療技術の例
• 低分子治療薬
• アデノ随伴ウイルスベクター(AAV)を用いたin vivo遺伝子治療
対象疾患:嚢胞性線維症(先天性肺疾患)
対象疾患:芳香族L-アミノ酸脱炭酸酵素欠損症(先天性神経疾患)
海外承認状況:米国等で承認済み
海外承認状況:米国で承認済み
国内想定患者数:50人程度
国内想定患者数:10人程度
2
我が国における医薬品・医療技術開発の現状と課題
特定医療技術等開発推進検討会
令和8年3月16日
資料1
患者数が特に少ない超希少疾病等に対しては、市場性等の課題から、企業による医薬品や医療技術の開発が進まない現状がある。
他方、海外においては、超希少疾病に対しても、新規的な治療薬の開発が認められる。
医薬品・医療技術の開発における市場性等の課題の例
• ドラッグ・ロス
海外承認済だが、国内開発未着手・未承認の医薬品(ドラッグ・ロス)については、政府が情報収集し、企業への開発要請等を行って
いる。2016年から2020年に欧米で承認された品目のうち、ドラッグ・ロス品目は86品目あり、医療上の必要性を確認するべきと判断
された品目が55品目、その中から開発要請・開発公募に繋がった品目が23品目であり、開発公募品目のうち2品目について企業から開
発の意思の申し出があった。
ドラッグ・ロス86品目の中にはベンチャー企業が開発したものが56%、希少疾病用医薬品が47%、小児用医薬品が37%あり、日本の
医療環境の周知、市場規模の小さい医薬品の導入が課題となっている。
• 感染症に対する危機対応医薬品(MCM)
有事に備えMCMの開発は重要であるが、平時に患者数が少ないため企業の開発が進みにくい現状があり、政府の「感染症協議会」に
おいて、プッシュ・プル型研究開発支援を通じたMCMエコシステムの構築が求められている。
• 再生医療等技術
超希少疾病に対する細胞医療や遺伝子治療については、国内で有望なシーズが出てきているが、高額な製造費用に加え、対象疾患の患
者数が限定的であること、有限の治療で完治に至るものもあることから、開発企業にとっては継続的な収益が見込みづらい事例なども
あり、開発が進みづらい。
海外で、開発・承認された、革新的な医薬品・医療技術の例
• 低分子治療薬
• アデノ随伴ウイルスベクター(AAV)を用いたin vivo遺伝子治療
対象疾患:嚢胞性線維症(先天性肺疾患)
対象疾患:芳香族L-アミノ酸脱炭酸酵素欠損症(先天性神経疾患)
海外承認状況:米国等で承認済み
海外承認状況:米国で承認済み
国内想定患者数:50人程度
国内想定患者数:10人程度
2