よむ、つかう、まなぶ。
総-3-1【最適GL】レチファンリマブ(肛門管扁平上皮癌) (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
3.臨床成績
切除不能な進行・再発の肛門管扁平上皮癌の承認時に評価を行った主な臨床試験の成
績を示す。
【有効性】
① 国際共同第Ⅲ相臨床試験(INCMGA 0012-303 試験)
化学療法歴のない*1 切除不能な進行・再発の肛門管扁平上皮癌患者*2308 例(日本人 16 例
を含む)を対象に、パクリタキセルとカルボプラチンとの併用投与下で本剤(154 例*3)と
プラセボ(154 例*4)の有効性及び安全性を検討した*5。
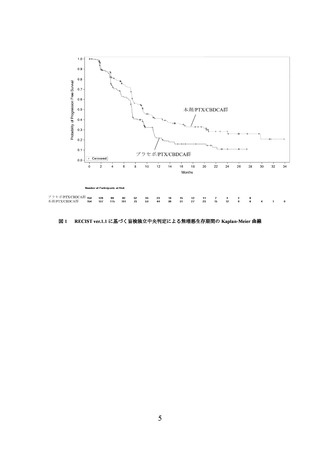
主要評価項目である RECIST ver.1.1 に基づく盲検下独立中央判定による無増悪生存期間
(中央値[95%信頼区間]
)は、本剤、パクリタキセル及びカルボプラチンの併用(以下、
「本剤/PTX/CBDCA」という。
)群で 9.3[7.5~11.3]ヵ月、プラセボ、パクリタキセル及び
カルボプラチンの併用(以下、
「プラセボ/PTX/CBDCA」という。
)群で 7.4[7.1~7.7]ヵ
月であり、本剤/PTX/CBDCA 群はプラセボ/PTX/CBDCA 群に対し統計学的に有意な延長
を示した(ハザード比 0.63[95%信頼区間:0.47~0.84]
、p=0.0006[層別 log-rank 検定]
、
有意水準(片側)0.025、2024 年 4 月 15 日データカットオフ)。
*1:放射線療法と併用する化学療法又は登録の 6 カ月以上前に完了している術前若しくは術後補助療法
は許容された。
*2:切除不能な局所再発又は遠隔転移を有する患者が対象とされた。
*3:PD-L1 発現<1%:11 例、≧1%かつ<5%:17 例、≧5%:123 例を含む
*4:PD-L1 発現<1%:7 例、≧1%かつ<5%:19 例、≧5%:121 例を含む
*5:4 週間を 1 サイクルとして、本剤 500 mg 又はプラセボを第 1 日目に、カルボプラチン AUC 5 mg・
min/mL 相当量を第 1 日目に、パクリタキセル 80 mg/m2 を第 1、8 及び 15 日目に最大 6 サイクル投
与後、4 週間間隔で本剤 500 mg 又はプラセボを単独で投与した。本薬又はプラセボの投与期間は
最大 13 サイクルとした。なお、プラセボ/PTX/CBDCA 群に割り付けられた患者は、盲検下独立
中央判定により疾患進行が確認された場合にはクロスオーバー期に移行し、本薬 500 mg を 4 週間
間隔で投与することが可能とされた。
4
切除不能な進行・再発の肛門管扁平上皮癌の承認時に評価を行った主な臨床試験の成
績を示す。
【有効性】
① 国際共同第Ⅲ相臨床試験(INCMGA 0012-303 試験)
化学療法歴のない*1 切除不能な進行・再発の肛門管扁平上皮癌患者*2308 例(日本人 16 例
を含む)を対象に、パクリタキセルとカルボプラチンとの併用投与下で本剤(154 例*3)と
プラセボ(154 例*4)の有効性及び安全性を検討した*5。
主要評価項目である RECIST ver.1.1 に基づく盲検下独立中央判定による無増悪生存期間
(中央値[95%信頼区間]
)は、本剤、パクリタキセル及びカルボプラチンの併用(以下、
「本剤/PTX/CBDCA」という。
)群で 9.3[7.5~11.3]ヵ月、プラセボ、パクリタキセル及び
カルボプラチンの併用(以下、
「プラセボ/PTX/CBDCA」という。
)群で 7.4[7.1~7.7]ヵ
月であり、本剤/PTX/CBDCA 群はプラセボ/PTX/CBDCA 群に対し統計学的に有意な延長
を示した(ハザード比 0.63[95%信頼区間:0.47~0.84]
、p=0.0006[層別 log-rank 検定]
、
有意水準(片側)0.025、2024 年 4 月 15 日データカットオフ)。
*1:放射線療法と併用する化学療法又は登録の 6 カ月以上前に完了している術前若しくは術後補助療法
は許容された。
*2:切除不能な局所再発又は遠隔転移を有する患者が対象とされた。
*3:PD-L1 発現<1%:11 例、≧1%かつ<5%:17 例、≧5%:123 例を含む
*4:PD-L1 発現<1%:7 例、≧1%かつ<5%:19 例、≧5%:121 例を含む
*5:4 週間を 1 サイクルとして、本剤 500 mg 又はプラセボを第 1 日目に、カルボプラチン AUC 5 mg・
min/mL 相当量を第 1 日目に、パクリタキセル 80 mg/m2 を第 1、8 及び 15 日目に最大 6 サイクル投
与後、4 週間間隔で本剤 500 mg 又はプラセボを単独で投与した。本薬又はプラセボの投与期間は
最大 13 サイクルとした。なお、プラセボ/PTX/CBDCA 群に割り付けられた患者は、盲検下独立
中央判定により疾患進行が確認された場合にはクロスオーバー期に移行し、本薬 500 mg を 4 週間
間隔で投与することが可能とされた。
4