よむ、つかう、まなぶ。
【資料2】感染症法に基づく病原体等管理規制の「除外の対象となる病原体の考え方」の変更について(報告事項) (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70821.html |
| 出典情報 | 厚生科学審議会 感染症部会(第102回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
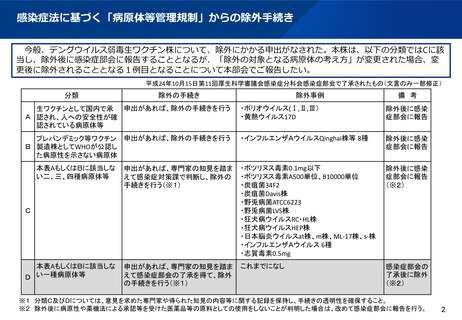
感染症法に基づく「病原体等管理規制」からの除外手続き
今般、デングウイルス弱毒生ワクチン株について、除外にかかる申出がなされた。本株は、以下の分類ではCに該
当し、除外後に感染症部会に報告することとなるが、「除外の対象となる病原体の考え方」が変更された場合、変
更後に除外されることとなる1例目となることについて本部会でご報告したい。
平成24年10月15日第11回厚生科学審議会感染症分科会感染症部会で了承されたもの(文言のみ一部修正)
分類
除外の手続き
除外事例
備 考
生ワクチンとして国内で承 申出があれば、除外の手続きを行う
A 認され、人への安全性が確
認されている病原体等
・ポリオウイルス(Ⅰ,Ⅱ,Ⅲ)
・黄熱ウイルス17D
除外後に感染
症部会に報告
プレパンデミック等ワクチン 申出があれば、除外の手続きを行う
B 製造株としてWHOが公認し
た病原性を示さない病原体
・インフルエンザAウイルスQinghai株等 8種
除外後に感染
症部会に報告
本表AもしくはBに該当しな
い二、三、四種病原体等
申出があれば、専門家の知見を踏ま
えて感染症対策課で判断し、除外の
手続きを行う(※1)
・ボツリヌス毒素0.1mg以下
・ボツリヌス毒素A500単位、B10000単位
・炭疽菌34F2
・炭疽菌Davis株
・野兎病菌ATCC6223
・野兎病菌LVS株
・狂犬病ウイルスRC・HL株
・狂犬病ウイルスHEP株
・日本脳炎ウイルスat株、m株、ML-17株、s-株
・インフルエンザAウイルス 6種
・志賀毒素0.5mg
除外後に感染
症部会に報告
(※2)
本表AもしくはBに該当しな
D い一種病原体等
申出があれば、専門家の知見を踏ま
えて感染症部会の了承を得て、除外
の手続きを行う(※1)
これまでになし
感染症部会の
了承後に除外
(※2)
C
※1 分類C及びDについては、意見を求めた専門家や得られた知見の内容等に関する記録を保持し、手続きの透明性を確保すること。
※2 除外後に病原性や薬機法による承認等を受けた医薬品等の原料としての使用をしないことが判明した場合は、改めて感染症部会に報告を行う。
2
今般、デングウイルス弱毒生ワクチン株について、除外にかかる申出がなされた。本株は、以下の分類ではCに該
当し、除外後に感染症部会に報告することとなるが、「除外の対象となる病原体の考え方」が変更された場合、変
更後に除外されることとなる1例目となることについて本部会でご報告したい。
平成24年10月15日第11回厚生科学審議会感染症分科会感染症部会で了承されたもの(文言のみ一部修正)
分類
除外の手続き
除外事例
備 考
生ワクチンとして国内で承 申出があれば、除外の手続きを行う
A 認され、人への安全性が確
認されている病原体等
・ポリオウイルス(Ⅰ,Ⅱ,Ⅲ)
・黄熱ウイルス17D
除外後に感染
症部会に報告
プレパンデミック等ワクチン 申出があれば、除外の手続きを行う
B 製造株としてWHOが公認し
た病原性を示さない病原体
・インフルエンザAウイルスQinghai株等 8種
除外後に感染
症部会に報告
本表AもしくはBに該当しな
い二、三、四種病原体等
申出があれば、専門家の知見を踏ま
えて感染症対策課で判断し、除外の
手続きを行う(※1)
・ボツリヌス毒素0.1mg以下
・ボツリヌス毒素A500単位、B10000単位
・炭疽菌34F2
・炭疽菌Davis株
・野兎病菌ATCC6223
・野兎病菌LVS株
・狂犬病ウイルスRC・HL株
・狂犬病ウイルスHEP株
・日本脳炎ウイルスat株、m株、ML-17株、s-株
・インフルエンザAウイルス 6種
・志賀毒素0.5mg
除外後に感染
症部会に報告
(※2)
本表AもしくはBに該当しな
D い一種病原体等
申出があれば、専門家の知見を踏ま
えて感染症部会の了承を得て、除外
の手続きを行う(※1)
これまでになし
感染症部会の
了承後に除外
(※2)
C
※1 分類C及びDについては、意見を求めた専門家や得られた知見の内容等に関する記録を保持し、手続きの透明性を確保すること。
※2 除外後に病原性や薬機法による承認等を受けた医薬品等の原料としての使用をしないことが判明した場合は、改めて感染症部会に報告を行う。
2