よむ、つかう、まなぶ。
資料2-4 要指導医薬品のリスク評価について[554KB] (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70725.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第4回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和8年3月6日
令和7年度第4回
医薬品等安全対策部会
資料2-4
要指導医薬品のリスク評価について
○
令和7年 11 月 11 日開催の安全対策調査会において、要指導医薬品に指定され
ていたプロピベリン塩酸塩について、製造販売後調査期間の終了見込みに伴
い、一般用医薬品としての適切性を確認するためのリスク評価を行った。
成分・含量
1日量(1錠)中
プロピベリン塩酸塩 10 ㎎
薬効分類
その他の泌尿生殖器官及び肛門用薬
投与経路
経口
販売名(製造販売業者) バップフォーレディ
(大鵬薬品工業株式会社)
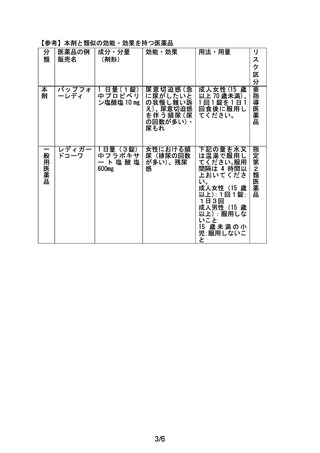
効能・効果
尿意切迫感(急に尿がしたいとの我慢し難い訴え)、尿意切迫
感を伴う頻尿(尿の回数が多い)・尿もれ
用法・用量
成人女性(15 歳以上 70 歳未満)、1 回 1 錠を 1 日 1 回食後に
服用してください。
承認年月日
2021 年5月 31 日
製造販売開始日
2021 年 11 月 24 日
評価を行う理由
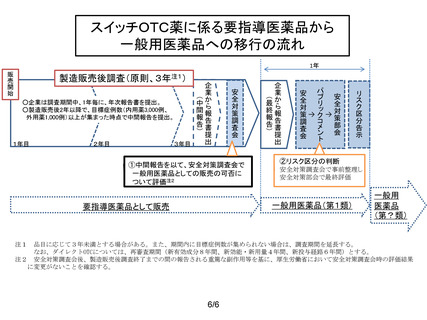
2026 年1月5日の製造販売後調査終了見込みに伴い、一般用
医薬品としての販売の可否について判断を行うため。
製造販売後調査概要
(中間報告書)
調査期間:2021 年 11 月 24 日~2025 年 5 月 15 日
(製造販売開始後、3 年 6 ヵ月間)
特別調査:3,308 症例(うち、安全性評価対象症例は 3,307 例)
副作用:235 例 340 件(7.1%)
うち重篤な副作用:尿閉 1 件※
未知の副作用:注意力障害、労作性呼吸困難、鼻乾燥、鼓
腸、口の錯感覚、黄色皮膚、膀胱刺激症状、腫瘤 各 1 件
一般調査
副作用:33 例 53 件
うち重篤な副作用:尿閉 1 件
未知の副作用:鼻出血、血尿、尿意切迫、上咽頭炎、夜間
頻尿、頻尿、硝子体浮遊物、体調不良 各 1 件
医薬品医療機器法第 中間報告書データロック後に、製造販売業者が報告した副作
68 条の 10 第1項に 用報告
基づき、製造販売業
2025 年 5 月 16 日~2025 年 10 月 8 日:0 件
者が報告した副作用
報告
1/6
令和7年度第4回
医薬品等安全対策部会
資料2-4
要指導医薬品のリスク評価について
○
令和7年 11 月 11 日開催の安全対策調査会において、要指導医薬品に指定され
ていたプロピベリン塩酸塩について、製造販売後調査期間の終了見込みに伴
い、一般用医薬品としての適切性を確認するためのリスク評価を行った。
成分・含量
1日量(1錠)中
プロピベリン塩酸塩 10 ㎎
薬効分類
その他の泌尿生殖器官及び肛門用薬
投与経路
経口
販売名(製造販売業者) バップフォーレディ
(大鵬薬品工業株式会社)
効能・効果
尿意切迫感(急に尿がしたいとの我慢し難い訴え)、尿意切迫
感を伴う頻尿(尿の回数が多い)・尿もれ
用法・用量
成人女性(15 歳以上 70 歳未満)、1 回 1 錠を 1 日 1 回食後に
服用してください。
承認年月日
2021 年5月 31 日
製造販売開始日
2021 年 11 月 24 日
評価を行う理由
2026 年1月5日の製造販売後調査終了見込みに伴い、一般用
医薬品としての販売の可否について判断を行うため。
製造販売後調査概要
(中間報告書)
調査期間:2021 年 11 月 24 日~2025 年 5 月 15 日
(製造販売開始後、3 年 6 ヵ月間)
特別調査:3,308 症例(うち、安全性評価対象症例は 3,307 例)
副作用:235 例 340 件(7.1%)
うち重篤な副作用:尿閉 1 件※
未知の副作用:注意力障害、労作性呼吸困難、鼻乾燥、鼓
腸、口の錯感覚、黄色皮膚、膀胱刺激症状、腫瘤 各 1 件
一般調査
副作用:33 例 53 件
うち重篤な副作用:尿閉 1 件
未知の副作用:鼻出血、血尿、尿意切迫、上咽頭炎、夜間
頻尿、頻尿、硝子体浮遊物、体調不良 各 1 件
医薬品医療機器法第 中間報告書データロック後に、製造販売業者が報告した副作
68 条の 10 第1項に 用報告
基づき、製造販売業
2025 年 5 月 16 日~2025 年 10 月 8 日:0 件
者が報告した副作用
報告
1/6