よむ、つかう、まなぶ。
参考資料1-2 (資料1-2関係)手続きに係るスキーム図[815KB] (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70725.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第4回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
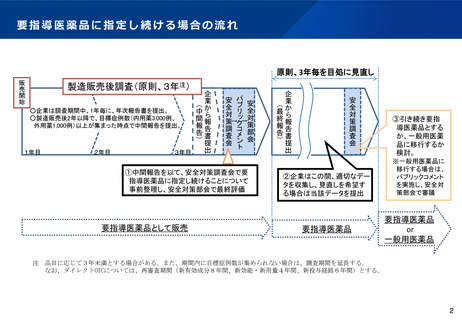
要指導医薬品に指定し続ける場合の流れ
原則、3年毎を目処に見直し
販
売
開
始
製造販売後調査(原則、3年注)
↑
安 パ 安
全 ブ 全
対 リ 対
策 ッ
ク 策
調 コ 部
査 メ 会
会 ン
ト
↑
企
業
(
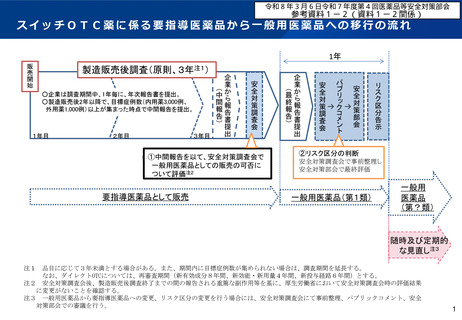
○企業は調査期間中、1年毎に、年次報告書を提出。
中か
ら
○製造販売後2年以降で、目標症例数(内用薬3,000例、
間報
外用薬1,000例)以上が集まった時点で中間報告を提出。
報告
告書
)提
出
1年目
2年目
3年目
①中間報告を以て、安全対策調査会で要
指導医薬品に指定し続けることについて
事前整理し、安全対策部会で最終評価
要指導医薬品として販売
企
業
(
最か
ら
終報
報告
告書
)提
出
安
全
対
策
調
査
会
②企業はこの間、適切なデー
タを収集し、見直しを希望す
る場合は当該データを提出
要指導医薬品
③引き続き要指
導医薬品とする
か、一般用医薬
品に移行するか
検討。
※一般用医薬品に
移行する場合は、
パブリックコメント
を実施し、安全対
策部会で審議
要指導医薬品
or
一般用医薬品
注 品目に応じて3年未満とする場合がある。また、期間内に目標症例数が集められない場合は、調査期間を延長する。
なお、ダイレクトOTCについては、再審査期間(新有効成分8年間、新効能・新用量4年間、新投与経路6年間)とする。
2
原則、3年毎を目処に見直し
販
売
開
始
製造販売後調査(原則、3年注)
↑
安 パ 安
全 ブ 全
対 リ 対
策 ッ
ク 策
調 コ 部
査 メ 会
会 ン
ト
↑
企
業
(
○企業は調査期間中、1年毎に、年次報告書を提出。
中か
ら
○製造販売後2年以降で、目標症例数(内用薬3,000例、
間報
外用薬1,000例)以上が集まった時点で中間報告を提出。
報告
告書
)提
出
1年目
2年目
3年目
①中間報告を以て、安全対策調査会で要
指導医薬品に指定し続けることについて
事前整理し、安全対策部会で最終評価
要指導医薬品として販売
企
業
(
最か
ら
終報
報告
告書
)提
出
安
全
対
策
調
査
会
②企業はこの間、適切なデー
タを収集し、見直しを希望す
る場合は当該データを提出
要指導医薬品
③引き続き要指
導医薬品とする
か、一般用医薬
品に移行するか
検討。
※一般用医薬品に
移行する場合は、
パブリックコメント
を実施し、安全対
策部会で審議
要指導医薬品
or
一般用医薬品
注 品目に応じて3年未満とする場合がある。また、期間内に目標症例数が集められない場合は、調査期間を延長する。
なお、ダイレクトOTCについては、再審査期間(新有効成分8年間、新効能・新用量4年間、新投与経路6年間)とする。
2