よむ、つかう、まなぶ。
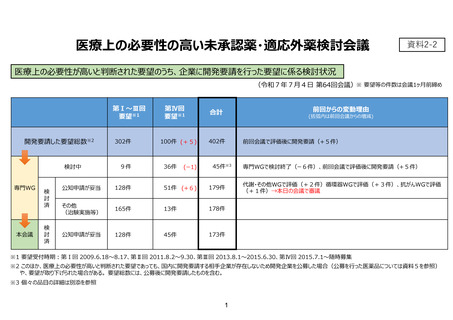
資料2-2 開発要請を行った要望に係る検討状況等について[341KB] (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第68回 7/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
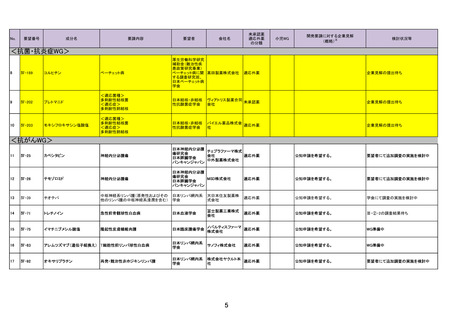
No.
要望番号
成分名
要請内容
要望者
会社名
未承認薬
適応外薬
の分類
小児WG
開発要請に対する企業見解
注
(概略)
検討状況等
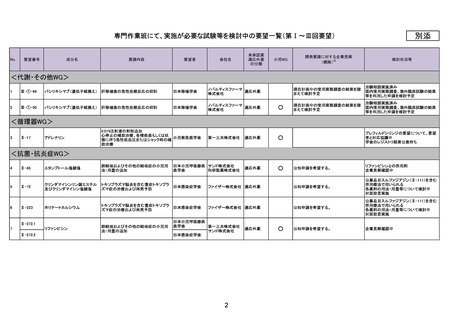
29
Ⅳ-171
オキサリプラチン
膵癌
日本膵臓学会
株式会社ヤクルト本
適応外薬
社
公知申請を希望する。
企業見解確認中
30
Ⅳ-172
イリノテカン塩酸塩水和物
膵癌
日本膵臓学会
株式会社ヤクルト本
社
適応外薬
アルフレッサファーマ
株式会社
公知申請を希望する。
企業見解確認中
31
Ⅳ-173
フルオロウラシル
膵癌
日本膵臓学会
協和キリン株式会社 適応外薬
公知申請を希望する。
企業見解確認中
32
Ⅳ-174
レボホリナートカルシウム水和物 膵癌
日本膵臓学会
ファイザー株式会社 適応外薬
公知申請を希望する。
企業見解確認中
33
Ⅳ-183
再発又は難治性病変に対する治療後に疾患
Naxitamab-gqgk[Naxitamab, ナキシ
進行を認めないものの骨及び/又は骨髄に 神経芽腫の会
タマブ]
病変の残存した高リスク神経芽腫
ノーベルファーマ株
式会社
未承認薬
治験の実施を検討する。
-
34
Ⅳ-190
ペムブロリズマブ(遺伝子組換
え)
がん化学療法後に増悪した絨毛性腫瘍
(絨毛癌*、PSTT、ETT)
*
臨床的絨毛癌、high-risk GTN を含む
日本産科婦人科学
会/日本婦人科腫
MSD株式会社
瘍学会/日本絨毛
性疾患研究会
適応外薬
申請方法について検討中。
企業見解確認中(企業からの追加情報待
ち)
35
Ⅳ-197
イリノテカン塩酸塩水和物
再発・難治性神経芽腫
日本小児血液・が
ん学会
アルフレッサ ファー
マ株式会社
適応外薬
〇
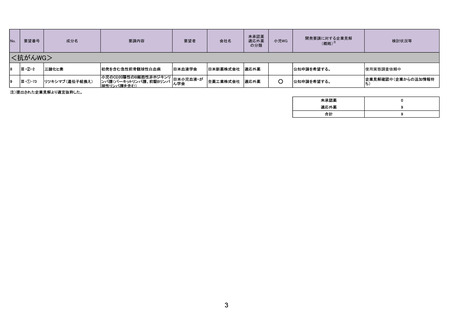
36
ⅣS-25
メルファラン
網膜芽細胞腫
小児血液・がん学
会
サンドファーマ株式
会社
迅速実用化
○
企業見解の提出待ち
公知申請を希望する。
企業見解確認中
注)提出された企業見解より適宜抜粋した。
7
未承認薬
3
適応外薬
31
迅速実用化
2
合計
36
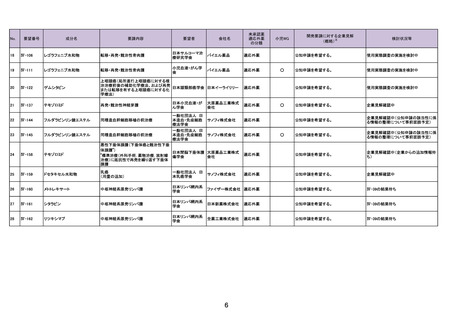
要望番号
成分名
要請内容
要望者
会社名
未承認薬
適応外薬
の分類
小児WG
開発要請に対する企業見解
注
(概略)
検討状況等
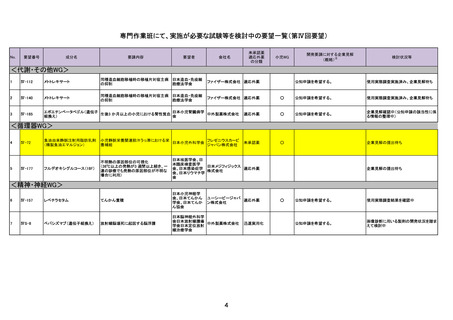
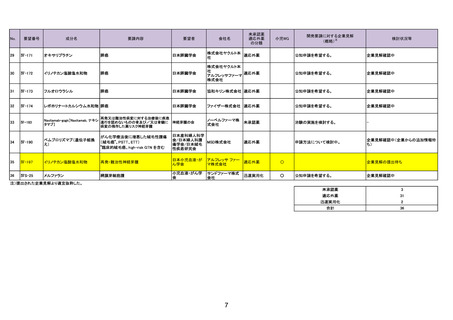
29
Ⅳ-171
オキサリプラチン
膵癌
日本膵臓学会
株式会社ヤクルト本
適応外薬
社
公知申請を希望する。
企業見解確認中
30
Ⅳ-172
イリノテカン塩酸塩水和物
膵癌
日本膵臓学会
株式会社ヤクルト本
社
適応外薬
アルフレッサファーマ
株式会社
公知申請を希望する。
企業見解確認中
31
Ⅳ-173
フルオロウラシル
膵癌
日本膵臓学会
協和キリン株式会社 適応外薬
公知申請を希望する。
企業見解確認中
32
Ⅳ-174
レボホリナートカルシウム水和物 膵癌
日本膵臓学会
ファイザー株式会社 適応外薬
公知申請を希望する。
企業見解確認中
33
Ⅳ-183
再発又は難治性病変に対する治療後に疾患
Naxitamab-gqgk[Naxitamab, ナキシ
進行を認めないものの骨及び/又は骨髄に 神経芽腫の会
タマブ]
病変の残存した高リスク神経芽腫
ノーベルファーマ株
式会社
未承認薬
治験の実施を検討する。
-
34
Ⅳ-190
ペムブロリズマブ(遺伝子組換
え)
がん化学療法後に増悪した絨毛性腫瘍
(絨毛癌*、PSTT、ETT)
*
臨床的絨毛癌、high-risk GTN を含む
日本産科婦人科学
会/日本婦人科腫
MSD株式会社
瘍学会/日本絨毛
性疾患研究会
適応外薬
申請方法について検討中。
企業見解確認中(企業からの追加情報待
ち)
35
Ⅳ-197
イリノテカン塩酸塩水和物
再発・難治性神経芽腫
日本小児血液・が
ん学会
アルフレッサ ファー
マ株式会社
適応外薬
〇
36
ⅣS-25
メルファラン
網膜芽細胞腫
小児血液・がん学
会
サンドファーマ株式
会社
迅速実用化
○
企業見解の提出待ち
公知申請を希望する。
企業見解確認中
注)提出された企業見解より適宜抜粋した。
7
未承認薬
3
適応外薬
31
迅速実用化
2
合計
36