よむ、つかう、まなぶ。
資 料 3-1 令和5年度第2回安全技術調査会の概要について (82 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38341.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会運営委員会(令和5年度第4回 3/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(参考)
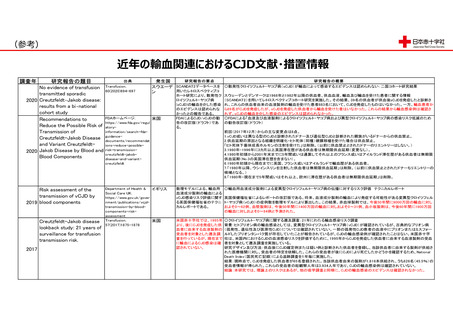
近年の輸血関連におけるCJD文献・措置情報
調査年
出典
研究報告の要点
研究報告の概要
発生国
研究報告の題目
スウエーデ SCANDAT2データベースを 〇散発性クロイツフェルト・ヤコブ病(sCJD)が輸血によって感染するエビデンスは認められない:二国コホート研究結果
No evidence of transfusion Transfusion.
60(2020)694-697
用いたレトロスペクティブコ
ン
transmitted sporadic
ホート研究により、散発性ク スウェーデンとデンマークは1968年と1982年以降の供血者、供血血液、輸血及び輸血を受けた患者に関する情報
ロイツフェルト・ヤコブ病
(SCANDAT2)を用いてレトロスペクティブコホート研究を実施した。その結果、39名の供血者が供血後sCJDを発症したと診断さ
2020 Creutzfeldt‐Jakob disease:
(sCJD)の輸血を介した感染 れ、これらの供血者由来の血液製剤の輸血を受けた患者883名において、CJDを発症したものはいなかった。一方、輸血患者か
results from a bi‐national
のエビデンスは認められな ら89名がCJDを発症したが、sCJDを発症した供血者から輸血を受けた者はいなかった。これらの結果から輸血感染例は確認さ
cohort study
かったとの報告である。
れず、sCJDの輸血を介した感染のエビデンスは認められなかった。
FDAホームページ.
FDAによるCJD/vCJDの勧 〇FDAによる「血液及び血液製剤によるクロイツフェルト・ヤコブ病および異型クロイツフェルト・ヤコブ病の感染リスク低減のため
米国
Recommendations to
https://www.fda.gov/regul
告の改訂版(ドラフト)であ の勧告改訂版(ドラフト)
Reduce the Possible Risk of atoryる。
information/search-fda前回(2017年12月)からの主な変更点は8点。
Transmission of
1.vCJD或いは異なる型のCJDと診断されたドナー及び遺伝型CJDと診断された親族がいるドナーからの供血禁止。
Creutzfeldt-Jakob Disease guidancedocuments/recommendat
2.供血延期の原因となる組織を明確化-ヒト死体(同種)硬膜移植を受けた場合は供血禁止。
and Variant Creutzfeldtions-reduce-possible「ヒト死体下垂体成長ホルモンの注射を受けた」は削除。(以前に供血禁止とされたドナーのリエントリーはしない。)
3.1980年-1996年に3カ月以上英国滞在歴がある供血者は無期限供血延期(変更なし)。
2020 Jakob Disease by Blood and risk-transmissioncreutzfeldt-jakob4.1980年初頭から2001年末までに5年間或いは通算してそれ以上のフランス或いはアイルランド滞在歴がある供血者は無期限
Blood Components
disease-and-variant供血延期(No.3の英国滞在歴を含まない)。
creutzfeldt
Risk assessment of the
transmission of vCJD by
2019 blood components
Creutzfeldt-Jakob disease
lookback study: 21 years of
surveillance for transfusion
transmission risk.
2017
Department of Health &
イギリス
Social Care UK.
https://www.gov.uk/gover
nment/publications/vcjdtransmission-by-bloodcomponents-riskassessment
Transfusion.
米国
57(2017)1875-1878
6.1980年初頭から現在までに英国、フランス或いはアイルランドで輸血歴がある供血者。
7.「1980年以降、ウシインスリンを注射した供血者は無期限供血延期」は削除。(以前に供血禁止とされたドナーもリエントリーの
候補となる。)
8.「1980年-現在まで5年間或いはそれ以上、欧州に滞在歴がある供血者は無期限供血延期」は削除。
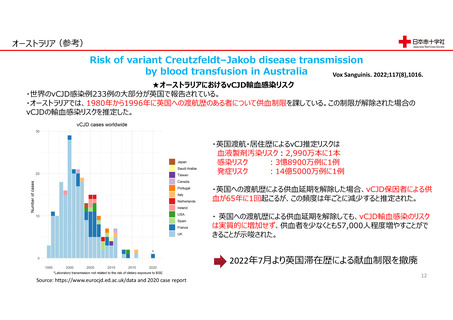
数理モデルによる、輸血用 〇輸血用血液成分製剤による変異型クロイツフェルト・ヤコブ病の伝播に対するリスク評価 テクニカルレポート
血液成分製剤の輸血による
vCJD感染リスク評価に関す 英国保健福祉省によるレポートの改訂版である。将来、血液成分製剤の輸血により発症する可能性がある変異型クロイツフェル
る英国保健福祉省のテクニ ト・ヤコブ病(vCJD)の症例数を数理モデルにより算出した。この結果、赤血球製剤では、今後50年間に9000万回の輸血に対し
カルレポートである。
およそ0~62例、血漿製剤は、今後50年間に1400万回の輸血に対しおよそ0~31例、血小板製剤は、今後60年間に1900万回
の輸血に対しおよそ0~84例と予測された。
米国赤十字社では、1995年 〇クロイツフェルト・ヤコブ病に関する遡及調査:21年にわたる輸血感染リスク調査
より、後にCJDを発症した供 背景:ヒトプリオン病の輸血感染としては、変異型クロイツフェルト・ヤコブ病(vCJD)が確認されているが、古典的なプリオン病
血者に由来する血液製剤の (孤発性、遺伝性及び医原性CJD)については確認されていない。一部の孤発性CJD患者の血液中にプリオンまたはミスフォー
受血者を対象とした遡及調 ルドしたプリオンタンパク質が存在していたことが報告されているが、CJDの輸血感染例が確認されたことはない。米国赤十字
査を行っているが、現在まで 社は、米国内におけるCJDの血液感染リスクを評価するために、1995年からCJDを発症した供血者に由来する血液製剤の受血
に輸血によるCJD感染は確 者を対象として遡及調査を実施している。
認されていない。
研究デザイン及び方法:供血後にCJD確定例または疑い例と診断された供血者を登録し、当該供血者に由来する製剤が供給さ
れた医療機関に対し、受血者の特定を依頼した。これらの受血者が後にCJDにより死亡したかどうかを確認するため、National
Death Index(国民死亡記録)による追跡調査を1年毎に実施した。
結果:現時点で、CJDを発症した供血者が65名登録された。当該供血者由来の製剤が1,816本供給され、うち826名(45.5%)の
受血者情報が得られた。これらの受血者の総観察人年は3,934人年であり、CJDの輸血感染例は確認されていない。
結論:本研究では、理論上のリスクはあるが、他の疫学調査と同様に、CJDの輸血感染のエビデンスは確認されなかった。
7
81
近年の輸血関連におけるCJD文献・措置情報
調査年
出典
研究報告の要点
研究報告の概要
発生国
研究報告の題目
スウエーデ SCANDAT2データベースを 〇散発性クロイツフェルト・ヤコブ病(sCJD)が輸血によって感染するエビデンスは認められない:二国コホート研究結果
No evidence of transfusion Transfusion.
60(2020)694-697
用いたレトロスペクティブコ
ン
transmitted sporadic
ホート研究により、散発性ク スウェーデンとデンマークは1968年と1982年以降の供血者、供血血液、輸血及び輸血を受けた患者に関する情報
ロイツフェルト・ヤコブ病
(SCANDAT2)を用いてレトロスペクティブコホート研究を実施した。その結果、39名の供血者が供血後sCJDを発症したと診断さ
2020 Creutzfeldt‐Jakob disease:
(sCJD)の輸血を介した感染 れ、これらの供血者由来の血液製剤の輸血を受けた患者883名において、CJDを発症したものはいなかった。一方、輸血患者か
results from a bi‐national
のエビデンスは認められな ら89名がCJDを発症したが、sCJDを発症した供血者から輸血を受けた者はいなかった。これらの結果から輸血感染例は確認さ
cohort study
かったとの報告である。
れず、sCJDの輸血を介した感染のエビデンスは認められなかった。
FDAホームページ.
FDAによるCJD/vCJDの勧 〇FDAによる「血液及び血液製剤によるクロイツフェルト・ヤコブ病および異型クロイツフェルト・ヤコブ病の感染リスク低減のため
米国
Recommendations to
https://www.fda.gov/regul
告の改訂版(ドラフト)であ の勧告改訂版(ドラフト)
Reduce the Possible Risk of atoryる。
information/search-fda前回(2017年12月)からの主な変更点は8点。
Transmission of
1.vCJD或いは異なる型のCJDと診断されたドナー及び遺伝型CJDと診断された親族がいるドナーからの供血禁止。
Creutzfeldt-Jakob Disease guidancedocuments/recommendat
2.供血延期の原因となる組織を明確化-ヒト死体(同種)硬膜移植を受けた場合は供血禁止。
and Variant Creutzfeldtions-reduce-possible「ヒト死体下垂体成長ホルモンの注射を受けた」は削除。(以前に供血禁止とされたドナーのリエントリーはしない。)
3.1980年-1996年に3カ月以上英国滞在歴がある供血者は無期限供血延期(変更なし)。
2020 Jakob Disease by Blood and risk-transmissioncreutzfeldt-jakob4.1980年初頭から2001年末までに5年間或いは通算してそれ以上のフランス或いはアイルランド滞在歴がある供血者は無期限
Blood Components
disease-and-variant供血延期(No.3の英国滞在歴を含まない)。
creutzfeldt
Risk assessment of the
transmission of vCJD by
2019 blood components
Creutzfeldt-Jakob disease
lookback study: 21 years of
surveillance for transfusion
transmission risk.
2017
Department of Health &
イギリス
Social Care UK.
https://www.gov.uk/gover
nment/publications/vcjdtransmission-by-bloodcomponents-riskassessment
Transfusion.
米国
57(2017)1875-1878
6.1980年初頭から現在までに英国、フランス或いはアイルランドで輸血歴がある供血者。
7.「1980年以降、ウシインスリンを注射した供血者は無期限供血延期」は削除。(以前に供血禁止とされたドナーもリエントリーの
候補となる。)
8.「1980年-現在まで5年間或いはそれ以上、欧州に滞在歴がある供血者は無期限供血延期」は削除。
数理モデルによる、輸血用 〇輸血用血液成分製剤による変異型クロイツフェルト・ヤコブ病の伝播に対するリスク評価 テクニカルレポート
血液成分製剤の輸血による
vCJD感染リスク評価に関す 英国保健福祉省によるレポートの改訂版である。将来、血液成分製剤の輸血により発症する可能性がある変異型クロイツフェル
る英国保健福祉省のテクニ ト・ヤコブ病(vCJD)の症例数を数理モデルにより算出した。この結果、赤血球製剤では、今後50年間に9000万回の輸血に対し
カルレポートである。
およそ0~62例、血漿製剤は、今後50年間に1400万回の輸血に対しおよそ0~31例、血小板製剤は、今後60年間に1900万回
の輸血に対しおよそ0~84例と予測された。
米国赤十字社では、1995年 〇クロイツフェルト・ヤコブ病に関する遡及調査:21年にわたる輸血感染リスク調査
より、後にCJDを発症した供 背景:ヒトプリオン病の輸血感染としては、変異型クロイツフェルト・ヤコブ病(vCJD)が確認されているが、古典的なプリオン病
血者に由来する血液製剤の (孤発性、遺伝性及び医原性CJD)については確認されていない。一部の孤発性CJD患者の血液中にプリオンまたはミスフォー
受血者を対象とした遡及調 ルドしたプリオンタンパク質が存在していたことが報告されているが、CJDの輸血感染例が確認されたことはない。米国赤十字
査を行っているが、現在まで 社は、米国内におけるCJDの血液感染リスクを評価するために、1995年からCJDを発症した供血者に由来する血液製剤の受血
に輸血によるCJD感染は確 者を対象として遡及調査を実施している。
認されていない。
研究デザイン及び方法:供血後にCJD確定例または疑い例と診断された供血者を登録し、当該供血者に由来する製剤が供給さ
れた医療機関に対し、受血者の特定を依頼した。これらの受血者が後にCJDにより死亡したかどうかを確認するため、National
Death Index(国民死亡記録)による追跡調査を1年毎に実施した。
結果:現時点で、CJDを発症した供血者が65名登録された。当該供血者由来の製剤が1,816本供給され、うち826名(45.5%)の
受血者情報が得られた。これらの受血者の総観察人年は3,934人年であり、CJDの輸血感染例は確認されていない。
結論:本研究では、理論上のリスクはあるが、他の疫学調査と同様に、CJDの輸血感染のエビデンスは確認されなかった。
7
81