よむ、つかう、まなぶ。
資料2-1 がんゲノム医療中核拠点病院等の指定要件等について (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_37348.html |
| 出典情報 | がん診療提供体制のあり方に関する検討会(第15回 1/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第5回がんゲノム医療中核拠点病院等の
指定要件に関するワーキンググループ
遺伝子パネル検査におけるエビデンスレベルについて
令和5年12月1日
資料1
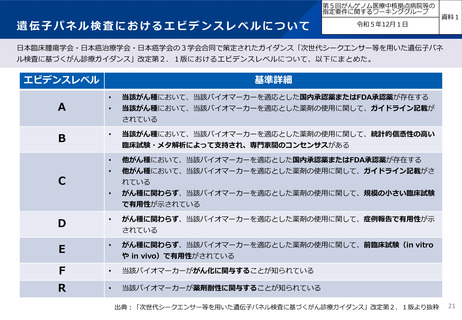
日本臨床腫瘍学会・日本癌治療学会・日本癌学会の3学会合同で策定されたガイダンス「次世代シークエンサー等を用いた遺伝子パネ
ル検査に基づくがん診療ガイダンス」改定第2.1版におけるエビデンスレベルについて、以下にまとめた。
エビデンスレベル
A
基準詳細
•
当該がん種において、当該バイオマーカーを適応とした国内承認薬またはFDA承認薬が存在する
•
当該がん種において、当該バイオマーカーを適応とした薬剤の使用に関して、ガイドライン記載が
されている
B
C
•
当該がん種において、当該バイオマーカーを適応とした薬剤の使用に関して、統計的信憑性の高い
臨床試験・メタ解析によって支持され、専門家間のコンセンサスがある
•
他がん種において、当該バイオマーカーを適応とした国内承認薬またはFDA承認薬が存在する
•
他がん種において、当該バイオマーカーを適応とした薬剤の使用に関して、ガイドライン記載がさ
れている
•
がん種に関わらず、当該バイオマーカーを適応とした薬剤の使用に関して、規模の小さい臨床試験
で有用性が示されている
がん種に関わらず、当該バイオマーカーを適応とした薬剤の使用に関して、症例報告で有用性が示
D
•
E
•
F
•
当該バイオマーカーががん化に関与することが知られている
R
•
当該バイオマーカーが薬剤耐性に関与することが知られている
されている
がん種に関わらず、当該バイオマーカーを適応とした薬剤の使用に関して、前臨床試験(in vitro
や in vivo)で有用性がされている
出典:「次世代シークエンサー等を用いた遺伝子パネル検査に基づくがん診療ガイダンス」改定第2.1版より抜粋
21
指定要件に関するワーキンググループ
遺伝子パネル検査におけるエビデンスレベルについて
令和5年12月1日
資料1
日本臨床腫瘍学会・日本癌治療学会・日本癌学会の3学会合同で策定されたガイダンス「次世代シークエンサー等を用いた遺伝子パネ
ル検査に基づくがん診療ガイダンス」改定第2.1版におけるエビデンスレベルについて、以下にまとめた。
エビデンスレベル
A
基準詳細
•
当該がん種において、当該バイオマーカーを適応とした国内承認薬またはFDA承認薬が存在する
•
当該がん種において、当該バイオマーカーを適応とした薬剤の使用に関して、ガイドライン記載が
されている
B
C
•
当該がん種において、当該バイオマーカーを適応とした薬剤の使用に関して、統計的信憑性の高い
臨床試験・メタ解析によって支持され、専門家間のコンセンサスがある
•
他がん種において、当該バイオマーカーを適応とした国内承認薬またはFDA承認薬が存在する
•
他がん種において、当該バイオマーカーを適応とした薬剤の使用に関して、ガイドライン記載がさ
れている
•
がん種に関わらず、当該バイオマーカーを適応とした薬剤の使用に関して、規模の小さい臨床試験
で有用性が示されている
がん種に関わらず、当該バイオマーカーを適応とした薬剤の使用に関して、症例報告で有用性が示
D
•
E
•
F
•
当該バイオマーカーががん化に関与することが知られている
R
•
当該バイオマーカーが薬剤耐性に関与することが知られている
されている
がん種に関わらず、当該バイオマーカーを適応とした薬剤の使用に関して、前臨床試験(in vitro
や in vivo)で有用性がされている
出典:「次世代シークエンサー等を用いた遺伝子パネル検査に基づくがん診療ガイダンス」改定第2.1版より抜粋
21