よむ、つかう、まなぶ。
【資料2-1】医薬品の品質確保に向けた取組みについて(医薬局からの説明資料) (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_37109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第14回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
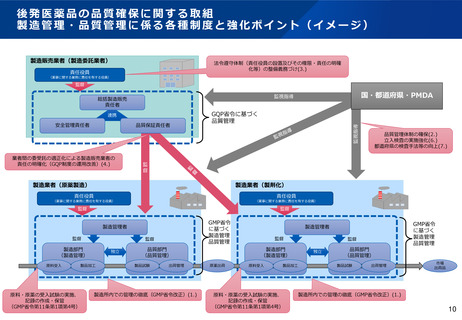
後発医薬品の品質確保に関する取組
製造管理・品質管理に係る各種制度と強化ポイント(イメージ)
製造販売業者(製造委託業者)
法令遵守体制(責任役員の設置及びその権限・責任の明確
化等)の整備義務づけ(3.)
責任役員
(薬事に関する業務に責任を有する役員)
監督
品質保証責任者
業者間の委受託の適正化による製造販売業者の
責任の明確化(GQP制度の運用改善)(4.)
GQP省令に基づく
品質管理
監視指導
連携
安全管理責任者
国・都道府県・PMDA
監視指導
総括製造販売
責任者
監
督
製造業者(原薬製造)
製造業者(製剤化)
責任役員
責任役員
(薬事に関する業務に責任を有する役員)
(薬事に関する業務に責任を有する役員)
監督
監督
GMP省令
に基づく
製造管理
品質管理
製造管理者
監督
監督
製造部門
(製造管理)
原料受入
独立
製品加工
原料・原薬の受入試験の実施、
記録の作成・保管
(GMP省令第11条第1項第4号)
品質管理体制の確保(2.)
立入検査の実施強化(6.)
都道府県の検査手法等の向上(7.)
品質部門
(品質管理)
製品試験
出荷管理
製造所内での管理の徹底(GMP省令改正)(1.)
監督
製造部門
(製造管理)
原薬出荷
GMP省令
に基づく
製造管理
品質管理
製造管理者
原料受入
製品加工
原料・原薬の受入試験の実施、
記録の作成・保管
(GMP省令第11条第1項第4号)
監督
独立
品質部門
(品質管理)
製品試験
出荷管理
市場
出荷品
製造所内での管理の徹底(GMP省令改正)(1.)
10
製造管理・品質管理に係る各種制度と強化ポイント(イメージ)
製造販売業者(製造委託業者)
法令遵守体制(責任役員の設置及びその権限・責任の明確
化等)の整備義務づけ(3.)
責任役員
(薬事に関する業務に責任を有する役員)
監督
品質保証責任者
業者間の委受託の適正化による製造販売業者の
責任の明確化(GQP制度の運用改善)(4.)
GQP省令に基づく
品質管理
監視指導
連携
安全管理責任者
国・都道府県・PMDA
監視指導
総括製造販売
責任者
監
督
製造業者(原薬製造)
製造業者(製剤化)
責任役員
責任役員
(薬事に関する業務に責任を有する役員)
(薬事に関する業務に責任を有する役員)
監督
監督
GMP省令
に基づく
製造管理
品質管理
製造管理者
監督
監督
製造部門
(製造管理)
原料受入
独立
製品加工
原料・原薬の受入試験の実施、
記録の作成・保管
(GMP省令第11条第1項第4号)
品質管理体制の確保(2.)
立入検査の実施強化(6.)
都道府県の検査手法等の向上(7.)
品質部門
(品質管理)
製品試験
出荷管理
製造所内での管理の徹底(GMP省令改正)(1.)
監督
製造部門
(製造管理)
原薬出荷
GMP省令
に基づく
製造管理
品質管理
製造管理者
原料受入
製品加工
原料・原薬の受入試験の実施、
記録の作成・保管
(GMP省令第11条第1項第4号)
監督
独立
品質部門
(品質管理)
製品試験
出荷管理
市場
出荷品
製造所内での管理の徹底(GMP省令改正)(1.)
10