よむ、つかう、まなぶ。
資料4_「がん研究10か年戦略」に係る文部科学省における取組 (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32589.html |
| 出典情報 | 今後のがん研究のあり方に関する有識者会議(第10回 4/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
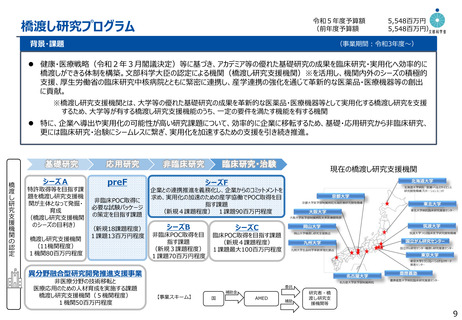
橋渡し研究支援事業 ~代表的な事業成果~
がんのウイルス療法 (開発名「G47Δ」)
R3.6悪性神経膠腫について製造販売承認取得
研究代表者:東京大学 藤堂 具紀
(販売名「デリタクト注」)
開発企業:第一三共株式会社
概要:
支援拠点:東京大学
がん細胞のみで増殖して細胞を破壊するウイルスによって、が
支援期間:2009年~
ん細胞を死滅させる。
支援内容:橋渡し事業研究費(2009~)
拠点は試験に参加する被験者問合せの窓口業務、データ
ウイルス感染
マネジメント業務、ウイルス製剤製造設備の維持、データ
センター・統計解析業務、モニタリング等の支援を担当。
がん細胞
成果:
ウイルス増殖と
2015年5月 膠芽腫に対する第II相医師主導治験開始
がん細胞の破壊
2016年2月 先駆け審査指定制度の対象品目に指定
2016年7月 企業へのライセンスアウト
2017年7月 希少疾病用製品の指定
がん細胞を
周囲への
2018年
悪性胸膜中皮腫に対する臨床研究開始
次々に破壊
ウイルス拡散
2018年7月 膠芽腫に対する第II相医師主導治験の中間解析において、
●膠芽腫:脳腫瘍の一種。最も悪性度が高い。
高い有効性を確認(有効中止)
●悪性胸膜中皮腫:肺を包む胸膜から発生する悪性腫瘍。
2020年12月 悪性神経膠腫に対して薬事承認申請
経口抗がん剤「ティーエスワン®」ホルモン受容体陽性かつHER2陰性で再発高リスクの乳癌
における術後薬物療法の適応追加承認を取得 概要:
研究代表者:京都大学 戸井雅和
開発企業:大鵬薬品工業株式会社
支援拠点:京都大学
支援期間:2011年~
支援内容:拠点は、リエゾン、開発・薬事戦略、スタディマネジ
メント、モニタリング、症例登録、データマネジメント
、統計解析、CRC、治験機器管理について支援
を行った。
成果:
2022年11月
医師主導臨床試験である「エストロゲン受容体陽性HER2陰性乳癌に対す
るTS-1術後療法」の結果より、TS-1と内分泌療法の併用は、再発中間リス
ク以上のエストロゲン受容体陽性かつHER2陰性の原発性乳がん患者さんに
対し、臨床的に意義のある浸潤性疾患のない生存期間(Invasive
Disease Free Survival:iDFS)の延長を認めた。
承認取得
10
がんのウイルス療法 (開発名「G47Δ」)
R3.6悪性神経膠腫について製造販売承認取得
研究代表者:東京大学 藤堂 具紀
(販売名「デリタクト注」)
開発企業:第一三共株式会社
概要:
支援拠点:東京大学
がん細胞のみで増殖して細胞を破壊するウイルスによって、が
支援期間:2009年~
ん細胞を死滅させる。
支援内容:橋渡し事業研究費(2009~)
拠点は試験に参加する被験者問合せの窓口業務、データ
ウイルス感染
マネジメント業務、ウイルス製剤製造設備の維持、データ
センター・統計解析業務、モニタリング等の支援を担当。
がん細胞
成果:
ウイルス増殖と
2015年5月 膠芽腫に対する第II相医師主導治験開始
がん細胞の破壊
2016年2月 先駆け審査指定制度の対象品目に指定
2016年7月 企業へのライセンスアウト
2017年7月 希少疾病用製品の指定
がん細胞を
周囲への
2018年
悪性胸膜中皮腫に対する臨床研究開始
次々に破壊
ウイルス拡散
2018年7月 膠芽腫に対する第II相医師主導治験の中間解析において、
●膠芽腫:脳腫瘍の一種。最も悪性度が高い。
高い有効性を確認(有効中止)
●悪性胸膜中皮腫:肺を包む胸膜から発生する悪性腫瘍。
2020年12月 悪性神経膠腫に対して薬事承認申請
経口抗がん剤「ティーエスワン®」ホルモン受容体陽性かつHER2陰性で再発高リスクの乳癌
における術後薬物療法の適応追加承認を取得 概要:
研究代表者:京都大学 戸井雅和
開発企業:大鵬薬品工業株式会社
支援拠点:京都大学
支援期間:2011年~
支援内容:拠点は、リエゾン、開発・薬事戦略、スタディマネジ
メント、モニタリング、症例登録、データマネジメント
、統計解析、CRC、治験機器管理について支援
を行った。
成果:
2022年11月
医師主導臨床試験である「エストロゲン受容体陽性HER2陰性乳癌に対す
るTS-1術後療法」の結果より、TS-1と内分泌療法の併用は、再発中間リス
ク以上のエストロゲン受容体陽性かつHER2陰性の原発性乳がん患者さんに
対し、臨床的に意義のある浸潤性疾患のない生存期間(Invasive
Disease Free Survival:iDFS)の延長を認めた。
承認取得
10