よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
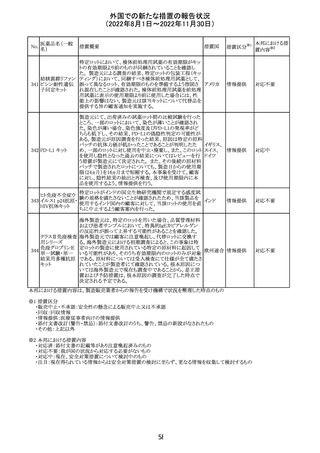
外国での新たな措置の報告状況
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
本邦における措
置内容※2
欧州CMDhは、欧州域各国の添付文書の4.4 Special
warnings and precautions for useおよびSection 4.8.
欧州連合 その他
Undesirable effectsで虚血性心疾患に関する注意喚起をす
る必要があるという、欧州PRACの勧告に同意した。
注目
【第1報】
2022/8/3に欧州EMAが公表したCOVID-19 vaccines
safety updateに、以下の情報が記載された。
〇PRACは、本剤接種後に心筋炎、心膜炎を発現した症例
が報告されていることに基づき、本剤接種後にこれらの事
象が発現する可能性があると結論付けた。 したがって本委
員会は、心筋炎及び心膜炎を新規の副反応として本剤の
欧州添付文書等に記載するとともに、医療従事者及び本
剤接種者に対して注意喚起を行うことを推奨するとした。
2022/8/5、心筋炎、心膜炎を重要な特定されたリスクであ
ると判断し、CCDS及びCore RMP(EU-RMP)も改訂する予
定であるとの情報を入手した。
【第2報】
本剤のCCDSが改訂された。改訂内容は以下の通り。
・Special Warnings and Precautions for Useに「心筋炎及び
心膜炎」を追記し、後述として「本剤を投与後14日以内に心
筋炎及び心膜炎が成人男女で報告されている。ワクチン接
種後の心筋炎及び心膜炎の経過は一般的な経過と変わら
ないことがデータから示唆されている。また、本剤との因果
組換えコロナウイ 関係はデータからは判断できない。ワクチン接種を受けた
アメリカ、
37 ルス(SARS-C 人は、ワクチン接種後に(急性及び持続性の)胸痛、息切れ
その他
オランダ
oV-2)ワクチン 又は動悸などの心筋炎又は心膜炎を示す症状を発症した
場合、直ちに医師の診察を受けてください。本剤3回目接
種後の心筋炎心膜炎のリスクはまだわかっておりません。」
との内容が記載されている。
・Undesirable Effectsに「心筋炎、心膜炎(頻度不明)」を追
記。
・Shelf Life/Storage 及びInstructions for Use/Handlingに
記載されているバイアルに針を刺した後の使用期限が6時
間から12時間に延長。
【第3報】
既報告のPRAC勧告及びCCDS改訂を受け、欧州添付文
書のSpecial warnings and precautionsに心筋炎及び心膜
炎に関する注意が追記された。
【第4報】
米国のFact SheetのWARNING AND PRECAUTIONS項に
おける心筋炎・心膜炎の注意喚起内容が改訂され、CDC
の新型コロナワクチン接種後の心筋炎・心膜炎の中間考察
に関する記載内容のリンクが追記された。また、併せて成人
追加免疫の適応取得に関する臨床試験情報が追記され
た。
注目
オンダンセトロン
36
塩酸塩水和物
7
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
措置区分※1
本邦における措
置内容※2
欧州CMDhは、欧州域各国の添付文書の4.4 Special
warnings and precautions for useおよびSection 4.8.
欧州連合 その他
Undesirable effectsで虚血性心疾患に関する注意喚起をす
る必要があるという、欧州PRACの勧告に同意した。
注目
【第1報】
2022/8/3に欧州EMAが公表したCOVID-19 vaccines
safety updateに、以下の情報が記載された。
〇PRACは、本剤接種後に心筋炎、心膜炎を発現した症例
が報告されていることに基づき、本剤接種後にこれらの事
象が発現する可能性があると結論付けた。 したがって本委
員会は、心筋炎及び心膜炎を新規の副反応として本剤の
欧州添付文書等に記載するとともに、医療従事者及び本
剤接種者に対して注意喚起を行うことを推奨するとした。
2022/8/5、心筋炎、心膜炎を重要な特定されたリスクであ
ると判断し、CCDS及びCore RMP(EU-RMP)も改訂する予
定であるとの情報を入手した。
【第2報】
本剤のCCDSが改訂された。改訂内容は以下の通り。
・Special Warnings and Precautions for Useに「心筋炎及び
心膜炎」を追記し、後述として「本剤を投与後14日以内に心
筋炎及び心膜炎が成人男女で報告されている。ワクチン接
種後の心筋炎及び心膜炎の経過は一般的な経過と変わら
ないことがデータから示唆されている。また、本剤との因果
組換えコロナウイ 関係はデータからは判断できない。ワクチン接種を受けた
アメリカ、
37 ルス(SARS-C 人は、ワクチン接種後に(急性及び持続性の)胸痛、息切れ
その他
オランダ
oV-2)ワクチン 又は動悸などの心筋炎又は心膜炎を示す症状を発症した
場合、直ちに医師の診察を受けてください。本剤3回目接
種後の心筋炎心膜炎のリスクはまだわかっておりません。」
との内容が記載されている。
・Undesirable Effectsに「心筋炎、心膜炎(頻度不明)」を追
記。
・Shelf Life/Storage 及びInstructions for Use/Handlingに
記載されているバイアルに針を刺した後の使用期限が6時
間から12時間に延長。
【第3報】
既報告のPRAC勧告及びCCDS改訂を受け、欧州添付文
書のSpecial warnings and precautionsに心筋炎及び心膜
炎に関する注意が追記された。
【第4報】
米国のFact SheetのWARNING AND PRECAUTIONS項に
おける心筋炎・心膜炎の注意喚起内容が改訂され、CDC
の新型コロナワクチン接種後の心筋炎・心膜炎の中間考察
に関する記載内容のリンクが追記された。また、併せて成人
追加免疫の適応取得に関する臨床試験情報が追記され
た。
注目
オンダンセトロン
36
塩酸塩水和物
7