よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況 (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31510.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和4年度第4回 3/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
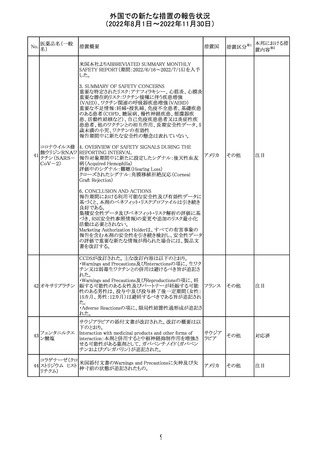
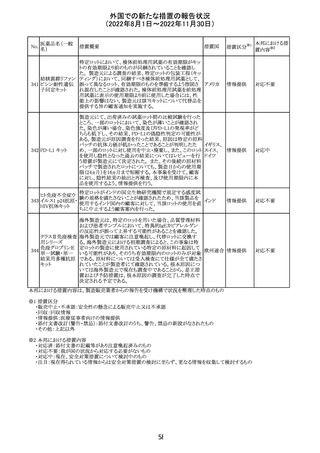
外国での新たな措置の報告状況
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
カナダにおいて、Apotex Inc.のアシクロビル錠(力価200mg
および800mg)の特定ロットについて、許容レベルを超える カナダ
ニトロソアミン不純物が含まれるとして回収されている。
アイルランドHPRAのHPに、デクスメデトミジンの医療専門
家向けレターが掲載された。概要は以下のとおり。
・SPICE III試験は、機械的人工呼吸を必要とする集中治療
室の重症成人患者3,904名を対象にデクスメデトミジンによ
る鎮静の影響を標準治療の影響と比較した無作為化臨床
試験である。
・デクスメデトミジン治療群と標準治療群の90日全死因死亡
率に差は認められなかった。
デクスメデトミジン ・患者のうち、65歳以下の年齢層ではデクスメデトミジン群 アイルラ
2
塩酸塩
は標準治療群より死亡リスクが高い結果であったが、機序 ンド
は不明。
・65歳以下の患者の死亡率に対する影響は、術後ケア以
外の理由で入院した患者投与したケースで最も顕著に現
れ、APACHEⅡスコアの増加とともに増大した。
・若年患者においては、臨床的有用性を他の鎮静剤と比較
検討すべきである。
・添付文書に65歳以下のICU患者の死亡率増加に関する
記載が追記される予定である。
1 アシクロビル
英国MHRAはhameln pharma ltd,社製のアミオダロン塩酸
アミオダロン塩酸 塩濃縮液50mg/mlの1ロットで再検査中に溶液内の目視可
3
イギリス
塩
能な結晶粒子の増加が確認されたため、予防措置としてク
ラス2の自主回収されたことを公表した。
4 オラパリブ
治験責任医師宛に情報が発出された。主な内容は以下の
とおり。
・一次導入療法後に進行が認められていない切除不能又
は転移性結腸・直腸癌患者を対象としたオラパリブ単独投
与又はベバシズマブとの併用投与の有効性及び安全性を
標準治療(ベバシズマブ+フッ化ピリミジン系製剤)と比較し
アメリカ
て評価する第Ⅲ相無作為化非盲検試験の無増悪生存期
間の中間解析について、標準治療群に対するオラパリブ単
独投与及びオラパリブとベバシズマブ併用投与での有効性
が、独立した外部データモニタリング委員会による無益性
の基準を満たしていると判断されたため、両投与群が中止
されることが決定された。
本剤の企業中核データシートが改訂された。主な改訂内容
は下記のとおり。
・Special warnings and precautionsに新生物、脊柱側弯症、
ソムアトロゴン(遺
5
骨端閉鎖、プラダー・ウィリ症候群、筋炎関連の注意内容が アメリカ
伝子組換え)
追加された。
・Undesirable effectsに小児成長ホルモン分泌不全性低身
長症患者で報告された副作用が追記された。
令和5年3月2日
令和4年度第4回
医薬品等安全対策部会
資料3-3
措置区分※1
本邦における措
置内容※2
回収
対応不要
情報提供
対応中
回収
対応不要
情報提供
対応不要
その他
注目
ニュージーランドMedsafeは、オピオイド系医薬品につい
て、乱用、誤用、依存のリスクについての表示変更を提案、
意見を求めていたが、今回回答とLabel Statements
トラマドール塩酸
ニュー
Databaseに追記される内容が示された。
6 塩・アセトアミノ
ジーラン その他
Label Statements Databaseには、この薬は依存や過量投
フェン配合剤
ド
与のリスクがある旨が追記される予定で、麻酔薬、術後の産
科鎮痛、オピオイド依存のみに処方される医薬品は対象か
ら除外される。
7 アシクロビル
シンガポールにおいて、アシクロビル800mg錠の特定ロット
シンガ
について、許容レベルを超えるニトロソアミン不純物が含ま
ポール
れるとして回収されている。
EU添付文書が改訂され、4.4 Special warnings and
8 ロキサデュスタット precautions for use及び4.8 Undesirable effects に続発性
甲状腺機能低下症が追記された。
1
回収
欧州連合 その他
対応不要
対応不要
対応済
(2022年8月1日~2022年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
カナダにおいて、Apotex Inc.のアシクロビル錠(力価200mg
および800mg)の特定ロットについて、許容レベルを超える カナダ
ニトロソアミン不純物が含まれるとして回収されている。
アイルランドHPRAのHPに、デクスメデトミジンの医療専門
家向けレターが掲載された。概要は以下のとおり。
・SPICE III試験は、機械的人工呼吸を必要とする集中治療
室の重症成人患者3,904名を対象にデクスメデトミジンによ
る鎮静の影響を標準治療の影響と比較した無作為化臨床
試験である。
・デクスメデトミジン治療群と標準治療群の90日全死因死亡
率に差は認められなかった。
デクスメデトミジン ・患者のうち、65歳以下の年齢層ではデクスメデトミジン群 アイルラ
2
塩酸塩
は標準治療群より死亡リスクが高い結果であったが、機序 ンド
は不明。
・65歳以下の患者の死亡率に対する影響は、術後ケア以
外の理由で入院した患者投与したケースで最も顕著に現
れ、APACHEⅡスコアの増加とともに増大した。
・若年患者においては、臨床的有用性を他の鎮静剤と比較
検討すべきである。
・添付文書に65歳以下のICU患者の死亡率増加に関する
記載が追記される予定である。
1 アシクロビル
英国MHRAはhameln pharma ltd,社製のアミオダロン塩酸
アミオダロン塩酸 塩濃縮液50mg/mlの1ロットで再検査中に溶液内の目視可
3
イギリス
塩
能な結晶粒子の増加が確認されたため、予防措置としてク
ラス2の自主回収されたことを公表した。
4 オラパリブ
治験責任医師宛に情報が発出された。主な内容は以下の
とおり。
・一次導入療法後に進行が認められていない切除不能又
は転移性結腸・直腸癌患者を対象としたオラパリブ単独投
与又はベバシズマブとの併用投与の有効性及び安全性を
標準治療(ベバシズマブ+フッ化ピリミジン系製剤)と比較し
アメリカ
て評価する第Ⅲ相無作為化非盲検試験の無増悪生存期
間の中間解析について、標準治療群に対するオラパリブ単
独投与及びオラパリブとベバシズマブ併用投与での有効性
が、独立した外部データモニタリング委員会による無益性
の基準を満たしていると判断されたため、両投与群が中止
されることが決定された。
本剤の企業中核データシートが改訂された。主な改訂内容
は下記のとおり。
・Special warnings and precautionsに新生物、脊柱側弯症、
ソムアトロゴン(遺
5
骨端閉鎖、プラダー・ウィリ症候群、筋炎関連の注意内容が アメリカ
伝子組換え)
追加された。
・Undesirable effectsに小児成長ホルモン分泌不全性低身
長症患者で報告された副作用が追記された。
令和5年3月2日
令和4年度第4回
医薬品等安全対策部会
資料3-3
措置区分※1
本邦における措
置内容※2
回収
対応不要
情報提供
対応中
回収
対応不要
情報提供
対応不要
その他
注目
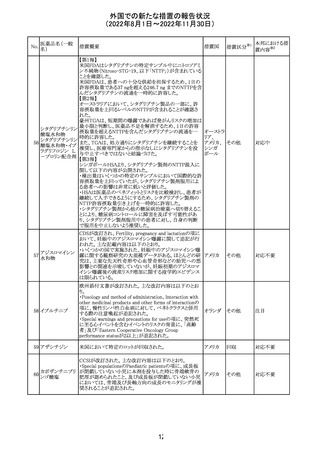
ニュージーランドMedsafeは、オピオイド系医薬品につい
て、乱用、誤用、依存のリスクについての表示変更を提案、
意見を求めていたが、今回回答とLabel Statements
トラマドール塩酸
ニュー
Databaseに追記される内容が示された。
6 塩・アセトアミノ
ジーラン その他
Label Statements Databaseには、この薬は依存や過量投
フェン配合剤
ド
与のリスクがある旨が追記される予定で、麻酔薬、術後の産
科鎮痛、オピオイド依存のみに処方される医薬品は対象か
ら除外される。
7 アシクロビル
シンガポールにおいて、アシクロビル800mg錠の特定ロット
シンガ
について、許容レベルを超えるニトロソアミン不純物が含ま
ポール
れるとして回収されている。
EU添付文書が改訂され、4.4 Special warnings and
8 ロキサデュスタット precautions for use及び4.8 Undesirable effects に続発性
甲状腺機能低下症が追記された。
1
回収
欧州連合 その他
対応不要
対応不要
対応済