よむ、つかう、まなぶ。
参考資料2 調査結果報告書 (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31125.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第25回 2/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
本剤の発売開始以降における本剤及び本剤の後発医薬品投与後の乳酸アシドーシスの報告
における禁忌患者 6への投与状況を調査した。
再審査期間と直近における禁忌患者への投与状況を比較するため、主に、表 4 に示す 3 つ
の期間において、本剤及び本剤の後発医薬品の乳酸アシドーシスの報告例数、及び乳酸アシ
ドーシスの報告例における禁忌患者への投与例数を調査した。
(1)
(2)
(3)
表 4. 乳酸アシドーシスの発現状況の確認期間
対象期間(当局報告受付日)
備考
2010 年 5 月 10 日~2014 年 1 月 19 日
(約 3 年 7 カ月) 本剤の販売開始以降、再審査期間中
本剤の再審査期間終了以降、禁忌事
2014 年 1 月 20 日~2019 年 6 月 17 日
(約 4 年 6 カ月)
項に係る添付文書改訂まで
2019 年 6 月 18 日~2022 年 11 月 30 日
(約 3 年 5 カ月) 禁忌事項に係る添付文書改訂以降
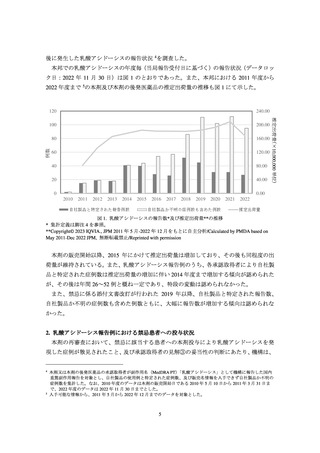
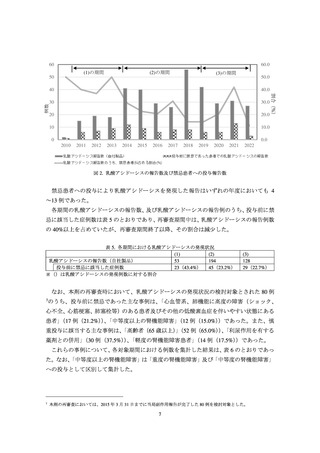
年度毎(当局報告受付日に基づく)の乳酸アシドーシス報告例数(自社製品と特定された
例数)、及び報告例のうち投与前に禁忌に該当する患者の報告数推移は図 2 のとおりであっ
た。
6
乳酸アシドーシスの懸念が禁忌理由である、以下の項目のいずれかに該当する患者
項目
定義
乳酸アシドーシス発現前に eGFR が 30 mL/min/1.73m2 未満の症例又は
重度の腎機能障害患者又は透析患者
透析(腹膜透析を含む)を要する症例
重度の肝機能障害患者
肝硬変(アルコール肝硬変を含む)を合併する症例
以下のいずれかに該当する症例
心血管系、肺機能に高度の障害(ショック、
・心不全、慢性心不全、又はうっ血性心不全を合併する症例
心不全、心筋梗塞、肺塞栓等)のある患者
・乳酸アシドーシス発現以前に以下のいずれかを合併する症例:慢性
及びその他の低酸素血症を伴いやすい状態
閉塞性肺疾患、間質性肺炎、肺気腫合併肺線維症、慢性気管支炎、肺
にある患者
炎後遺症、睡眠時無呼吸症候群
以下のいずれかに該当する症例
脱水症の患者又は脱水状態が懸念される患 ・脱水により入院した症例
者(下痢、嘔吐等の胃腸障害のある患者、 ・熱中症(炎天下/高温下の作業、ゴルフ)があった症例
経口摂取が困難な患者等)
・下痢の持続が認められた症例
・非経口摂取(胃ろう等)の症例
以下のいずれかに該当する症例
・敗血症及びショックを合併する症例
重症感染症、手術前後、重篤な外傷のある
・
(緊急手術を除く)術前投与症例(手術前日に中止された症例を含む)、
患者
及び術後投与再開後に乳酸アシドーシスを発現した症例
・乳酸アシドーシス発現前に重篤な外傷がある症例
過度のアルコール摂取者
アルコール依存症又はアルコール中毒の症例
6
における禁忌患者 6への投与状況を調査した。
再審査期間と直近における禁忌患者への投与状況を比較するため、主に、表 4 に示す 3 つ
の期間において、本剤及び本剤の後発医薬品の乳酸アシドーシスの報告例数、及び乳酸アシ
ドーシスの報告例における禁忌患者への投与例数を調査した。
(1)
(2)
(3)
表 4. 乳酸アシドーシスの発現状況の確認期間
対象期間(当局報告受付日)
備考
2010 年 5 月 10 日~2014 年 1 月 19 日
(約 3 年 7 カ月) 本剤の販売開始以降、再審査期間中
本剤の再審査期間終了以降、禁忌事
2014 年 1 月 20 日~2019 年 6 月 17 日
(約 4 年 6 カ月)
項に係る添付文書改訂まで
2019 年 6 月 18 日~2022 年 11 月 30 日
(約 3 年 5 カ月) 禁忌事項に係る添付文書改訂以降
年度毎(当局報告受付日に基づく)の乳酸アシドーシス報告例数(自社製品と特定された
例数)、及び報告例のうち投与前に禁忌に該当する患者の報告数推移は図 2 のとおりであっ
た。
6
乳酸アシドーシスの懸念が禁忌理由である、以下の項目のいずれかに該当する患者
項目
定義
乳酸アシドーシス発現前に eGFR が 30 mL/min/1.73m2 未満の症例又は
重度の腎機能障害患者又は透析患者
透析(腹膜透析を含む)を要する症例
重度の肝機能障害患者
肝硬変(アルコール肝硬変を含む)を合併する症例
以下のいずれかに該当する症例
心血管系、肺機能に高度の障害(ショック、
・心不全、慢性心不全、又はうっ血性心不全を合併する症例
心不全、心筋梗塞、肺塞栓等)のある患者
・乳酸アシドーシス発現以前に以下のいずれかを合併する症例:慢性
及びその他の低酸素血症を伴いやすい状態
閉塞性肺疾患、間質性肺炎、肺気腫合併肺線維症、慢性気管支炎、肺
にある患者
炎後遺症、睡眠時無呼吸症候群
以下のいずれかに該当する症例
脱水症の患者又は脱水状態が懸念される患 ・脱水により入院した症例
者(下痢、嘔吐等の胃腸障害のある患者、 ・熱中症(炎天下/高温下の作業、ゴルフ)があった症例
経口摂取が困難な患者等)
・下痢の持続が認められた症例
・非経口摂取(胃ろう等)の症例
以下のいずれかに該当する症例
・敗血症及びショックを合併する症例
重症感染症、手術前後、重篤な外傷のある
・
(緊急手術を除く)術前投与症例(手術前日に中止された症例を含む)、
患者
及び術後投与再開後に乳酸アシドーシスを発現した症例
・乳酸アシドーシス発現前に重篤な外傷がある症例
過度のアルコール摂取者
アルコール依存症又はアルコール中毒の症例
6