よむ、つかう、まなぶ。
総-10再生医療等製品の医療保険上の取扱いについて(エドスチラドリン) (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_73124.html |
| 出典情報 | 中央社会保険医療協議会 総会(第650回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
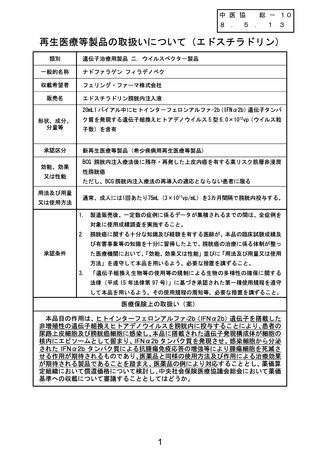
製品概要
販売名
エドスチラドリン膀胱内注入液
使用目的
本品は、ヒトインターフェロンアルファ-2b(IFNα2b)遺伝子を搭載した非増殖性の
遺伝子組換えヒトアデノウイルスを主成分とする再生医療等製品である。
膀胱内に投与された本品が患者の尿路上皮細胞及び膀胱癌細胞に感染することによ
り、本品に搭載された遺伝子発現構成体が細胞の核内にエピソームとして留まり、
IFNα2b タンパク質を発現させ、感染細胞から分泌された IFNα2b タンパク質による抗腫
瘍免疫応答の増強等により腫瘍細胞を死滅させる作用が期待される。
主な使用方法
【用法及び用量又は使用方法】
通常、成人には 1 回あたり 75mL(3×1011vp/mL)を 3 カ月間隔で膀胱内投与する。
本品は BCG-unresponsive(注 1)で高リスクの筋層非浸潤性膀胱癌(NMIBC)患者に対し
て、非盲検非対照試験として海外第Ⅲ相試験である rAd-IFN-CS-003 試験、並びに非盲検非
対照試験として国内第Ⅲ相試験である 000381 試験が実施された。
rAd-IFN-CS-003 試験においては、主要評価項目である、上皮内癌(CIS)併発ありコ
ホートにおける本品の初回投与後 3 カ月までの完全奏効率 (注 2)[95%CI](%)は 53.4
[43.3, 63.3](55/103 例)であり、95%CI の下限が事前に規定した閾値 27%を上回った。
主な有用性
000381 試験においては、主要評価項目である、CIS 併発ありコホートにおける本品の初
回投与後 3 カ月までの完全奏効率[95%CI](%)は 75.0[50.9, 91.3](15/20 例)であ
り、95%CI の下限が事前に規定した閾値 2%を上回った。
(注 1)BCG-refractory(BCG 導入療法後 3 ヵ月の時点で再発または腫瘍が残存し 6 ヵ月時
点(BCG 維持療法を含む)でも消失しない)と早期の BCG-relapsing(BCG 最終投与から
12 ヵ月以内の再発)の総称であり、十分な BCG 膀胱内注入療法を行ったにもかかわらず
再発し、BCG 膀胱内注入療法再導入が無効と考えられる疾患群と定義される。
(注 2)実施医療機関(rAd-IFN-CS-003 試験)もしくは中央病理診断施設(000381 試験)
における尿細胞診及び膀胱鏡検査、必要に応じて生検によって評価し、「①尿細胞診で
陰性であり、膀胱鏡検査で正常所見、又は所見がある場合は低グレード病変であり、高
グレード病変の再発が認められない。」、「②生検を行った場合、低グレード病変、高
グレード病変の再発が認められない。」のいずれかの基準を満たす場合と定義された。
2
販売名
エドスチラドリン膀胱内注入液
使用目的
本品は、ヒトインターフェロンアルファ-2b(IFNα2b)遺伝子を搭載した非増殖性の
遺伝子組換えヒトアデノウイルスを主成分とする再生医療等製品である。
膀胱内に投与された本品が患者の尿路上皮細胞及び膀胱癌細胞に感染することによ
り、本品に搭載された遺伝子発現構成体が細胞の核内にエピソームとして留まり、
IFNα2b タンパク質を発現させ、感染細胞から分泌された IFNα2b タンパク質による抗腫
瘍免疫応答の増強等により腫瘍細胞を死滅させる作用が期待される。
主な使用方法
【用法及び用量又は使用方法】
通常、成人には 1 回あたり 75mL(3×1011vp/mL)を 3 カ月間隔で膀胱内投与する。
本品は BCG-unresponsive(注 1)で高リスクの筋層非浸潤性膀胱癌(NMIBC)患者に対し
て、非盲検非対照試験として海外第Ⅲ相試験である rAd-IFN-CS-003 試験、並びに非盲検非
対照試験として国内第Ⅲ相試験である 000381 試験が実施された。
rAd-IFN-CS-003 試験においては、主要評価項目である、上皮内癌(CIS)併発ありコ
ホートにおける本品の初回投与後 3 カ月までの完全奏効率 (注 2)[95%CI](%)は 53.4
[43.3, 63.3](55/103 例)であり、95%CI の下限が事前に規定した閾値 27%を上回った。
主な有用性
000381 試験においては、主要評価項目である、CIS 併発ありコホートにおける本品の初
回投与後 3 カ月までの完全奏効率[95%CI](%)は 75.0[50.9, 91.3](15/20 例)であ
り、95%CI の下限が事前に規定した閾値 2%を上回った。
(注 1)BCG-refractory(BCG 導入療法後 3 ヵ月の時点で再発または腫瘍が残存し 6 ヵ月時
点(BCG 維持療法を含む)でも消失しない)と早期の BCG-relapsing(BCG 最終投与から
12 ヵ月以内の再発)の総称であり、十分な BCG 膀胱内注入療法を行ったにもかかわらず
再発し、BCG 膀胱内注入療法再導入が無効と考えられる疾患群と定義される。
(注 2)実施医療機関(rAd-IFN-CS-003 試験)もしくは中央病理診断施設(000381 試験)
における尿細胞診及び膀胱鏡検査、必要に応じて生検によって評価し、「①尿細胞診で
陰性であり、膀胱鏡検査で正常所見、又は所見がある場合は低グレード病変であり、高
グレード病変の再発が認められない。」、「②生検を行った場合、低グレード病変、高
グレード病変の再発が認められない。」のいずれかの基準を満たす場合と定義された。
2