よむ、つかう、まなぶ。
参考資料1-3 (資料1-3関係)リスク区分変更検討手順(案)[296KB] (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70725.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第4回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和8年3月6日令和7年度第4回医薬品等安全対策部会
参考資料1-3(資料1-3関係)
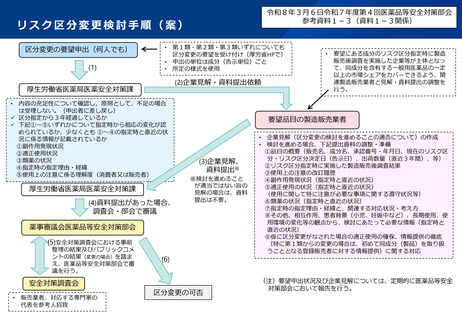
リスク区分変更検討手順(案)
区分変更の要望申出(何人でも)
(1)
•
•
•
第1類・第2類・第3類いずれについても
区分変更の要望を受け付け(厚労省HPで)
申出の単位は成分(告示単位)ごと
所定の様式を使用
(2)企業見解・資料提出依頼
厚生労働省医薬局医薬安全対策課
内容の充足性について確認し、原則として、不足の場合
は受理しない。(申出者に差し戻し)
✓ 区分指定から3年経過しているか
✓ 下記①~⑤いずれかについて指定時から相応の変化が認
められているか、少なくとも ①~④の指定時と直近の状
況に係る情報が記載されているか
①副作用発現状況
②適正使用状況
③類薬の状況
④指定時の指定理由・経緯
⑤使用上の注意に係る理解度(消費者又は販売者)
•
要望にある成分のリスク区分指定時に製造
販売後調査を実施した企業等が主体となっ
て、同成分を含有する一般用医薬品の一定
以上の市場シェアをカバーできるよう、関
連製造販売業者と見解・資料提出の調整を
行う。
•
厚生労働省医薬局医薬安全対策課
(4)資料提出があった場合、
調査会・部会で審議
要望品目の製造販売業者
•
•
(3)企業見解、
資料提出※
※検討を進めること
が適当ではない旨の
見解の場合は、資料
提出は不要。
薬事審議会医薬品等安全対策部会
(5)安全対策調査会における事前
整理の結果及びパブリックコメ
ントの結果(変更の場合)を踏ま
え、医薬品等安全対策部会で審
議を行う。
(6)
安全対策調査会
•
販売業者、対応する専門家の
代表を参考人招致
区分変更の可否
企業見解(区分変更の検討を進めることの適否について)の作成
検討を進める場合、下記提出資料の調整・準備
①品目の概要(販売名、成分名、承認番号・年月日、現在のリスク区
分・リスク区分決定日(告示日)、出荷数量(直近3年間)、等)
②リスク区分指定時に実施した製造販売後調査結果
③使用上の注意の改訂履歴
④副作用発現状況(指定時と直近の状況)
⑤適正使用の状況(指定時と直近の状況)
(使用に関して特に注意が必要な事項に関する遵守状況等)
⑥類薬の状況(指定時と直近の状況)
⑦指定時の指定理由・経緯と、関連する対応状況・考え方
⑧その他、相互作用、患者背景(小児、妊娠中など)、長期使用、使
用環境の変化等の観点から、検討にあたって必要な情報(指定時と
直近の状況)
⑨仮に区分変更がなされた場合の適正使用の確保、情報提供の徹底
(特に第1類からの変更の場合は、初めて同成分(製品)を取り扱
うこととなる登録販売者に対する情報提供)に関する対応
(注)要望申出状況及び企業見解については、定期的に医薬品等安全
対策部会において報告を行う。
参考資料1-3(資料1-3関係)
リスク区分変更検討手順(案)
区分変更の要望申出(何人でも)
(1)
•
•
•
第1類・第2類・第3類いずれについても
区分変更の要望を受け付け(厚労省HPで)
申出の単位は成分(告示単位)ごと
所定の様式を使用
(2)企業見解・資料提出依頼
厚生労働省医薬局医薬安全対策課
内容の充足性について確認し、原則として、不足の場合
は受理しない。(申出者に差し戻し)
✓ 区分指定から3年経過しているか
✓ 下記①~⑤いずれかについて指定時から相応の変化が認
められているか、少なくとも ①~④の指定時と直近の状
況に係る情報が記載されているか
①副作用発現状況
②適正使用状況
③類薬の状況
④指定時の指定理由・経緯
⑤使用上の注意に係る理解度(消費者又は販売者)
•
要望にある成分のリスク区分指定時に製造
販売後調査を実施した企業等が主体となっ
て、同成分を含有する一般用医薬品の一定
以上の市場シェアをカバーできるよう、関
連製造販売業者と見解・資料提出の調整を
行う。
•
厚生労働省医薬局医薬安全対策課
(4)資料提出があった場合、
調査会・部会で審議
要望品目の製造販売業者
•
•
(3)企業見解、
資料提出※
※検討を進めること
が適当ではない旨の
見解の場合は、資料
提出は不要。
薬事審議会医薬品等安全対策部会
(5)安全対策調査会における事前
整理の結果及びパブリックコメ
ントの結果(変更の場合)を踏ま
え、医薬品等安全対策部会で審
議を行う。
(6)
安全対策調査会
•
販売業者、対応する専門家の
代表を参考人招致
区分変更の可否
企業見解(区分変更の検討を進めることの適否について)の作成
検討を進める場合、下記提出資料の調整・準備
①品目の概要(販売名、成分名、承認番号・年月日、現在のリスク区
分・リスク区分決定日(告示日)、出荷数量(直近3年間)、等)
②リスク区分指定時に実施した製造販売後調査結果
③使用上の注意の改訂履歴
④副作用発現状況(指定時と直近の状況)
⑤適正使用の状況(指定時と直近の状況)
(使用に関して特に注意が必要な事項に関する遵守状況等)
⑥類薬の状況(指定時と直近の状況)
⑦指定時の指定理由・経緯と、関連する対応状況・考え方
⑧その他、相互作用、患者背景(小児、妊娠中など)、長期使用、使
用環境の変化等の観点から、検討にあたって必要な情報(指定時と
直近の状況)
⑨仮に区分変更がなされた場合の適正使用の確保、情報提供の徹底
(特に第1類からの変更の場合は、初めて同成分(製品)を取り扱
うこととなる登録販売者に対する情報提供)に関する対応
(注)要望申出状況及び企業見解については、定期的に医薬品等安全
対策部会において報告を行う。