よむ、つかう、まなぶ。
資料1-4 新型コロナワクチンの副反応疑い報告状況について[595KB] (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/newpage_00170.html |
| 出典情報 | 厚生科学審議会・薬事審議会(合同開催) 予防接種・ワクチン分科会副反応検討部会(第110回 2/4)医薬品等安全対策部会安全対策調査会(令和7年度第11回 2/4)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
新型コロナワクチンの副反応疑い報告状況について
第110回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和7年
度第11回薬事審議会医薬品等安全対策部会安全対策調査会(合同開催)
2026(令和8)年2月4日
○
資料
1ー4
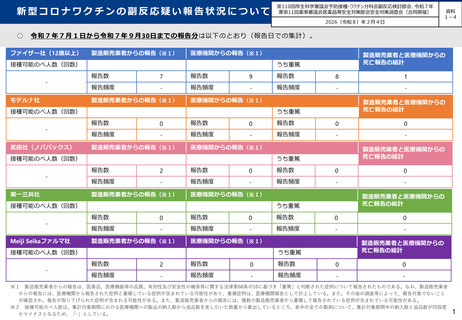
令和7年7月1日から令和7年9月30日までの報告分は以下のとおり(報告日での集計)。
ファイザー社(12歳以上)
製造販売業者からの報告(※1)
医療機関からの報告(※1)
接種可能のべ人数(回数)
-
モデルナ社
うち重篤
報告数
7
報告数
9
報告数
8
1
報告頻度
-
報告頻度
-
報告頻度
-
-
製造販売業者からの報告(※1)
医療機関からの報告(※1)
接種可能のべ人数(回数)
武田社(ノババックス)
第一三共社
報告数
0
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
製造販売業者からの報告(※1)
医療機関からの報告(※1)
報告数
2
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
医療機関からの報告(※1)
接種可能のべ人数(回数)
Meiji Seikaファルマ社
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
報告数
0
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
製造販売業者からの報告(※1)
医療機関からの報告(※1)
接種可能のべ人数(回数)
-
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
製造販売業者からの報告(※1)
-
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
接種可能のべ人数(回数)
-
製造販売業者と医療機関からの
死亡報告の総計
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
報告数
2
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
※1 製造販売業者からの報告は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第68条の10に基づき「重篤」と判断された症例について報告されたものである。なお、製造販売業者
からの報告には、医療機関から報告された症例と重複している症例が含まれている可能性があり、重複症例は、医療機関報告として計上している。また、その後の調査等によって、報告対象でないこと
が確認され、報告が取り下げられた症例が含まれる可能性がある。また、製造販売業者からの報告には、複数の製造販売業者から重複して報告されている症例が含まれている可能性がある。
※2 接種可能のべ人数は、集計対象期間における医療機関への製品の納入数から返品数を差し引いた数量から算出しているところ、表中の全ての製剤について、集計対象期間中の納入数と返品数が同程度
かマイナスとなるため、「ー」としている。
1
第110回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和7年
度第11回薬事審議会医薬品等安全対策部会安全対策調査会(合同開催)
2026(令和8)年2月4日
○
資料
1ー4
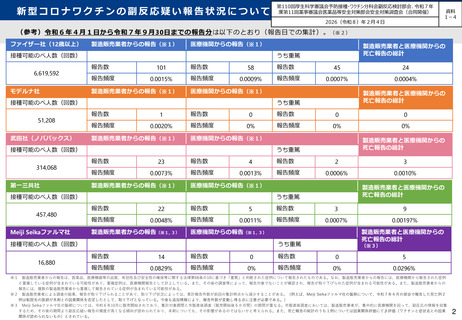
令和7年7月1日から令和7年9月30日までの報告分は以下のとおり(報告日での集計)。
ファイザー社(12歳以上)
製造販売業者からの報告(※1)
医療機関からの報告(※1)
接種可能のべ人数(回数)
-
モデルナ社
うち重篤
報告数
7
報告数
9
報告数
8
1
報告頻度
-
報告頻度
-
報告頻度
-
-
製造販売業者からの報告(※1)
医療機関からの報告(※1)
接種可能のべ人数(回数)
武田社(ノババックス)
第一三共社
報告数
0
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
製造販売業者からの報告(※1)
医療機関からの報告(※1)
報告数
2
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
医療機関からの報告(※1)
接種可能のべ人数(回数)
Meiji Seikaファルマ社
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
報告数
0
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
製造販売業者からの報告(※1)
医療機関からの報告(※1)
接種可能のべ人数(回数)
-
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
製造販売業者からの報告(※1)
-
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
接種可能のべ人数(回数)
-
製造販売業者と医療機関からの
死亡報告の総計
製造販売業者と医療機関からの
死亡報告の総計
うち重篤
報告数
2
報告数
0
報告数
0
0
報告頻度
-
報告頻度
-
報告頻度
-
-
※1 製造販売業者からの報告は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第68条の10に基づき「重篤」と判断された症例について報告されたものである。なお、製造販売業者
からの報告には、医療機関から報告された症例と重複している症例が含まれている可能性があり、重複症例は、医療機関報告として計上している。また、その後の調査等によって、報告対象でないこと
が確認され、報告が取り下げられた症例が含まれる可能性がある。また、製造販売業者からの報告には、複数の製造販売業者から重複して報告されている症例が含まれている可能性がある。
※2 接種可能のべ人数は、集計対象期間における医療機関への製品の納入数から返品数を差し引いた数量から算出しているところ、表中の全ての製剤について、集計対象期間中の納入数と返品数が同程度
かマイナスとなるため、「ー」としている。
1