よむ、つかう、まなぶ。
総-1再生医療等製品の医療保険上の取扱いについて (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62391.html |
| 出典情報 | 中央社会保険医療協議会 総会(第615回 8/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
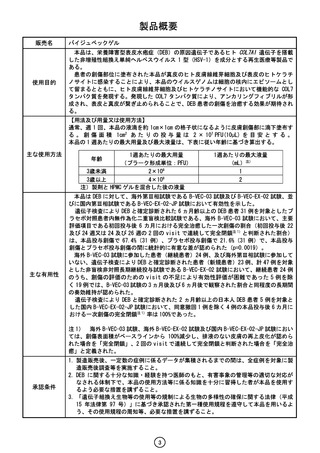
製品概要
販売名
バイジュベックゲル
使用目的
本品は、栄養障害型表皮水疱症(DEB)の原因遺伝子であるヒト COL7A1 遺伝子を搭載
した非増殖性組換え単純ヘルペスウイルス 1 型(HSV-1)を成分とする再生医療等製品で
ある。
患者の創傷部位に塗布された本品が真皮のヒト皮膚線維芽細胞及び表皮のヒトケラチ
ノサイトに感染することにより、本品のウイルスゲノムは細胞の核内にエピソームとし
て留まるとともに、ヒト皮膚線維芽細胞及びヒトケラチノサイトにおいて機能的な COL7
タンパク質を発現する。発現した COL7 タンパク質により、アンカリングフィブリルが形
成され、表皮と真皮が繋ぎ止められることで、DEB 患者の創傷を治癒する効果が期待され
る。
【用法及び用量又は使用方法】
通常、週 1 回、本品の液滴を約 1cm×1cm の格子状になるように皮膚創傷部に滴下塗布す
る 。 創 傷 面 積 1cm2 あ た り の 投 与 量 は 2 × 107 PFU(10µL) を 目 安 と す る 。
本品の 1 週あたりの最大用量及び最大液量は、下表に従い年齢に基づき算出する。
主な使用方法
主な有用性
1週あたりの最大用量
(プラーク形成単位:PFU)
3歳未満
2×109
3歳以上
4×109
注)製剤と HPMC ゲルを混合した後の液量
年齢
1週あたりの最大液量
(mL)注)
1
2
本品は DEB に対して、海外第Ⅲ相試験である B-VEC-03 試験及び B-VEC-EX-02 試験、並
びに国内第Ⅲ相試験である B-VEC-EX-02-JP 試験において有効性を示した。
遺伝子検査により DEB と確定診断された 6 ヵ月齢以上の DEB 患者 31 例を対象としたプ
ラセボ対照患者内無作為化二重盲検比較試験である、海外 B-VEC-03 試験において、主要
評価項目である初回投与後 6 カ月における完全治癒した一次創傷の割合(初回投与後 22
及び 24 週又は 24 及び 26 週の 2 回の visit で連続して完全閉鎖注 1)と判断された割合)
は、本品投与創傷で 67.4%(31 例)、プラセボ投与創傷で 21.6%(31 例)で、本品投与
創傷とプラセボ投与創傷の間に統計的に有意な差が認められた(p=0.0019)。
海外 B-VEC-03 試験に参加した患者(継続患者)24 例、及び海外第Ⅲ相試験に参加して
いない、遺伝子検査により DEB と確定診断された患者(新規患者)23 例、計 47 例を対象
とした非盲検非対照長期継続投与試験である B-VEC-EX-02 試験において、継続患者 24 例
のうち、創傷の評価のための visit の不足により有効性評価が困難であった 5 例を除
く 19 例では、B-VEC-03 試験の 3 ヵ月後及び 6 ヵ月後で観察された割合と同程度の長期間
の奏効維持が認められた。
遺伝子検査により DEB と確定診断された 2 ヵ月齢以上の日本人 DEB 患者 5 例を対象と
した国内 B-VEC-EX-02-JP 試験において、同意撤回 1 例を除く 4 例の本品投与後 6 カ月に
おける一次創傷の完全閉鎖注 1)率は 100%であった。
注 1) 海外 B-VEC-03 試験、海外 B-VEC-EX-02 試験及び国内 B-VEC-EX-02-JP 試験におい
ては、創傷表面積がベースラインから 100%減少し、排液のない皮膚の再上皮化が認めら
れた場合を「完全閉鎖」、2 回の visit で連続して完全閉鎖と判断された場合を「完全治
癒」と定義された。
承認条件
1. 製造販売後、一定数の症例に係るデータが集積されるまでの間は、全症例を対象に製
造販売後調査等を実施すること。
2. DEB に関する十分な知識・経験を持つ医師のもと、有害事象の管理等の適切な対応が
なされる体制下で、本品の使用方法等に係る知識を十分に習得した者が本品を使用す
るよう必要な措置を講ずること。
3. 「遺伝子組換え生物等の使用等の規制による生物の多様性の確保に関する法律(平成
15 年法律第 97 号)」に基づき承認された第一種使用規程を遵守して本品を用いるよ
う、その使用規程の周知等、必要な措置を講ずること。
3
販売名
バイジュベックゲル
使用目的
本品は、栄養障害型表皮水疱症(DEB)の原因遺伝子であるヒト COL7A1 遺伝子を搭載
した非増殖性組換え単純ヘルペスウイルス 1 型(HSV-1)を成分とする再生医療等製品で
ある。
患者の創傷部位に塗布された本品が真皮のヒト皮膚線維芽細胞及び表皮のヒトケラチ
ノサイトに感染することにより、本品のウイルスゲノムは細胞の核内にエピソームとし
て留まるとともに、ヒト皮膚線維芽細胞及びヒトケラチノサイトにおいて機能的な COL7
タンパク質を発現する。発現した COL7 タンパク質により、アンカリングフィブリルが形
成され、表皮と真皮が繋ぎ止められることで、DEB 患者の創傷を治癒する効果が期待され
る。
【用法及び用量又は使用方法】
通常、週 1 回、本品の液滴を約 1cm×1cm の格子状になるように皮膚創傷部に滴下塗布す
る 。 創 傷 面 積 1cm2 あ た り の 投 与 量 は 2 × 107 PFU(10µL) を 目 安 と す る 。
本品の 1 週あたりの最大用量及び最大液量は、下表に従い年齢に基づき算出する。
主な使用方法
主な有用性
1週あたりの最大用量
(プラーク形成単位:PFU)
3歳未満
2×109
3歳以上
4×109
注)製剤と HPMC ゲルを混合した後の液量
年齢
1週あたりの最大液量
(mL)注)
1
2
本品は DEB に対して、海外第Ⅲ相試験である B-VEC-03 試験及び B-VEC-EX-02 試験、並
びに国内第Ⅲ相試験である B-VEC-EX-02-JP 試験において有効性を示した。
遺伝子検査により DEB と確定診断された 6 ヵ月齢以上の DEB 患者 31 例を対象としたプ
ラセボ対照患者内無作為化二重盲検比較試験である、海外 B-VEC-03 試験において、主要
評価項目である初回投与後 6 カ月における完全治癒した一次創傷の割合(初回投与後 22
及び 24 週又は 24 及び 26 週の 2 回の visit で連続して完全閉鎖注 1)と判断された割合)
は、本品投与創傷で 67.4%(31 例)、プラセボ投与創傷で 21.6%(31 例)で、本品投与
創傷とプラセボ投与創傷の間に統計的に有意な差が認められた(p=0.0019)。
海外 B-VEC-03 試験に参加した患者(継続患者)24 例、及び海外第Ⅲ相試験に参加して
いない、遺伝子検査により DEB と確定診断された患者(新規患者)23 例、計 47 例を対象
とした非盲検非対照長期継続投与試験である B-VEC-EX-02 試験において、継続患者 24 例
のうち、創傷の評価のための visit の不足により有効性評価が困難であった 5 例を除
く 19 例では、B-VEC-03 試験の 3 ヵ月後及び 6 ヵ月後で観察された割合と同程度の長期間
の奏効維持が認められた。
遺伝子検査により DEB と確定診断された 2 ヵ月齢以上の日本人 DEB 患者 5 例を対象と
した国内 B-VEC-EX-02-JP 試験において、同意撤回 1 例を除く 4 例の本品投与後 6 カ月に
おける一次創傷の完全閉鎖注 1)率は 100%であった。
注 1) 海外 B-VEC-03 試験、海外 B-VEC-EX-02 試験及び国内 B-VEC-EX-02-JP 試験におい
ては、創傷表面積がベースラインから 100%減少し、排液のない皮膚の再上皮化が認めら
れた場合を「完全閉鎖」、2 回の visit で連続して完全閉鎖と判断された場合を「完全治
癒」と定義された。
承認条件
1. 製造販売後、一定数の症例に係るデータが集積されるまでの間は、全症例を対象に製
造販売後調査等を実施すること。
2. DEB に関する十分な知識・経験を持つ医師のもと、有害事象の管理等の適切な対応が
なされる体制下で、本品の使用方法等に係る知識を十分に習得した者が本品を使用す
るよう必要な措置を講ずること。
3. 「遺伝子組換え生物等の使用等の規制による生物の多様性の確保に関する法律(平成
15 年法律第 97 号)」に基づき承認された第一種使用規程を遵守して本品を用いるよ
う、その使用規程の周知等、必要な措置を講ずること。
3