よむ、つかう、まなぶ。
「再生医療等の安全性の確保等に関する法律及び臨床研究法の一部を改正する法律」の施行に伴う「遺伝子治療等臨床研究に関する指針」の取扱いについて (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_57618.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第106回 5/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
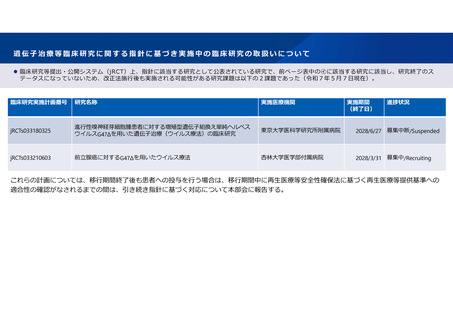
遺伝子治療等臨床研究に関する指針に基づき実施中の臨床研究の取扱いについて
臨床研究等提出・公開システム(jRCT)上、指針に該当する研究として公表されている研究で、前ページ表中の㋑に該当する研究に該当し、研究終了のス
テータスになっていないため、改正法施行後も実施される可能性がある研究課題は以下の2課題であった(令和7年5月7日現在)。
臨床研究実施計画番号
研究名称
実施医療機関
実施期間
(終了日)
進捗状況
jRCTs033180325
進行性嗅神経芽細胞腫患者に対する増殖型遺伝子組換え単純ヘルペス
ウイルスG47Δを用いた遺伝子治療(ウイルス療法)の臨床研究
東京大学医科学研究所附属病院
2028/6/27 募集中断/Suspended
jRCTs033210603
前立腺癌に対するG47Δを用いたウイルス療法
杏林大学医学部付属病院
2028/3/31 募集中/Recruiting
これらの計画については、移行期間終了後も患者への投与を行う場合は、移行期間中に再生医療等安全性確保法に基づく再生医療等提供基準への
適合性の確認がなされるまでの間は、引き続き指針に基づく対応について本部会に報告する。
臨床研究等提出・公開システム(jRCT)上、指針に該当する研究として公表されている研究で、前ページ表中の㋑に該当する研究に該当し、研究終了のス
テータスになっていないため、改正法施行後も実施される可能性がある研究課題は以下の2課題であった(令和7年5月7日現在)。
臨床研究実施計画番号
研究名称
実施医療機関
実施期間
(終了日)
進捗状況
jRCTs033180325
進行性嗅神経芽細胞腫患者に対する増殖型遺伝子組換え単純ヘルペス
ウイルスG47Δを用いた遺伝子治療(ウイルス療法)の臨床研究
東京大学医科学研究所附属病院
2028/6/27 募集中断/Suspended
jRCTs033210603
前立腺癌に対するG47Δを用いたウイルス療法
杏林大学医学部付属病院
2028/3/31 募集中/Recruiting
これらの計画については、移行期間終了後も患者への投与を行う場合は、移行期間中に再生医療等安全性確保法に基づく再生医療等提供基準への
適合性の確認がなされるまでの間は、引き続き指針に基づく対応について本部会に報告する。