よむ、つかう、まなぶ。
【資料1】柏谷構成員提出資料 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38892.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第9回 3/21)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
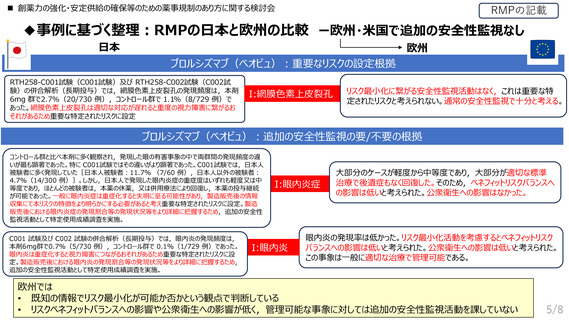
◼ 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会
◆日本の追加の安全性監視に対する業界の通知改訂案
特定されたリスク・潜在的リスクの中からリスクベネフィットバランスへの影
響,公衆衛生への影響等を評価し,重要なリスクを設定する。
重要なリスクでなければ,通常の安全性監視
重要な特定されたリスク・重要な潜在的リスクのうち,リスクベネフィットバ
ランス及び公衆衛生への影響を踏まえ,リスク最小化に寄与する懸念
事項かを明確にし,懸念事項に対して科学的に適切な対処方法を
E2Eの医薬品安全性監視方法から決定する。
重要なリスクであっても,リスクベネフィットバランス
や公衆衛生への影響が低いものや既存の情報
でリスク最小化が実施可能なものは,通常の安
全性監視
• ステップ1では「重要なリスク」かどうかの判断を行
う
• ステップ2では「重要なリスク」の中から,リスクベネ
フィットバランスや公衆衛生への影響,さらに,リ
スク最小化に寄与する懸念事項か否か(既存の
情報でリスク最小化を行えるか否か)を検討し,
追加の安全性監視活動が必要かを判断する
• ステップ3,4は変更しない
このような改訂をすることで,欧米と同様の考え方で
日本の追加の安全性監視が行われていることの理解
が進み,ドラッグロス・ラグの課題の一助となる
8/8
◆日本の追加の安全性監視に対する業界の通知改訂案
特定されたリスク・潜在的リスクの中からリスクベネフィットバランスへの影
響,公衆衛生への影響等を評価し,重要なリスクを設定する。
重要なリスクでなければ,通常の安全性監視
重要な特定されたリスク・重要な潜在的リスクのうち,リスクベネフィットバ
ランス及び公衆衛生への影響を踏まえ,リスク最小化に寄与する懸念
事項かを明確にし,懸念事項に対して科学的に適切な対処方法を
E2Eの医薬品安全性監視方法から決定する。
重要なリスクであっても,リスクベネフィットバランス
や公衆衛生への影響が低いものや既存の情報
でリスク最小化が実施可能なものは,通常の安
全性監視
• ステップ1では「重要なリスク」かどうかの判断を行
う
• ステップ2では「重要なリスク」の中から,リスクベネ
フィットバランスや公衆衛生への影響,さらに,リ
スク最小化に寄与する懸念事項か否か(既存の
情報でリスク最小化を行えるか否か)を検討し,
追加の安全性監視活動が必要かを判断する
• ステップ3,4は変更しない
このような改訂をすることで,欧米と同様の考え方で
日本の追加の安全性監視が行われていることの理解
が進み,ドラッグロス・ラグの課題の一助となる
8/8