よむ、つかう、まなぶ。
【資料1】柏谷構成員提出資料 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36390.html |
| 出典情報 | 創薬力の強化・安定供給の確保等のための薬事規制のあり方に関する検討会(第5回 11/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
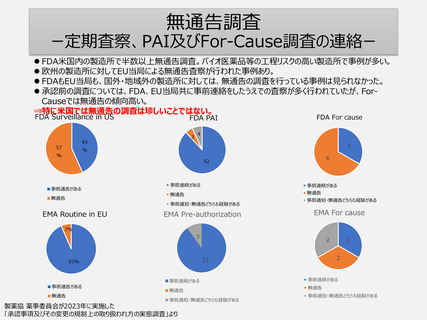
無通告調査
ー定期査察、PAI及びFor-Cause調査の連絡ー
FDA米国内の製造所で半数以上無通告調査。バイオ医薬品等の工程リスクの高い製造所で事例が多い。
欧州の製造所に対してEU当局による無通告査察が行われた事例あり。
FDAもEU当局も、国外・地域外の製造所に対しては、無通告の調査を行っている事例は見られなかった。
承認前の調査については、FDA、EU当局共に事前連絡をしたうえでの査察が多く行われていたが、ForCauseでは無通告の傾向高い。
⇒特に米国では無通告の調査は珍しいことではない。
FDA Surveillance in US
FDA PAI
3
43
57
FDA For cause
4
3
%
%
6
52
■事前通告がある
■無通告
事前連絡がある
事前連絡がある
無通告
無通告
事前通知・無通告どちらも経験がある
EMA Routine in EU
EMA Pre-authorization
7%
■無通告
EMA For cause
3
2
事前連絡がある
無通告
事前通知・無通告どちらも経験がある
製薬協 薬事委員会が2023年に実施した
「承認事項及びその変更の規制上の取り扱われ方の実態調査」より
2
2
27
93%
■事前通告がある
事前通知・無通告どちらも経験がある
事前連絡がある
無通告
事前通知・無通告どちらも経験がある
ー定期査察、PAI及びFor-Cause調査の連絡ー
FDA米国内の製造所で半数以上無通告調査。バイオ医薬品等の工程リスクの高い製造所で事例が多い。
欧州の製造所に対してEU当局による無通告査察が行われた事例あり。
FDAもEU当局も、国外・地域外の製造所に対しては、無通告の調査を行っている事例は見られなかった。
承認前の調査については、FDA、EU当局共に事前連絡をしたうえでの査察が多く行われていたが、ForCauseでは無通告の傾向高い。
⇒特に米国では無通告の調査は珍しいことではない。
FDA Surveillance in US
FDA PAI
3
43
57
FDA For cause
4
3
%
%
6
52
■事前通告がある
■無通告
事前連絡がある
事前連絡がある
無通告
無通告
事前通知・無通告どちらも経験がある
EMA Routine in EU
EMA Pre-authorization
7%
■無通告
EMA For cause
3
2
事前連絡がある
無通告
事前通知・無通告どちらも経験がある
製薬協 薬事委員会が2023年に実施した
「承認事項及びその変更の規制上の取り扱われ方の実態調査」より
2
2
27
93%
■事前通告がある
事前通知・無通告どちらも経験がある
事前連絡がある
無通告
事前通知・無通告どちらも経験がある