よむ、つかう、まなぶ。
材-4○ 医療機器業界からの意見聴取について (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212455_00033.html |
| 出典情報 | 中央社会保険医療協議会 保険医療材料専門部会(第121回 8/30)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
A.イノベーション評価 ①有用性・革新性の評価
ー 市場性評価について ー
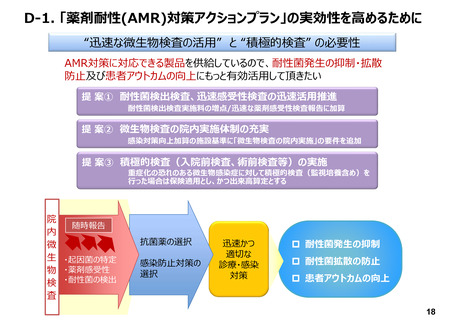
提案 ②
医療的アンメットニーズである、測定検体数が少ないことが想定される項目の開発・上市を
推進するため、市場性評価を行い、加算を要望する。
開発促進の障害になる事象に関する検証(アンケートより)
• 点数に対する予見性がない
• 利益が多く見込めない項目に対する開発投資には慎重にならざるをえない
(市場規模が小さく企業規模が小さいため、検体数が多いことが想定される製品の開発を優先)
• 加算は上限10%等ではなく、予測される販売数も考慮したインセンティブがつくことが必要
(検査数が極端に少ない項目もあることから、測定数に応じた加算が必要)
• 実際に想定より検査数が少なかったとしても販売中止も困難 (1社のみで販売する可能性が高い)
市場性加算とその後の推察
• 検査数が少なく企業が開発してこなかった検査は予見性等が高まることにより一部開発の可能性あり
• 市場性加算があっても開発に躊躇する場合
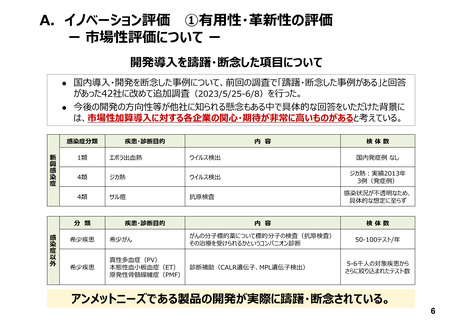
• 緊急対応 (エボラ出血熱、ジカ熱、エムポックス等々)
• 承認申請などに対し、手当をされている場合もあるが、時限的対応の場合も多く企業側の負担が多いため、何らかの
保証(国の買い取り等)が重要。→ ほとんど販売されなくても販売中止も困難:抗原等原料、ラインの確保等々
5
ー 市場性評価について ー
提案 ②
医療的アンメットニーズである、測定検体数が少ないことが想定される項目の開発・上市を
推進するため、市場性評価を行い、加算を要望する。
開発促進の障害になる事象に関する検証(アンケートより)
• 点数に対する予見性がない
• 利益が多く見込めない項目に対する開発投資には慎重にならざるをえない
(市場規模が小さく企業規模が小さいため、検体数が多いことが想定される製品の開発を優先)
• 加算は上限10%等ではなく、予測される販売数も考慮したインセンティブがつくことが必要
(検査数が極端に少ない項目もあることから、測定数に応じた加算が必要)
• 実際に想定より検査数が少なかったとしても販売中止も困難 (1社のみで販売する可能性が高い)
市場性加算とその後の推察
• 検査数が少なく企業が開発してこなかった検査は予見性等が高まることにより一部開発の可能性あり
• 市場性加算があっても開発に躊躇する場合
• 緊急対応 (エボラ出血熱、ジカ熱、エムポックス等々)
• 承認申請などに対し、手当をされている場合もあるが、時限的対応の場合も多く企業側の負担が多いため、何らかの
保証(国の買い取り等)が重要。→ ほとんど販売されなくても販売中止も困難:抗原等原料、ラインの確保等々
5