よむ、つかう、まなぶ。
総-2○再生医療等製品の医療保険上の取扱いについて (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000212500_00185.html |
| 出典情報 | 中央社会保険医療協議会 総会(第544回 5/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
製品概要
販売名
使用目的
ビズノバ
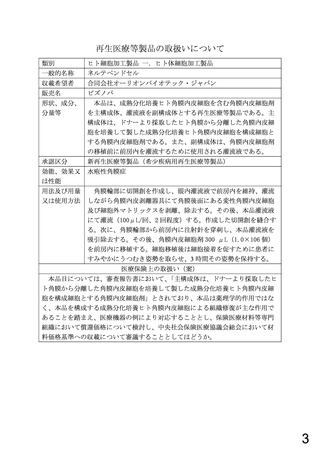
本品は、ヒト角膜より分離・培養して製した成熟分化培養ヒト角膜内皮細胞を含む角
膜内皮細胞剤を主構成体、灌流液を副構成体とする再生医療等製品であり、 水疱性
角膜症患者の前房内に移植することで角膜内皮細胞欠損部分に接着・伸展し、障害さ
れた単層角膜内皮組織を再建、角膜の透明性を回復させることを目的に使用される。
角膜輪部を切開し、眼内灌流液で前房内を
維持・灌流しながら角膜後面にある変性角膜
内皮細胞及び細胞外マトリックスを剥離、除
去する。その後、本品灌流液で灌流する。作
成した切開創を縫合する。次に、角膜輪部か
主な使用方法
ら前房内に注射針を穿刺し、本品灌流液を
吸引除去する。その後、角膜内皮細胞剤を
前房内に移植する。細胞移植後は、細胞接
着を促すために患者に速やかにうつむき姿
勢を取らせ、3時間その姿勢を保持する。
主な有用性
本品は成熟分化培養ヒト角膜内皮細胞で構成される角膜内皮細胞剤が主構成体で
あり、水疱性角膜症患者の前房内に移植することで、障害を受けた単層角膜内皮組織
が再建される。
国内第Ⅲ相検証的医師主導試験において、水疱性角膜症を有し、「最良矯正視力が
0.5未満」、「角膜内皮細胞密度が500個/mm2未満又は観察不可」、「角膜厚が630μm
以上かつ角膜上皮浮腫が存在」の全てを満たす患者12 例(表1)に対し、本品を前房内
へ移植する非盲検非対照試験が実施された。主要評価項目である角膜内皮細胞密度
について、移植後24週に1000個/mm2以上が達成された被験者の割合は100.0%(12例
中12例)であった。また、移植前及び移植後24週における角膜内皮細胞密度、角膜厚
及び最良矯正視力は表2のとおりであった。
表1
水疱性角膜症の要因
例
フックス角膜内皮ジストロフィ
5
フックス角膜内皮ジストロフィ+その他
1
偽水晶体眼水疱性角膜症+その他
1
落屑症候群関連水疱性角膜症
1
落屑症候群関連水疱性角膜症
+偽水晶体眼水疱性角膜症
その他
承認条件
表2
1
3
1.水疱性角膜症に関連する十分な知識及び経験を有する医師が本品の使用方法に関
する技能や手技に伴う合併症等の知識を十分に習得した上で、水疱性角膜症の治療
に係る体制が整った医療機関において「効能、効果又は性能」並びに「用法及び用量
又は使用方法」を遵守して本品を用いるよう、関連学会との協力により作成された適正
使用指針の周知、講習の実施等、必要な措置を講ずること。
2.治験症例が極めて限られていることから、製造販売後、一定数の症例に係るデータが
集積されるまでの間は、全症例を対象に使用の成績に関する調査を実施することによ
り、本品使用患者の背景情報を把握するとともに、本品の安全性及び有効性に関する
データを早期に収集し、本品の適正使用に必要な措置を講ずること。
5
〇
販売名
使用目的
ビズノバ
本品は、ヒト角膜より分離・培養して製した成熟分化培養ヒト角膜内皮細胞を含む角
膜内皮細胞剤を主構成体、灌流液を副構成体とする再生医療等製品であり、 水疱性
角膜症患者の前房内に移植することで角膜内皮細胞欠損部分に接着・伸展し、障害さ
れた単層角膜内皮組織を再建、角膜の透明性を回復させることを目的に使用される。
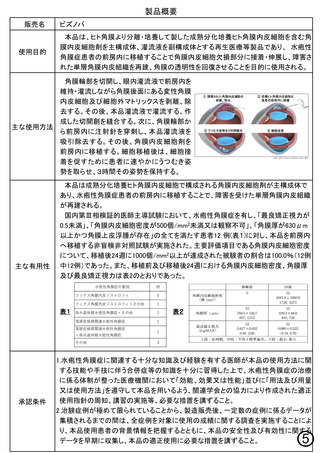
角膜輪部を切開し、眼内灌流液で前房内を
維持・灌流しながら角膜後面にある変性角膜
内皮細胞及び細胞外マトリックスを剥離、除
去する。その後、本品灌流液で灌流する。作
成した切開創を縫合する。次に、角膜輪部か
主な使用方法
ら前房内に注射針を穿刺し、本品灌流液を
吸引除去する。その後、角膜内皮細胞剤を
前房内に移植する。細胞移植後は、細胞接
着を促すために患者に速やかにうつむき姿
勢を取らせ、3時間その姿勢を保持する。
主な有用性
本品は成熟分化培養ヒト角膜内皮細胞で構成される角膜内皮細胞剤が主構成体で
あり、水疱性角膜症患者の前房内に移植することで、障害を受けた単層角膜内皮組織
が再建される。
国内第Ⅲ相検証的医師主導試験において、水疱性角膜症を有し、「最良矯正視力が
0.5未満」、「角膜内皮細胞密度が500個/mm2未満又は観察不可」、「角膜厚が630μm
以上かつ角膜上皮浮腫が存在」の全てを満たす患者12 例(表1)に対し、本品を前房内
へ移植する非盲検非対照試験が実施された。主要評価項目である角膜内皮細胞密度
について、移植後24週に1000個/mm2以上が達成された被験者の割合は100.0%(12例
中12例)であった。また、移植前及び移植後24週における角膜内皮細胞密度、角膜厚
及び最良矯正視力は表2のとおりであった。
表1
水疱性角膜症の要因
例
フックス角膜内皮ジストロフィ
5
フックス角膜内皮ジストロフィ+その他
1
偽水晶体眼水疱性角膜症+その他
1
落屑症候群関連水疱性角膜症
1
落屑症候群関連水疱性角膜症
+偽水晶体眼水疱性角膜症
その他
承認条件
表2
1
3
1.水疱性角膜症に関連する十分な知識及び経験を有する医師が本品の使用方法に関
する技能や手技に伴う合併症等の知識を十分に習得した上で、水疱性角膜症の治療
に係る体制が整った医療機関において「効能、効果又は性能」並びに「用法及び用量
又は使用方法」を遵守して本品を用いるよう、関連学会との協力により作成された適正
使用指針の周知、講習の実施等、必要な措置を講ずること。
2.治験症例が極めて限られていることから、製造販売後、一定数の症例に係るデータが
集積されるまでの間は、全症例を対象に使用の成績に関する調査を実施することによ
り、本品使用患者の背景情報を把握するとともに、本品の安全性及び有効性に関する
データを早期に収集し、本品の適正使用に必要な措置を講ずること。
5
〇
関連画像
ページ内で利用されている画像ファイルです。
有料会員登録をして頂くことで、このページ内で利用されている画像を個別に閲覧・ダウンロードすることができるようになります。