よむ、つかう、まなぶ。
○1 患者申出療養の中間報告について患-2 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00020.html |
| 出典情報 | 患者申出療養評価会議(第33回 9/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
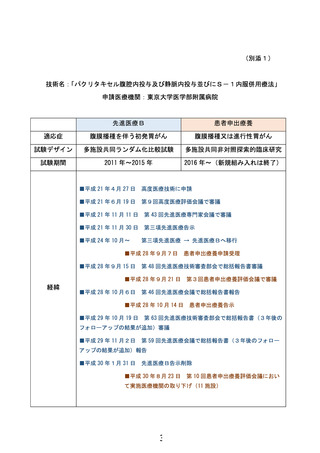
(別添2)
先進医療B
患者申出療養
169 例
症例数
111 例
( S - 1 + パ クリ タキ セ ル 経 静
(2016 年 10 月~2017 年 6 月の期
脈・腹腔内併用療法群:116 例、S
間で、19 施設より 111 例が登録さ
- 1 + シ ス プ ラチ ン併 用 療 法 群
れ、109 例に試験治療が実施)
(対照群):53 例)
主要評価項目
全生存期間
有害事象発現状況
副次評価項目
抗腫瘍効果、安全性
全生存期間、奏効割合
腹腔洗浄細胞診陰性化割合
主要評価項目である全生存期間の
FAS 対象の主解析では、対照群に対
する優越性は示されなかった。
試験結果
後治療に関する違反例(対照群で
腹腔内化学療法を受けた6例)を
除外した PPS 解析や、腹水量を調
整した解析においては、生存期間
に統計学的有意差を認めた。
なお、主解析の 1 年後の追跡調査
の結果では、探索的な全生存期間
の層別ログランク検定で有意差は
あり、主解析の結果と比較して差
が開く傾向を認めた。
4
試験継続中
中間報告(令和4年8月 10 日作成)
において、
●有害事象発現状況(CTCAE Grade
3以上の発現頻度):血液毒性
38.5%、非血液毒性 43.1%
●全生存期間中央値:19.6 か月
●標的病変を有する8例における奏
効割合:25%
●腹腔洗浄細胞診陰性化割合:70%
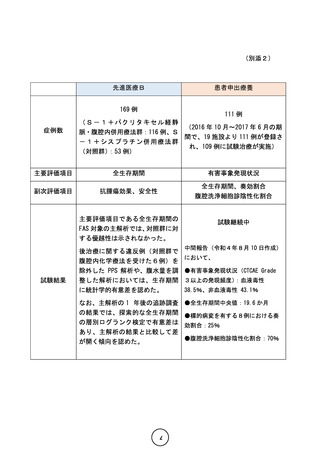
先進医療B
患者申出療養
169 例
症例数
111 例
( S - 1 + パ クリ タキ セ ル 経 静
(2016 年 10 月~2017 年 6 月の期
脈・腹腔内併用療法群:116 例、S
間で、19 施設より 111 例が登録さ
- 1 + シ ス プ ラチ ン併 用 療 法 群
れ、109 例に試験治療が実施)
(対照群):53 例)
主要評価項目
全生存期間
有害事象発現状況
副次評価項目
抗腫瘍効果、安全性
全生存期間、奏効割合
腹腔洗浄細胞診陰性化割合
主要評価項目である全生存期間の
FAS 対象の主解析では、対照群に対
する優越性は示されなかった。
試験結果
後治療に関する違反例(対照群で
腹腔内化学療法を受けた6例)を
除外した PPS 解析や、腹水量を調
整した解析においては、生存期間
に統計学的有意差を認めた。
なお、主解析の 1 年後の追跡調査
の結果では、探索的な全生存期間
の層別ログランク検定で有意差は
あり、主解析の結果と比較して差
が開く傾向を認めた。
4
試験継続中
中間報告(令和4年8月 10 日作成)
において、
●有害事象発現状況(CTCAE Grade
3以上の発現頻度):血液毒性
38.5%、非血液毒性 43.1%
●全生存期間中央値:19.6 か月
●標的病変を有する8例における奏
効割合:25%
●腹腔洗浄細胞診陰性化割合:70%