よむ、つかう、まなぶ。
【参考資料1】医薬品等行政評価・監視委員会の概要等 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27999.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第9回 9/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
改正薬機法等における規定
○ 厚生労働省に、医薬品等行政の監視・評価機能を果たす「医薬品等行政評価・監視委員会」を設置
※ 施行は令和2年9月1日付け
委員会の所掌(法第76条3の5)
※ 薬食審の所掌に属するものは除く
(1)施策の実施状況の評価・監視
医薬品、医薬部外品、化粧品、医療機器及び再生医療等製品(医薬品等)に関する以下の施策の実施状況の評価、監視を行う
①安全性の確保、②医薬品等の使用に関する保健衛生上の危害の発生・拡大の防止
※ 個別の医薬品等の安全性に関する最終的な評価は、従来どおり、薬事・食品衛生審議会が行う。
(2)厚生労働大臣への意見、勧告
施策の実施状況の評価・監視の結果を踏まえ、必要に応じて、安全性の確保等のために講ずべき施策を厚生労働大臣に意見又
は勧告
※ 当該意見等の内容は、遅滞なく公表
※ 厚生労働大臣は、当該意見等に基づき講じた施策を委員会に報告
委員会の規定等
① 委員会の委員は、独立してその職権を行う(法第76条3の6)
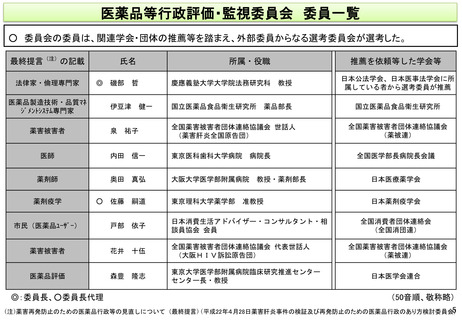
② 委員は10名以内(臨時委員、専門委員を置くことができる)(法第76条3の8)
※ 委員は、医薬品等の安全性の確保等に関して優れた識見を有する者のうちから、厚生労働大臣が任命
③ 関係行政機関の長に対し、①情報収集、②資料提出、③意見表明等、必要な協力を求めることができる(法第76条3の7)
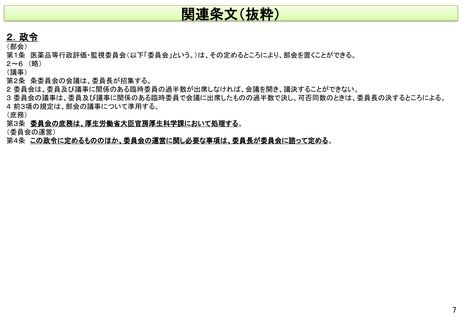
④ 委員会の庶務は、厚生科学課が行う(令第3条)
法:医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律
令:医薬品等行政評価・監視委員会令
3
○ 厚生労働省に、医薬品等行政の監視・評価機能を果たす「医薬品等行政評価・監視委員会」を設置
※ 施行は令和2年9月1日付け
委員会の所掌(法第76条3の5)
※ 薬食審の所掌に属するものは除く
(1)施策の実施状況の評価・監視
医薬品、医薬部外品、化粧品、医療機器及び再生医療等製品(医薬品等)に関する以下の施策の実施状況の評価、監視を行う
①安全性の確保、②医薬品等の使用に関する保健衛生上の危害の発生・拡大の防止
※ 個別の医薬品等の安全性に関する最終的な評価は、従来どおり、薬事・食品衛生審議会が行う。
(2)厚生労働大臣への意見、勧告
施策の実施状況の評価・監視の結果を踏まえ、必要に応じて、安全性の確保等のために講ずべき施策を厚生労働大臣に意見又
は勧告
※ 当該意見等の内容は、遅滞なく公表
※ 厚生労働大臣は、当該意見等に基づき講じた施策を委員会に報告
委員会の規定等
① 委員会の委員は、独立してその職権を行う(法第76条3の6)
② 委員は10名以内(臨時委員、専門委員を置くことができる)(法第76条3の8)
※ 委員は、医薬品等の安全性の確保等に関して優れた識見を有する者のうちから、厚生労働大臣が任命
③ 関係行政機関の長に対し、①情報収集、②資料提出、③意見表明等、必要な協力を求めることができる(法第76条3の7)
④ 委員会の庶務は、厚生科学課が行う(令第3条)
法:医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律
令:医薬品等行政評価・監視委員会令
3